Протеините
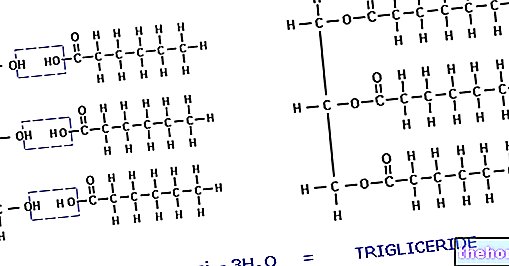
Протеините са полимерни молекули, съставени от повече от 100 аминокиселини свързани с пептидни връзки (по -късите аминокиселинни вериги се наричат полипептиди или пептиди); структурата на протеините може да бъде повече или по -малко дълга, сгъната обратно върху себе си и фиксирана към други молекули (фактори, които определят тяхната сложност и характеризират тяхната биологична функция). Тези структури могат да бъдат класифицирани в: първична структура, вторична структура (α-спирала и β-лист), третична структура и четвъртична структура.


Функции на протеините
В природата протеините изпълняват много функции и най -известната несъмнено е структурната; просто си помислете, че всяка тъканна матрица на нашия организъм се основава на скелет или полимерна мозайка, образувана от пептиди (напр. Мускулни влакна, костен матрикс, тъканна връзка и, от определена гледна точка, дори кръв).
Не по-малко важна е функцията на биорегулация и химическо / хормонално посредничество, всъщност протеините са основните съставки както на ензимите, така и на много хормони.
В кръвта протеините също изпълняват много важна транспортна функция; това е случаят с хемоглобин (транспорт на кислород), трансферрин (транспорт на желязо), албумин (транспорт на липидни молекули) и т.н.
Винаги в кръвния поток протеините се оказват полезни като имунна защита; те съставляват АНТИТЕЛИТЕ, основни молекули, произвеждани от лимфоцитите, полезни за реакцията на организма срещу патогени.
И накрая, протеините - но по -точно аминокиселините - могат да се използват за енергийни цели чрез чернодробна неоглюкогенеза и да осигурят 4 килокалории (kcal) на грам. Това е доста сложен процес, който чрез трансаминиране и дезаминиране позволява на организма да произвежда глюкоза при хипогликемични състояния (вероятно предизвикани от гладуване, особено интензивно и / или продължително мускулно усилие, неблагоприятни патологични или клинични състояния и др.). Неоглюкогенни аминокиселини също могат да бъдат кетогенни, така че тяхното превръщане определя освобождаването на киселинни молекули, наречени кетонови тела.
NB. Енергийната функция на протеините трябва да бъде пределна и подчинена на тази на захарите и мазнините.
Аминокиселините
Аминокиселините са кватернерни молекули, съставени от въглерод, водород, кислород и азот. Известни са повече от 500 вида и тяхната комбинация различава безброй форми на пептиди. Обикновените, L-аминокиселините, са 20: аланин, аргинин, аспарагин, аспарагинова киселина, цистеин, глутаминова киселина, глутамин, глицин, хистидин, изолевцин, левцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин и валин. От метаболизма на последната е възможно да се получи широк спектър от НЕ-обикновени или случайни аминокиселини, които съставляват главно хормони, ензими или междинни молекули (карнитин, хомоцистеин, креатин, таурин и др.).
Сред обикновените аминокиселини някои НЕ МОГАТ да бъдат синтезирани от организма и се наричат НЕОБХОДИМИ; за възрастния мъж има 9: фенилаланин, левцин, изолевцин, лизин, метионин, треонин, триптофан и валин. При децата има общо 11; към горното се добавят: хистидин и аргинин.
Други класификации на аминокиселините са: въз основа на полярността на техните странични вериги (неутрална полярна, неутрална полярна, киселинен заряд, основен заряд) или въз основа на типа радикална група (хидрофобна, хидрофилна, киселинна, основна, ароматна).
Аминокиселини с разклонена верига
Сред незаменимите има и три аминокиселини, наречени съответно разклонена верига (BCAA): левцин, изолевцин и валин; особеността, която отличава аминокиселините с разклонена верига, е представена от различен метаболитен път на производство на енергия.
Както вече беше обяснено, след трансаминиране-дезаминиране, повечето от аминокиселините могат да бъдат предназначени за неоглюкогенеза и да влязат в цикъла на Кребс под формата на оксалоацетат мразиш пируват. В крайна сметка, ако имаше реална нужда, някои от аминокиселините, присъстващи в кръвния поток, биха влезли в хепатоцитите на черния дроб и излезли под формата на глюкоза; за аминокиселините с разклонена верига това не е така. В сравнение с останалите, ВСАА са молекули, които могат да се използват ПРЯМО от мускулите и тази особеност ги прави много по -ефективни при директно производство на енергия и при преобразуване за възстановяване на гликогеновите резерви; от само себе си се разбира, че ако организмът е достатъчно подхранван, катаболизмът на разклонените аминокиселини представлява почти неуместна неоглюкогенна част; глюкозата ВИНАГИ остава основният енергиен източник, следователно, в условията на ДОСТАТЪЧНА гликемия и гликогенови резерви, дори по време на обикновени спортни постижения няма причина да се страхуваме, че мускулът се нуждае от излишък от аминокиселини с разклонена верига.
Други статии на тема „Протеини и аминокиселини с разклонена верига“
- Аминокиселини с разклонена верига: кога да ги приемаме?
- Диетични протеини
- Разграждане на протеини - кога да го приемате?