Активни съставки: палиперидон
XEPLION 25 mg инжекционна суспензия с удължено освобождаване
XEPLION 50 mg инжекционна суспензия с удължено освобождаване
XEPLION 75 mg инжекционна суспензия с удължено освобождаване
XEPLION 100 mg инжекционна суспензия с удължено освобождаване
XEPLION 150 mg инжекционна суспензия с удължено освобождаване
Показания Защо се използва Xeplion? За какво е?
Xeplion съдържа активното вещество палиперидон, което принадлежи към класа на антипсихотични лекарства и се използва като поддържащо лечение за симптомите на шизофрения при възрастни пациенти, стабилизирани на палиперидон или рисперидон.
Ако в миналото е доказано, че сте реагирали на палиперидон или рисперидон и имате леки до умерени симптоми, Вашият лекар може да започне лечение с Xeplion без предварително стабилизиране с палиперидон или рисперидон.
Шизофренията е заболяване, характеризиращо се с "положителни" и "отрицателни" симптоми. Положително означава излишък от симптоми, които обикновено не присъстват. Например, човек с шизофрения може да чуе гласове или да види неща, които всъщност не съществуват (наречени халюцинации), да вярва в неща, които не са верни (наречени заблуди), или да бъде необичайно подозрителен към другите. Отрицателните симптоми означават липса на поведение или чувства, които обикновено присъстват. Например, човек с шизофрения може да има тенденция да бъде изолиран и може да не реагира емоционално или може да има затруднения да говори ясно и логично. Хората с това разстройство също могат да се чувстват депресирани, тревожни, виновни или напрегнати.
Xeplion може да помогне за облекчаване на симптомите на Вашето заболяване и да предотврати тяхното завръщане.
Противопоказания Когато Xeplion не трябва да се използва
Не използвайте Xeplion
- ако сте алергични към палиперидон или към някоя от останалите съставки на това лекарство (изброени в точка 6).
- ако сте алергични към друго антипсихотично лекарство, включително рисперидон.
Предпазни мерки при употреба Какво трябва да знаете, преди да приемете Xeplion
Говорете с Вашия лекар, фармацевт или медицинска сестра, преди да използвате Xeplion. 4, възможни странични ефекти).
Всички лекарства имат странични ефекти и някои от страничните ефекти на това лекарство могат да влошат симптомите на други заболявания. Поради тази причина е важно да обсъдите с Вашия лекар някое от следните състояния, които потенциално могат да се влошат по време на лечението с това лекарство.
- Ако страдате от Паркинсонова болест.
- Ако някога сте били диагностицирани с заболяване, чиито симптоми включват висока температура и скованост на мускулите (известен също като Невролептичен злокачествен синдром).
- Ако някога сте имали необичайни движения на езика или лицето (Тардивна дискинезия).
- Ако знаете, че в миналото сте имали ниски нива на белите кръвни клетки (което може или не е било причинено от други лекарства).
- Ако сте диабетик или сте предразположени към диабет.
- Ако сте били диагностицирани с рак на гърдата или тумор на хипофизната жлеза в мозъка.
- Ако имате сърдечно заболяване или приемате лечение за сърдечно заболяване, което има тенденция да понижава кръвното Ви налягане.
- Ако имате ниско кръвно налягане, когато се изправите или внезапно преминете от лъжа към седене.
- Ако страдате от епилепсия.
- Ако имате бъбречни проблеми.
- Ако имате проблеми с черния дроб.
- Ако имате продължителна и / или болезнена ерекция.
- Ако имате затруднения с контролирането на основната телесна температура или прекомерни топлинни условия.
- Ако имате необичайно високо ниво на пролактинов хормон в кръвта си или ако имате възможен пролактин-зависим тумор.
- Ако вие или някой друг във вашето семейство имате анамнеза за кръвни съсиреци (тромби), тъй като антипсихотиците са свързани с образуването на кръвни съсиреци.
Ако имате някое от тези състояния, говорете с Вашия лекар, за да може той да прецени дали трябва да коригирате дозата си или да я следвате внимателно за известно време.
Тъй като при пациенти, приемащи това лекарство, много рядко се наблюдава опасно нисък брой на определен вид бели кръвни клетки, необходими за спиране на инфекции в кръвта, Вашият лекар може да провери броя на белите Ви кръвни клетки.
Въпреки че преди това сте понасяли перорален палиперидон или перорален рисперидон, рядко се появяват алергични реакции след инжектиране на Xeplion. Потърсете незабавно Вашия лекар, ако получите обрив, подуване на гърлото, сърбеж или проблеми с дишането, тъй като това може да са признаци на тежка алергична реакция.
Това лекарство може да причини наддаване на тегло. Значителното наддаване на тегло може да повлияе неблагоприятно на здравето. Вашият лекар трябва редовно да Ви претегля.
Тъй като при пациенти, приемащи това лекарство, се наблюдава захарен диабет или влошаване на съществуващ захарен диабет, Вашият лекар трябва да провери за високи нива на кръвната захар. При пациенти с предшестващ захарен диабет нивото на кръвната захар трябва да се следи редовно.
Тъй като това лекарство може да намали желанието за повръщане, има вероятност да прикрие нормалната реакция на организма при поглъщане на токсични вещества или други медицински състояния.
По време на „операция на окото“ поради помътняване на лещата (катаракта), зеницата (черният кръг в центъра на окото) може да не се увеличи по размер, ако е необходимо. Също така, ирисът (оцветената част на окото) може да стане отпуснат по време на операцията, което може да причини увреждане на окото. Ако планирате операция на очите, не забравяйте да кажете на офталмолога си, че приемате това лекарство.
Деца и юноши
Това лекарство не трябва да се използва при деца и юноши под 18 години.
Взаимодействия Кои лекарства или храни могат да променят ефекта на Xeplion
Уведомете Вашия лекар, ако приемате, наскоро сте приемали или е възможно да приемете други лекарства.
Приемът на това лекарство с карбамазепин (антиепилептик и стабилизатор на настроението) може да наложи коригиране на дозата на това лекарство.
Тъй като това лекарство действа главно върху мозъка, намесата с други лекарства (или алкохол), които действат върху мозъка, като други психиатрични лекарства, опиати, антихистамини и лекарства за нарушения на съня, може да причини „преувеличаване на странични ефекти като сънливост или други ефекти върху мозъка.
Тъй като това лекарство може да понижи кръвното налягане, бъдете внимателни, когато това лекарство се използва с други лекарства, които понижават кръвното налягане.
Това лекарство може да намали ефекта на лекарствата, използвани за лечение на болестта на Паркинсон и синдрома на неспокойните крака (напр. Леводопа).
Това лекарство може да причини "аномалия на електрокардиограмата (ЕКГ)", която се характеризира с по -дълъг период за прогресиране на електрически импулс през определена част на сърцето (известен като "удължаване на" QT интервала "). Други лекарства, които тези ефекти включват някои лекарства, използвани за лечение на сърдечен ритъм или за лечение на инфекции и други антипсихотици Важно е да информирате Вашия лекар за всички лекарства, които приемате за лечение на тези състояния.
Ако сте предразположени към развитие на гърчове, това лекарство може да увеличи шансовете Ви да ги получите. Други лекарства, които имат този ефект, включват някои лекарства, използвани за лечение на депресия или инфекции и други антипсихотици. Важно е да уведомите Вашия лекар за всички лекарства, които приемате за лечение на тези състояния.
Предупреждения Важно е да знаете, че:
Бременност и кърмене
Ако сте бременна или кърмите, мислите, че може да сте бременна или планирате бременност, посъветвайте се с Вашия лекар или фармацевт, преди да приемете това лекарство. Не трябва да използвате това лекарство по време на бременност, освен ако вече не сте обсъдили това с Вашия лекар. Следните симптоми могат да се появят при новородени бебета, на майки, които са използвали палиперидон през последния триместър (последните три месеца от бременността): треперене, скованост на мускулите и / или слабост, сънливост, възбуда, проблеми с дишането и затруднено хранене. Вашето дете има някой от тези симптоми, може да се наложи да се свържете с Вашия лекар.
Това лекарство може да преминава от майка на бебе чрез кърмата и може да навреди на бебето. Затова не кърмете, ако използвате това лекарство.
Шофиране и работа с машини
По време на лечението с това лекарство могат да възникнат замаяност, силна умора и проблеми със зрението (вж. Точка 4). Това трябва да се има предвид в случаите, когато се изисква пълна бдителност, например при шофиране на кола или работа с машини.
Важна информация за някои от съставките на Xeplion
Нормалният диапазон на дозиране за този лекарствен продукт съдържа по -малко от 1 mmol (23 mg) натрий на доза; на практика той по същество е „без натрий“.
Доза, метод и време на приложение Как да използвате Xeplion: Дозировка
Това лекарство се дава от Вашия лекар или друг медицински специалист в лекарски кабинет или клиника. Вашият лекар ще реши кога трябва да се върнете в лекарския кабинет или клиниката за инжектиране. Важно е да не пропуснете планираната доза. Ако смятате, че няма да можете да присъствате на срещата с Вашия лекар, свържете се с него незабавно, за да Ви предложи нова може да се уговори.назначаване възможно най -скоро. Ще Ви бъде направена първа инжекция (150 mg) и втора инжекция (100 mg) от това лекарство в горната част на ръката с интервал от приблизително една седмица. След това ще получите инжекция (която може да варира от 25 mg до 150 mg) или в горната част на ръката или седалището веднъж месечно.
Ако Вашият лекар Ви премине от рисперидон с удължено освобождаване към това лекарство, ще получите първата си инжекция от това лекарство (която може да варира от 25 mg до 150 mg) или в горната част на ръката или в задните части на датата, която вече е насрочена за следващата Ви инжекция . След това ще получите инжекция (която може да варира от 25 mg до 150 mg) или в горната част на ръката, или в седалището веднъж месечно.
В зависимост от симптомите, Вашият лекар може да увеличи или намали количеството лекарство, което получавате по време на планираната месечна инжекция с едно ниво на доза.
Пациенти с бъбречни проблеми
Вашият лекар може да коригира дозата на лекарството въз основа на бъбречната Ви функция. Ако имате леки бъбречни проблеми, Вашият лекар може да Ви предпише по -ниска доза. Ако имате умерени до тежки бъбречни проблеми, това лекарство не трябва да се използва.
Възрастни граждани
Вашият лекар може да намали дозата Ви на това лекарство, ако бъбречната Ви функция е намалена.
Предозиране Какво да направите, ако сте приели твърде много Xeplion
Ако сте приели повече от необходимата доза Xeplion
Това лекарство ще Ви бъде дадено под лекарско наблюдение; следователно е малко вероятно да ви бъде дадено твърде много.
Пациентите, които са получили предозиране на палиперидон, могат да получат следните симптоми: сънливост или седация, ускорен пулс, ниско кръвно налягане, анормална електрокардиограма (проследяване на електрическата активност на сърцето) или бавни или необичайни движения на лицето, тялото, ръцете или краката.
Ако спрете да използвате Xeplion
Ако спрете да си инжектирате, ще загубите ефектите на лекарството. Не трябва да спирате употребата на това лекарство, освен ако Вашият лекар не Ви каже, тъй като симптомите Ви могат да се върнат.
Ако имате някакви допълнителни въпроси относно приема на това лекарство, попитайте Вашия лекар или фармацевт
Странични ефекти Какви са страничните ефекти на Xeplion
Както всички лекарства, това лекарство може да предизвика нежелани реакции, въпреки че не всеки ги получава.
Незабавно уведомете Вашия лекар, ако:
- Мислите, че имате кръвни съсиреци във вените си, особено в краката (симптомите включват подуване, болка и зачервяване на краката), които могат да преминават по кръвоносните съдове до белите дробове, причинявайки болка в гърдите и затруднено дишане. Ако забележите някой от тези симптоми, незабавно се консултирайте с Вашия лекар.
- Имате деменция и забелязвате внезапна промяна в психическото си състояние или „внезапна слабост или изтръпване на лицето, ръцете или краката, особено от едната страна, или ако езикът ви е неразбираем, дори и за кратко. Те могат“. да са признаци на инсулт.
- Имате треска, скованост на мускулите, изпотяване или намалено ниво на съзнание (разстройство, наречено „Невролептичен злокачествен синдром“). Може да се наложи незабавно медицинско лечение.
- Той е мъж и има продължителна или болезнена ерекция. Това състояние се нарича приапизъм. Може да се наложи незабавно медицинско лечение.
- Има неволни ритмични движения на езика, устата и лицето. Може да се наложи преустановяване на лечението с палиперидон.
- Имате тежка алергична реакция, характеризираща се с повишена температура, подуване на устата, лицето, устните или езика, задух, сърбеж, кожен обрив и понякога спадане на кръвното налягане (съответстващо на анафилактична реакция). палиперидон, алергични реакции рядко се появяват след инжектиране на Xeplion.
Възможни са следните нежелани реакции:
Много чести: могат да засегнат повече от 1 на 10 души
- трудно заспиване или заспиване
- главоболие
Чести: могат да засегнат до 1 на 10 души
- обикновена настинка, инфекция на пикочните пътища, усещане за грип
- Xeplion може да повиши нивата на хормон, наречен „пролактин“, открит в кръвен тест (който може или не може да причини симптоми). Когато се появят симптоми на високо ниво на пролактин, това може да включва (при мъжете) подуване на гърдите, затруднено поддържане или поддържане на ерекция или друга сексуална дисфункция; (при жените) дискомфорт в гърдите, загуба на мляко от гърдите, менструален цикъл или други проблеми с менструацията ти
- висока кръвна захар, наддаване на тегло, загуба на тегло, повишаване на триглицеридите (мазнини) в кръвта
- възбуда, депресия, тревожност
- паркинсонизъм: Това състояние може да включва бавни или необичайни движения, усещане за скованост или напрежение на мускулите (което прави движенията резки), а понякога дори усещане за движение, което замръзва и след това се рестартира. Други признаци на паркинсонизъм включват бавно разбъркване при ходене, тремор в покой, повишена слюнка и / или лигавене и загуба на изражение на лицето.
- безпокойство, сънливост или загуба на бдителност
- дистония: това е състояние, което включва бавно или продължително неволно свиване на мускулите. Въпреки че може да засегне всяка част от тялото (което води до анормална стойка), дистонията често включва мускулите на лицето, включително необичайни движения на очите, устата, езика или челюстта
- виене на свят
- дискинезия: Това е състояние, което включва неволеви мускулни движения и може да включва повтарящи се, спастични или усукани движения или потрепване.
- тремор
- ниска сърдечна честота, ускорена сърдечна честота
- високо кръвно налягане
- кашлица, запушен нос
- коремна болка, повръщане, гадене, запек, диария, лошо храносмилане, зъбобол
- повишаване на чернодробните трансаминази в кръвта
- обрив
- болка в костите или мускулите, болки в гърба
- треска, слабост, умора (умора)
- реакция на мястото на инжектиране, включително сърбеж, болка или подуване
Нечести: могат да засегнат до 1 на 100 души
- пневмония, гръдна инфекция (бронхит), инфекция на дихателните пътища, синузит, инфекция на пикочния мехур, ушна инфекция, инфекция на очите, тонзилит, кожна инфекция, възпаление на кожата, причинено от акари, абсцес под кожата
- намаляване на броя на белите кръвни клетки, анемия, намаляване на червените кръвни клетки, повишаване на кръвните еозинофили (вид бели кръвни клетки)
- алергична реакция
- диабет или влошаване на диабета, повишаване на инсулина в кръвта (хормон, който контролира нивата на кръвната захар)
- повишен апетит, загуба на апетит, което води до недохранване и ниско телесно тегло
- повишен холестерол в кръвта
- нарушения на съня, повишено настроение (мания), объркване, намален сексуален порив, нервност, кошмари
- късна дискинезия (потрепващи или резки движения, които не можете да контролирате в лицето, езика или други части на тялото). Свържете се незабавно с Вашия лекар, ако почувствате неволни ритмични движения на езика, устата и лицето. Може да се наложи спиране на това лекарство
- гърчове (припадъци), припадък, спешна нужда от преместване на част от тялото, замаяност при изправяне, нарушения на вниманието, проблеми с говора, загуба или необичайно чувство за вкус, намалена чувствителност на кожата към болка и допир, a изтръпване, изтръпване или изтръпване на кожата
- замъглено зрение, инфекция на „окото“ или „леко зачервено“, сухо око
- усещане за въртене (световъртеж), шум в ушите, болка в ушите
- предсърдно мъждене (анормален сърдечен ритъм), прекъсване на проводимостта между горните и долните части на сърцето, анормална електрическа проводимост на сърцето, удължаване на QT интервала на сърцето, ускорен сърдечен ритъм при изправяне, ненормално електрическо проследяване на сърцето ( електрокардиограма или ЕКГ), усещане за състезание или пулсиране в гърдите (сърцебиене)
- ниско кръвно налягане, понижаване на кръвното налягане при изправяне (в резултат на това някои хора, приемащи това лекарство, могат да почувстват припадък, замаяност или припадък при внезапно изправяне или сядане)
- задух, белодробна конгестия, хрипове, болки в гърлото, кървене от носа
- коремен дискомфорт, стомашна или чревна инфекция, сухота в устата, прекомерно преминаване на газове или въздух
- повишаване на GGT в кръвта (чернодробен ензим, наречен гама-глутамилтрансфераза), повишаване на чернодробните ензими в кръвта
- обрив (или копривна треска), сърбеж, косопад, екзема, суха кожа, зачервена кожа, акне
- мускулни спазми, скованост на ставите, болки в шията, болки в ставите
- инконтиненция (липса на контрол) на урината, често уриниране, болка при уриниране
- еректилна дисфункция, нарушение на еякулацията, загуба на менструация, забавена менструация, липса на менструация или други проблеми с менструацията (жени), развитие на гърди при мъже, загуба на кърма, сексуална дисфункция, вагинално течение.
- подуване на лицето, устата, очите или устните, подуване на тялото, ръцете или краката
- промяна в начина, по който ходите
- болка в гърдите, дискомфорт в гърдите, гадене
- втвърдяване на кожата
- падат
Редки: могат да засегнат до 1 на 1 000 души
- гъбична инфекция на ноктите
- опасно нисък брой на определен вид бели кръвни клетки, необходими за борба с инфекциите
- намаляване на определен вид бели кръвни клетки, което служи за защита на организма от инфекция, намаляване на тромбоцитите (кръвни клетки, които помагат за спиране на кървенето)
- тежка алергична реакция, характеризираща се с повишена температура, подуване на устата, лицето, устните или езика, задух, сърбеж, обрив и понякога спад на кръвното налягане,
- неподходяща секреция на хормон, който контролира обема на урината
- опасно прекомерен прием на вода, животозастрашаващи усложнения от неконтролиран диабет
- ниска кръвна захар, прекомерен прием на вода
- липса на емоции
- невъзможност за постигане на оргазъм
- невролептичен злокачествен синдром (объркване, намалена или загуба на съзнание, висока температура и тежка мускулна скованост), внезапна загуба на кръвоснабдяване на мозъка (инсулт или "мини" инсулт), липса на отговор на стимули, загуба на съзнание, ниско ниво на съзнание, нарушения на равновесието
- съдови проблеми в мозъка, кома, причинена от неконтролиран диабет, нарушена координация, тремор в главата
- глаукома (повишено налягане вътре в очната ябълка), проблеми с движението на очите, търкаляне на очите към задната част на главата, свръхчувствителност на очите, повишена сълза, зачервяване на очите
- неравномерен сърдечен ритъм на сърцето
- кръвни съсиреци във вените, особено в краката (симптомите включват подуване, болка и зачервяване на краката), които могат да преминават по кръвоносните съдове до белите дробове, причинявайки болка в гърдите и затруднено дишане. Ако забележите някой от тези симптоми, незабавно се консултирайте с Вашия лекар.
- намален кислород в части от тялото (тъй като притока на кръв намалява), зачервяване
- проблеми с дишането по време на сън (сънна апнея), бързо и плитко дишане, пневмония, причинена от вдишване на храна, задръстване на дихателните пътища, гласови смущения.
- възпаление на панкреаса, запушване на червата, подут език, фекална инконтиненция, много твърди изпражнения, затруднено преглъщане, напукани устни, липса на движение на мускулите на червата, което причинява запушване
- пожълтяване на кожата и очите (жълтеница)
- тежка алергична реакция с подуване, което може да засегне гърлото, което води до затруднено дишане,
- обрив, свързан с наркотици, обезцветяване на кожата, удебеляване на кожата, лющене и сърбеж на скалпа или кожата, пърхот
- разпадане на мускулните влакна и мускулни болки (рабдомиолиза), анормална стойка
- повишаване на CPK (креатин фосфокиназа) в кръвта, ензим, който понякога се освобождава, когато има мускулно увреждане, подуване на ставите, мускулна слабост
- невъзможност за уриниране
- приапизъм (продължителна ерекция на пениса, която може да изисква хирургично лечение)
- болка в гърдите, дискомфорт в гърдите, уголемяване на гърдите, уголемяване на гърдите, изтичане на млечна течност от гърдите
- много ниска телесна температура, понижаване на телесната температура, втрисане, повишаване на телесната температура, чувство на жажда, симптоми на отнемане на лекарството
- натрупване на гной, причинено от инфекция на мястото на инжектиране, дълбока кожна инфекция, киста на мястото на инжектиране, синини на мястото на инжектиране
С неизвестна честота: от наличните данни не може да се направи оценка
- захар в урината Следните нежелани реакции са наблюдавани при употребата на друго лекарство, наречено рисперидон, което е много подобно на палиперидон, така че тези ефекти могат да се очакват и при това лекарство: други видове проблеми с мозъчните кръвоносни съдове, белодробен крепитат, смърт на кожни клетки на мястото на инжектиране и язва на мястото на инжектиране. Очни проблеми могат да възникнат и по време на операция на катаракта. По време на операция на катаракта може да възникне състояние, наречено синдром на интраоперативна дискета (IFIS), ако приемате или сте приемали Xeplion. Ако Ви предстои операция на катаракта, не забравяйте да уведомите Вашия лекар, ако приемате или сте приемали това лекарство.
Докладване на странични ефекти
Ако получите някакви нежелани реакции, говорете с Вашия лекар, фармацевт или медицинска сестра. предоставете повече информация за безопасността на това лекарство
Срок на годност и задържане
Съхранявайте това лекарство на място, недостъпно за деца.
Не използвайте това лекарство след срока на годност, отбелязан върху картонената опаковка.Срокът на годност се отнася до последния ден от месеца.
Да не се съхранява над 30 ° C.
Не изхвърляйте никакви лекарства през отпадни води или битови отпадъци. Попитайте Вашия фармацевт как да изхвърлите лекарства, които вече не използвате. Това ще помогне за опазването на околната среда.
Състав и лекарствена форма
Какво съдържа Xeplion
Активната съставка е палиперидон.
Всяка предварително напълнена спринцовка с Xeplion 25 mg съдържа 39 mg палиперидон палмитат.
Всяка предварително напълнена спринцовка с Xeplion 50 mg съдържа 78 mg палиперидон палмитат.
Всяка предварително напълнена спринцовка с Xeplion 75 mg съдържа 117 mg палиперидон палмитат.
Всяка предварително напълнена спринцовка Xeplion 100 mg съдържа 156 mg палиперидон палмитат.
Всяка предварително напълнена спринцовка с Xeplion 150 mg съдържа 234 mg палиперидон палмитат.
Другите съставки са: полисорбат 20 полиетилен гликол 4000 лимонена киселина монохидрат двунатриев хидроген фосфат безводен натриев дихидроген фосфат монохидрат натриев хидроксид (за регулиране на рН) вода за инжекции
Описание на това как изглежда Xeplion и съдържанието на опаковката
Xeplion е бяла до почти бяла суспензия за инжектиране с удължено освобождаване в предварително напълнена спринцовка.
Всяка опаковка съдържа 1 предварително напълнена спринцовка и 2 игли.
Опаковка за започване на лечението: Всяка опаковка съдържа 1 опаковка Xeplion 150 mg и 1 опаковка Xeplion 100 mg.
Източник на листовката: AIFA (Италианска агенция по лекарствата). Съдържание, публикувано през януари 2016 г. Наличната информация може да не е актуална.
За да имате достъп до най-актуалната версия, препоръчително е да получите достъп до уебсайта на AIFA (Италианска агенция по лекарствата). Отказ от отговорност и полезна информация.
01.0 ИМЕ НА ЛЕКАРСТВЕНИЯ ПРОДУКТ
XEPLION 100 MG ПРОДЪЛЖИТЕЛНО ИЗПУСКАНЕ ИНЖЕКТИРУЕМА СУСПЕНЗИЯ
02.0 КАЧЕСТВЕН И КОЛИЧЕСТВЕН СЪСТАВ
Всяка предварително напълнена спринцовка съдържа 156 mg палиперидон палмитат, еквивалентен на 100 mg палиперидон.
За пълния списък на помощните вещества вижте точка 6.1.
03.0 ЛЕКАРСТВЕНА ФОРМА
Инжекционна суспензия с удължено освобождаване.
Суспензията е бяла до почти бяла на цвят. Суспензията е с неутрално рН (приблизително 7,0).
04.0 КЛИНИЧНА ИНФОРМАЦИЯ
04.1 Терапевтични показания
XEPLION е показан за поддържаща терапия на шизофрения при възрастни пациенти, стабилизирани на палиперидон или рисперидон.
При избрани възрастни пациенти с шизофрения и които преди това са реагирали на перорален палиперидон или рисперидон, XEPLION може да се използва без предварително орално стабилизиране, ако психотичните симптоми са леки до умерени и е необходимо продължително инжекционно лечение.
04.2 Дозировка и начин на приложение
Дозировка
Препоръчва се XEPLION да започне с доза от 150 mg на ден 1 от лечението и доза от 100 mg една седмица по -късно (ден 8), като и в двата случая се прилага в делтоидния мускул, за да се постигнат бързо терапевтични концентрации (вж. Точка 5.2 ). Третата доза трябва да се приложи един месец след втората доза. Препоръчителната месечна поддържаща доза е 75 mg; някои пациенти могат да се възползват от по-ниски или по-високи дози в препоръчителния диапазон от 25-150 mg въз основа на субективната поносимост и / или ефикасността. Пациентите с наднормено тегло или със затлъстяване може да изискват дози, близки до горните граници (вж. Точка 5.2). След втората доза могат да се прилагат месечни поддържащи дози както в делтоидния мускул, така и в седалището.
"Корекция на поддържащата доза може да се прави ежемесечно. Когато се правят корекции на дозата, трябва да се вземат предвид характеристиките на XEPLION с удължено освобождаване (вж. Точка 5.2), тъй като пълният ефект от поддържащите дози може да не е очевиден за няколко" месеца.
Преминаване от перорален палиперидон или перорален рисперидон
В началната фаза на лечение с XEPLION може да се отмени предишния перорален палиперидон или перорален рисперидон. XEPLION трябва да се стартира, както е описано по -горе в началото на раздел 4.2.
Преминаване от инжекционен рисперидон към удължено освобождаване
Когато пациентите преминат от инжекционен рисперидон към удължено освобождаване, започнете терапия с XEPLION вместо следващата планирана инжекция. След това XEPLION трябва да продължи на месечни интервали. Първоначалната схема на дозиране от седмица 1, която включва интрамускулни инжекции (съответно на ден 1 и ден 8), както е описано в точка 4.2, не се изисква.
Пациентите, стабилизирани преди това с различни дози инжекционен рисперидон с удължено освобождаване, могат да постигнат подобна стабилна експозиция на палиперидон по време на поддържащо лечение с месечни дози XEPLION съгласно следната схема:
Дози с инжектируем рисперидон с удължено освобождаване и XEPLION, необходими за постигане на подобна експозиция в равновесно състояние на палиперидон
Прекратяването на антипсихотичните лекарства трябва да се извърши в съответствие с подходящата информация за предписване. Ако XEPLION бъде преустановен, трябва да се вземат предвид характеристиките му с удължено освобождаване. Както се препоръчва и за други антипсихотични лекарства, необходимостта от продължаване на всички съществуващи антипсихотични лекарства. Екстрапирамидни симптоми (EPS , Екстрапирамидни симптоми) трябва да се преразглеждат периодично.
Пропусната доза
Как да избегнете пропускане на доза
Препоръчва се втората доза от началната фаза на терапията с XEPLION да се прилага една седмица след първата доза. За да се избегне пропускане на доза, втората доза може да се даде на пациенти 4 дни преди или 4 дни след едноседмичния срок (ден 8). По същия начин, след началната фаза, се препоръчва третата инжекция и следващите инжекции да се правят веднъж месечно. За да се избегне пропускане на месечна доза, пациентите могат да се инжектират до 7 дни преди или 7 дни след изтичането на месечния срок.
Ако планираната дата за втората инжекция на XEPLION (ден 8 ± 4 дни) е изтекла, препоръчителният начин за възобновяване на терапията зависи от времето, което е изминало от първата инжекция на пациента.
Пропусната втора доза от началната фаза (
Ако са минали по -малко от 4 седмици от първата инжекция, тогава на пациента трябва да се направи втората инжекция от 100 mg в делтоидния мускул възможно най -скоро. Трета инжекция от 75 mg XEPLION в делтоидния или седалищния мускул трябва да се направи 5 седмици след първата инжекция (независимо от това кога е била поставена втората инжекция). След това трябва да се следва нормалният месечен курс на инжекции в делтоидния или глутеусния мускул от 25-150 mg, въз основа на индивидуалната поносимост и / или ефикасността на пациента.
Пропусната втора доза от началната фаза (4-7 седмици след първата инжекция)
Ако са изминали 4 до 7 седмици от първата инжекция на XEPLION, възстановете дозата с две инжекции от 100 mg, както следва:
1. инжекция в делтоида възможно най -скоро
2. още една инжекция в делтоида една седмица по -късно
3. възобновяване на нормалния месечен цикъл на инжекции в делтоидния или седалищния мускул от 25-150 mg, въз основа на индивидуалната поносимост и / или ефикасността на пациента.
Пропусната втора доза от началната фаза (> 7 седмици след първата инжекция)
Ако са минали повече от 7 седмици от първата инжекция на XEPLION, започнете приложението, както е описано в препоръките за началната фаза на XEPLION, посочени по -горе.
Пропусната месечна поддържаща доза (от 1 месец до 6 седмици)
След началната фаза препоръчителният курс на инжектиране на XEPLION е месечен. Ако са минали по -малко от 6 седмици от последната инжекция, тогава предварително зададената доза трябва да се приложи възможно най -скоро, последвана от инжекции на месечни интервали.
Пропусната месечна поддържаща доза (> 6 седмици до 6 месеца)
Ако са минали повече от 6 седмици от последната инжекция на XEPLION, препоръките са следните:
За пациенти, стабилизирани с дози от 25 до 100 mg:
1. инжекция с делтоид възможно най -скоро в същата доза, с която пациентът е стабилизиран преди това
2. друга инжекция с делтоид (същата доза) една седмица по -късно (ден 8)
3. възобновяване на нормалния месечен цикъл на инжекции в делтоидния или седалищния мускул от 25-150 mg, въз основа на индивидуалната поносимост и / или ефикасността на пациента.
За пациенти, стабилизирани със 150 mg:
1. инжекция в делтоида възможно най -скоро в доза от 100 mg
2. друга инжекция с делтоид една седмица по -късно (ден 8) в доза от 100 mg
3. възобновяване на нормалния месечен цикъл на инжекции в делтоидния или седалищния мускул от 25-150 mg, въз основа на индивидуалната поносимост и / или ефикасността на пациента.
Пропусната месечна поддържаща доза (> 6 месеца). Ако са минали повече от 6 месеца от последната инжекция на XEPLION, започнете дозирането, както е описано в препоръките за началната фаза на XEPLION, посочени по -горе.
Специални популации
Възрастно население
Ефикасността и безопасността при лица на възраст> 65 години не са установени.
Като цяло препоръчителната дозировка на XEPLION за възрастни пациенти с нормална бъбречна функция е същата като за по -млади възрастни пациенти с нормална бъбречна функция. Въпреки това, тъй като по -възрастните пациенти могат да имат нарушена бъбречна функция, може да се наложи коригиране на дозата (вж. Точка Бъбречна недостатъчност по -долу за препоръки за дозиране при пациенти с бъбречна недостатъчност).
Бъбречна недостатъчност
XEPLION не е систематично проучен при пациенти с бъбречна недостатъчност (вж. Точка 5.2). При пациенти с леко бъбречно увреждане (креатининов клирънс ≥ 50 до
XEPLION не се препоръчва при пациенти с умерено или тежко бъбречно увреждане (креатининов клирънс
Чернодробна недостатъчност
Въз основа на опита с перорален палиперидон не се налага коригиране на дозата при пациенти с леко до умерено чернодробно увреждане.Тъй като палиперидон не е проучен при пациенти с тежко чернодробно увреждане, се препоръчва повишено внимание при такива пациенти.
Други специални популации
Не се препоръчва коригиране на дозата за XEPLION въз основа на пол, раса или статус на пушач.
Педиатрична популация
Безопасността и ефикасността на XEPLION при деца на възраст под 18 години не са установени. Няма налични данни.
Начин на приложение
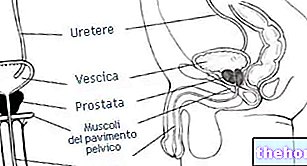
XEPLION е само за интрамускулна употреба. Трябва да се инжектира бавно и дълбоко в мускула. Всяка инжекция трябва да се прилага от медицински специалист. Приложението трябва да се извършва в една инжекция. Дозата не трябва да се прилага като отделни инжекции. Дозата не трябва да се прилага интравенозно или подкожно.
Дозите на 1 и 8 ден от началната фаза трябва да се прилагат и в делтоидния мускул, за да се постигнат бързо терапевтични концентрации (вж. Точка 5.2). След втората доза могат да се прилагат месечни поддържащи дози в делтоидния мускул или глутеус максимус. Преминаването от седалище към делтоид (и обратно) трябва да се обмисли за болка на мястото на инжектиране, ако такъв дискомфорт не се понася добре (вж. Точка 4.8). Препоръчва се и редуване между лява и дясна страна (вижте по -долу).
За инструкции за употреба и боравене с XEPLION вижте раздела с листовката (информация, предназначена за медицински или здравни специалисти).
Въвеждане в делтоидния мускул
Препоръчителният размер на иглата за първоначално и поддържащо приложение на XEPLION в делтоидния мускул се определя от теглото на пациента.За тегло ≥ 90 kg, 1½-инчов, 22 G (38.1 mm x 0. 72 mm) делтоидни мускули.
Прилагане в седалищния мускул
Препоръчителният размер на иглата за поддържащо приложение на XEPLION в седалищния мускул е 1½ инча, 22 G (38,1 mm x 0,72 mm). Администрирането трябва да се извърши във външния горен квадрант на областта на седалището. Инжекциите в седалището трябва да се редуват между двата седалищни мускула.
04.3 Противопоказания
Свръхчувствителност към активното вещество, към рисперидон или към някое от помощните вещества, изброени в точка 6.1.
04.4 Специални предупреждения и подходящи предпазни мерки при употреба
Употреба при пациенти в остра възбуда или в тежко психотично състояние
XEPLION не трябва да се използва за лечение на остро възбуждане или тежки психотични състояния, когато се изисква незабавен контрол на симптомите.
QT интервал
Трябва да се внимава при предписване на палиперидон при пациенти с известни сърдечно -съдови заболявания или с фамилна анамнеза за удължаване на QT интервала и при едновременна употреба на други лекарства, за които се смята, че удължават QT интервала.
Невролептичен злокачествен синдром
Невролептичен злокачествен синдром (НМС), характеризиращ се с хипертермия, скованост на мускулите, нестабилност на автономната нервна система, промени в съзнанието и повишена серумна креатинфосфокиназа, е докладван при палиперидон Допълнителни клинични прояви могат да включват миоглобинурия (рабдомиолиза) и остра бъбречна недостатъчност. Ако пациентът показва признаци или симптоми, предполагащи НМС, лечението с който и да е антипсихотик, включително палиперидон, трябва да се преустанови.
Тардивна дискинезия
Лекарства с антагонистично действие върху допаминергичните рецептори са свързани с индуцирането на тардивна дискинезия, характеризираща се с ритмични и неволеви движения, особено на езика и / или лицето.
Левкопения, неутропения и агранулоцитоза
Съобщавани са случаи на левкопения, неутропения и агранулоцитоза при употребата на антипсихотици, включително XEPLION.Агранулоцитоза се съобщава много рядко (белите кръвни клетки (WBC) или индуцираната от лекарството левкопения / неутропения трябва да се проследяват по време на постмаркетинговото наблюдение) по време на. първите месеци от терапията и преустановяването на XEPLION трябва да се обмислят при първите признаци на клинично значимо намаляване на WBC при липса на други причинители.Пациентите с клинично значима неутропения трябва да бъдат внимателно проследявани за треска или други симптоми или признаци на инфекция и да се лекуват незабавно, ако се появят такива симптоми или признаци Пациенти с тежка неутропения (абсолютен брой неутрофили
Хипергликемия и захарен диабет
По време на лечението с палиперидон са съобщени хипергликемия, захарен диабет и обостряне на съществуващ диабет. В някои случаи е докладвано предишно наддаване на тегло, което може да бъде предразполагащ фактор. Много рядко и рядко се съобщава за връзка с кетоацидоза с диабетна кома. Препоръчва се подходящо клинично проследяване в съответствие с насоките, използвани за антипсихотици. Пациентите, лекувани с който и да е атипичен антипсихотик, включително XEPLION, трябва да бъдат наблюдавани за симптоми на хипергликемия. полидипсия, полиурия, полифагия и слабост) и пациентите със захарен диабет трябва да се наблюдават редовно за влошаване на гликемичния контрол.
Качване на тегло
Съобщава се за значително наддаване на тегло по време на употреба на XEPLION. Теглото трябва да се оценява редовно.
Хиперпролактинемия
Изследванията на клетъчната култура показват, че клетъчният растеж при човешки тумори на гърдата може да бъде стимулиран от пролактин. Въпреки че досега не е доказана ясна връзка с прилагането на антипсихотици в клинични и епидемиологични проучвания, се препоръчва повишено внимание при пациенти със съответна анамнеза. Палиперидон трябва да се използва с повишено внимание при пациенти с възможни пролактин-зависими тумори.
Ортостатична хипотония
Палиперидон може да предизвика ортостатична хипотония при някои пациенти поради алфа-блокиращото си действие.
Въз основа на обединени данни от три плацебо-контролирани, 6-седмични изпитвания с фиксирани дози с перорални таблетки с удължено освобождаване палиперидон (3, 6, 9 и 12 mg), ортостатична хипотония е докладвана от 2,5% от пациентите, лекувани с перорален палиперидон спрямо 0,8% от субектите, лекувани с плацебо. XEPLION трябва да се използва с повишено внимание при пациенти с известни сърдечно -съдови заболявания (напр. сърдечна недостатъчност, миокарден инфаркт или исхемия, дефекти на проводимостта), цереброваскуларно заболяване или състояния, предразполагащи пациента към хипотония (като напр. дехидратация и хиповолемия).
Конвулсии
XEPLION трябва да се използва с повишено внимание при пациенти с анамнеза за гърчове или други състояния, които могат да понижат гърчовия праг.
Бъбречна недостатъчност
Плазмените концентрации на палиперидон се увеличават при пациенти с бъбречна недостатъчност и поради това се препоръчва коригиране на дозата при пациенти с лека бъбречна недостатъчност. XEPLION не се препоръчва при пациенти с умерено или тежко бъбречно увреждане (креатининов клирънс
Чернодробна недостатъчност
Няма налични данни при пациенти с тежко чернодробно увреждане (клас С по Child-Pugh). Препоръчва се повишено внимание при използване на палиперидон при такива пациенти.
Пациенти в старческа възраст с деменция
Не са провеждани проучвания с XEPLION при пациенти в старческа възраст с деменция. XEPLION трябва да се използва с повишено внимание при възрастни пациенти с деменция с рискови фактори за инсулт. Опитът с рисперидон, споменат по -долу, също се счита за валиден за палиперидон.
Глобална смъртност
В мета-анализ на 17 контролирани клинични проучвания, пациенти в старческа възраст с деменция, лекувани с други атипични антипсихотици, включително рисперидон, арипипразол, оланзапин и кветиапин, са имали по-висок риск от смъртност от плацебо. Сред лекуваните с рисперидон, смъртността е 4% в сравнение с 3,1% за плацебо.
Цереброваскуларни нежелани реакции
При рандомизирани плацебо-контролирани клинични проучвания при пациенти с деменция, лекувани с някои атипични антипсихотици, включително рисперидон, арипипразол и оланзапин, се наблюдава приблизително три пъти повишен риск от мозъчно-съдови нежелани реакции. Механизмът зад повишения риск е неизвестен.
Болест на Паркинсон и деменция с телата на Леви
Лекарите трябва да преценят рисковете и ползите от предписването на XEPLION на пациенти с болест на Паркинсон или деменция с тела на Lewy (DLB), тъй като и двете групи пациенти могат да бъдат изложени на по -голям риск от развитие на невролептичен злокачествен синдром, както и да покажат повишена чувствителност към антипсихотици. Проявите на тази повишена чувствителност могат да включват объркване, тъпота, постурална нестабилност с чести падания, както и екстрапирамидни симптоми.
Приапизъм
Съобщава се, че антипсихотични лекарствени продукти (включително рисперидон) с алфа-адренергични блокиращи ефекти предизвикват приапизъм. По време на постмаркетинговото наблюдение се съобщава и за приапизъм при перорален палиперидон, който е активният метаболит на рисперидон. Пациентите трябва да бъдат предупредени, че ако приапизмът не отшуми в рамките на 3-4 часа, те трябва да потърсят спешна медицинска помощ.
Регулиране на телесната температура
Нарушената способност на организма да понижава основната телесна температура се дължи на антипсихотични лекарства. Препоръчва се особено внимание при предписване на XEPLION на пациенти, които могат да бъдат изложени на състояния, които могат да допринесат за повишаване на основната телесна температура, като например тежки физически упражнения, излагане на силна топлина, съпътстващо лечение с антихолинергични лекарства или са склонни към дехидратация.
Венозна тромбоемболия
Съобщавани са случаи на венозна тромбоемболия (ВТЕ) с антипсихотични лекарства.
Пациентите, лекувани с антипсихотици, често са придобили рискови фактори за ВТЕ, поради което всички възможни рискови фактори за ВТЕ трябва да бъдат идентифицирани преди и по време на лечението с XEPLION и да се предприемат превантивни мерки.
Антиеметичен ефект
В предклинични проучвания с палиперидон се наблюдава антиеметичен ефект. Този ефект, ако се прояви при хора, би могъл да прикрие признаците и симптомите на предозиране на някои лекарства или на състояния като чревна обструкция, синдром на Reye и мозъчен тумор.
Администрация
Трябва да се внимава да се избегне неволно инжектиране на XEPLION в кръвоносен съд.
Интраоперативен синдром на флопи ирис
Интраоперативен синдром на флопи ирис (IFIS) е наблюдаван по време на операция на катаракта при пациенти, лекувани с лекарствени продукти с алфа1а-адренергичен антагонистичен ефект, като XEPLION (вж. Точка 4.8).
IFIS може да увеличи риска от очни усложнения по време и след операцията. Текущата или миналата употреба на лекарствени продукти с алфа1а-адренергичен антагонистичен ефект трябва да се съобщи на очния хирург преди операцията. Потенциалната полза от преустановяване на терапията с алфа1 блокер преди операция на катаракта не е установена и трябва да се прецени спрямо риска от преустановяване на антипсихотичната терапия.
04.5 Взаимодействия с други лекарствени продукти и други форми на взаимодействие
Препоръчва се повишено внимание при предписване на XEPLION в комбинация с лекарствени продукти, за които е известно, че удължават QT интервала, като антиаритмици от клас IA (напр. Хинидин, дизопирамид) и антиаритмици от клас III (напр. Например амиодарон, соталол), някои антихистамини, някои други антипсихотици и някои антималарийни средства (напр. мефлохин). Списъкът е ориентировъчен и не е изчерпателен.
Възможност XEPLION да повлияе на други лекарства
Не се очаква палиперидон да предизвика клинично значими фармакокинетични взаимодействия с лекарствени продукти, които се метаболизират от изоензимите на цитохром Р-450.
Като се имат предвид ефектите на палиперидон върху първичната централна нервна система (ЦНС) (вж. Точка 4.8), XEPLION трябва да се използва с повишено внимание в комбинация с други лекарствени продукти с централно действие, напр. анксиолитици, повечето антипсихотици, сънотворни, опиати и др. или с алкохол.
Палиперидон може да антагонизира ефекта на леводопа и други допаминови агонисти.
Поради потенциала си да индуцира ортостатична хипотония (вж. Точка 4.4), може да се наблюдава адитивен ефект, когато XEPLION се прилага с други терапевтични средства, които имат този потенциал, например с други антипсихотици или трициклици.
Препоръчва се повишено внимание, ако палиперидон се прилага в комбинация с други лекарствени продукти, за които се смята, че понижават прага на припадъци (например, фенотиазини или бутирофенони, трициклични или SSRIs, трамадол, мефлохин и др.).
Едновременното приложение на палиперидон перорални таблетки с удължено освобождаване в стационарно състояние (12 mg веднъж дневно) с таблетки с удължено освобождаване валпроева киселина + валпроат натрий (500 до 2000 mg веднъж дневно) не повлиява фармакокинетиката на валпроат в равновесно състояние.
Не са провеждани проучвания за взаимодействие между XEPLION и литий, но фармакокинетичното взаимодействие е малко вероятно.
Потенциал за други лекарства да повлияят на XEPLION
Образование инвитро показват, че CYP2D6 и CYP3A4 могат да бъдат минимално включени в метаболизма на палиперидон, но няма индикации или инвитро нито едно in vivo че тези изоензими играят значителна роля в метаболизма на палиперидон. Едновременното приложение на перорален палиперидон с пароксетин, мощен инхибитор на CYP2D6, не показва клинично значими ефекти върху фармакокинетиката на палиперидон.
Едновременното приложение на перорален палиперидон с удължено освобождаване веднъж дневно с карбамазепин 200 mg два пъти дневно причинява приблизително 37% намаление на средните Cmax и AUC при стабилно състояние на палиперидон. Това намаление се дължи в значителна степен на 35% увеличение на бъбречния клирънс на палиперидон, вероятно в резултат на индуцирана от карбамазепин бъбречна P-gp. Незначително намаляване на количеството на активното вещество, екскретирано непроменено в урината, предполага минимален ефект върху метаболизма на CYP или бионаличността на палиперидон по време на едновременно приложение с карбамазепин.При по-високи дози карбамазепин може да настъпи по-голямо намаляване на плазмените концентрации на палиперидон.При започване на лечение с карбамазепин, дозата на XEPLION трябва да се преоцени и при необходимост да се увеличи. Обратно, в случай на преустановяване на лечението с карбамазепин, дозата на XEPLION трябва да се преоцени и да се намали, ако е необходимо.
Едновременното приложение на еднократна доза от 12 mg перорална таблетка палиперидон с удължено освобождаване с таблетки с удължено освобождаване на валпроева киселина + натриев валпроат (две таблетки от 500 mg веднъж дневно) води до увеличаване на приблизително 50% Cmax и AUC на палиперидон, вероятно като в резултат на повишена перорална абсорбция. Тъй като не е наблюдаван ефект върху системния клирънс, не се очаква клинично значимо взаимодействие между таблетки с удължено освобождаване на валпроева киселина + натриев валпроат и интрамускулна инжекция XEPLION. Това взаимодействие не е проучвано с XEPLION.
Едновременна употреба на XEPLION с рисперидон
Орално или интрамускулно рисперидон ще се метаболизира до различна степен до палиперидон. Бъдете внимателни, ако пероралният рисперидон или палиперидон се прилагат едновременно с XEPLION.
04.6 Бременност и кърмене
Бременност
Няма адекватни данни за употребата на палиперидон по време на бременност.Палиперидон палмитат, инжектиран интрамускулно и палиперидон, приложен през устата, не е показал тератогенен ефект при проучвания при животни, но са наблюдавани други видове репродуктивна токсичност (вж. Точка 5.3). антипсихотиците (включително палиперидон) през третия триместър на бременността са изложени на риск от нежелани реакции, включително екстрапирамидни и / или симптоми на отнемане, които могат да варират по тежест и продължителност след раждането. безпокойство, хипертония, хипотония, тремор, сънливост, затруднено дишане или хранителни разстройства . Следователно бебетата трябва да бъдат наблюдавани внимателно. XEPLION не трябва да се приема по време на бременност, освен ако не е абсолютно необходимо.
Време за хранене
Палиперидон се екскретира в кърмата до такава степен, че ефектите върху кърмачето са възможни, когато терапевтичните дози се прилагат на кърмещи жени. XEPLION не трябва да се използва по време на периода на кърмене.
Плодовитост
Неклинични ефекти не са наблюдавани при неклинични проучвания.
04.7 Ефекти върху способността за шофиране и работа с машини
Палиперидон може леко или умерено да повлияе способността за шофиране или работа с машини поради потенциални нервна система и визуални ефекти като седация, сънливост, синкоп и замъглено зрение (вж. Точка 4.8). Поради това пациентите трябва да бъдат посъветвани да не шофират и не работят с машини, докато не е известна индивидуалната чувствителност към XEPLION.
04.8 Нежелани реакции
Обобщение на профила на безопасност
Най -често съобщаваните нежелани лекарствени реакции (НЛР) в клиничните изпитвания са безсъние, главоболие, тревожност, инфекция на горните дихателни пътища, реакция на мястото на инжектиране, паркинсонизъм, наддаване на тегло, акатизия, възбуда, седация / сънливост., Гадене, запек, замаяност, мускулно -скелетна система болка, тахикардия, тремор, коремна болка, повръщане, диария, умора и дистония. От тях акатизията и седацията / сънливостта изглежда са свързани с дозата.
Таблица на нежеланите реакции
Всички следните нежелани лекарствени реакции са докладвани с палиперидон по честотна категория, изчислена от клиничните изпитвания на XEPLION. Прилагат се следните условия и честоти: много често (≥ 1/10), често срещани (≥ 1/100 до нечести (≥ 1/1000 до редки (≥ 1/10 000 до много редки (с неизвестна честота (не може да бъде оценена от наличните данни от клинични изпитвания))
a Вижте "хиперпролактинемия" по -долу.
b Вижте "екстрапирамидни симптоми" по -долу.
c В плацебо-контролирани клинични изпитвания, захарен диабет е докладван при 0,32% от пациентите, лекувани с XEPLION, в сравнение с 0,39% в групата на плацебо. Общата честота на всички клинични проучвания е 0,47% при всички пациенти, лекувани с XEPLION.
d Безсънието включва: първоначално безсъние, централно безсъние; припадъците включват: припадъци grand mal; отокът включва: генерализиран оток, периферен оток, пластичен оток; менструалното разстройство включва: нередовна менструация, олигоменорея
e Не се наблюдава в клиничните изпитвания на XEPLION, но се наблюдава в постмаркетинговия опит с палиперидон.
Нежелани реакции, съобщени при формулировки на рисперидон
Палиперидон е активният метаболит на рисперидон, следователно профилите на нежеланите реакции на тези съединения (включително орални и инжекционни форми) са релевантни един за друг. В допълнение към нежеланите реакции, споменати по -горе, следните нежелани реакции са съобщени при употребата на рисперидонови продукти и могат да се очакват с XEPLION.
Нарушения на нервната система: мозъчно -съдови нарушения
Очни нарушения: sсиндром на флаг ирис (интраоперативен)
Дихателни, гръдни и медиастинални нарушения: хрипове
Общи нарушения и състояния на мястото на приложение (наблюдавани при инжекционния състав на рисперидон): некроза на мястото на инжектиране, язва на мястото на инжектиране.
Описание на избрани нежелани реакции
Анафилактична реакция
Случаи на анафилактична реакция след инжектиране с XEPLION са докладвани рядко в постмаркетинговия опит при пациенти, които преди това са понасяли перорален рисперидон или перорален палиперидон.
Реакции на мястото на инжектиране
Най -често съобщаваната нежелана реакция на мястото на инжектиране е болка. По -голямата част от тези съобщени реакции са леки до умерени по тежест. Оценките на пациентите за болка в мястото на инжектиране, базирани на визуална аналогова скала, имаха тенденция да намаляват с течение на времето по честота и интензивност във всички проучвания от Фаза 2 и Фаза 3. Инжекциите с делтоид се възприемат като леко болезнени, по -големи от съответните инжекции в задните части. Други реакции на мястото на инжектиране са предимно леки по интензитет и включват индурация (често), сърбеж (нечести) и възли (редки).
Екстрапирамидни симптоми (EPS)
EPS включва обединен анализ на следните термини: паркинсонизъм (включва слюнчена хиперсекреция, мускулно -скелетна скованост, паркинсонизъм, загуба на слюнка, скованост на зъбчатото колело, брадикинезия, хипокинезия, фация на маска, мускулно напрежение, акинезия, скованост на мускулите, скованост на мускулите, паркинсоланова походка и абнормна глабилна походка рефлекс, паркинсонов тремор в покой), акатизия (включва акатизия, безпокойство, хиперкинезия, синдром на неспокойните крака), дискинезия (включително дискинезия, потрепване на мускулите, хореоатетоза, атетоза и миоклония), дистония (включва дистония, хипертония, тортиколис, инктолус мускулна контрактура, блефароспазъм, окулорация, лингвална парализа, лицев спазъм, ларингоспазъм, миотония, опистотонус, орофарингеален спазъм, плеврототонус, езичен спазъм и тризмус) и тремор. Трябва да се отбележи, че е включен по-широк спектър от симптоми, които не са непременно с екстрапирамиден произход
Качване на тегло
В 13-седмичното проучване, включващо първоначално приложение на 150 mg, делът на субектите с необичайно наддаване на тегло ≥ 7% показва свързана с дозата тенденция, с честота на заболеваемост от 5% в групата на плацебо в сравнение с процентите от 6%, 8% и 13% в групите XEPLION 25 mg, 100 mg и 150 mg съответно.
По време на 33-седмичния отворен период на преход / поддържане на дългосрочното изпитване за предотвратяване на рецидив, 12% от пациентите, лекувани с XEPLION, са имали този ефект (≥ 7% наддаване на тегло от двойно-сляпа фаза до крайна точка); средно (SD) промяната на теглото спрямо изходното ниво във фазата на отворения етикет е + 0,7 кг.
Хиперпролактинемия
В клинични проучвания са наблюдавани средни повишения на серумния пролактин и при двата пола, получаващи XEPLION. Като цяло са докладвани нежелани реакции, които биха могли да предполагат повишаване на нивата на пролактин (напр. Аменорея, галакторея, менструални нарушения, гинекомастия)
Категории ефекти
Удължаване на QT интервала, камерни аритмии (вентрикуларна фибрилация, камерна тахикардия), внезапна необяснима смърт, сърдечен арест и torsades de pointes могат да настъпят при прилагането на антипсихотици. Случаи на венозна тромбоемболия и случаи на дълбока венозна тромбоза (честота не се знае).
Докладване на предполагаеми нежелани реакции
Съобщаването на предполагаеми нежелани реакции, настъпили след разрешаване на лекарствения продукт, е важно, тъй като позволява непрекъснато проследяване на съотношението полза / риск на лекарствения продукт. От медицинските специалисти се изисква да съобщават всякакви предполагаеми нежелани реакции чрез националната система за докладване. В „Приложение V .
04.9 Предозиране
Като цяло очакваните признаци и симптоми са тези, дължащи се на усилване на известните фармакологични ефекти на палиперидон, напр. Сънливост и седация, тахикардия и хипотония, удължаване на QT и екстрапирамидни симптоми. Torsade de pointes и вентрикуларна фибрилация са докладвани при пациент в състояние на предозиране с перорален палиперидон. В случай на остро предозиране трябва да се обмисли възможността за включване на множество лекарства.
При оценката на нуждите от лечение и възстановяването трябва да се има предвид естеството на лекарството с удължено освобождаване и дългият елиминационен полуживот на палиперидон. Няма специфичен антидот за палиперидон. Трябва да се въведат подходящи общи поддържащи мерки.
Сърдечно -съдовият мониторинг трябва да започне незабавно и трябва да включва непрекъснато електрокардиографско наблюдение за възможни аритмии. Хипотонията и циркулаторният колапс трябва да се лекуват с подходящи мерки, като например интравенозни течности и / или симпатикомиметици.
05.0 ФАРМАКОЛОГИЧНИ СВОЙСТВА
05.1 Фармакодинамични свойства
Фармакотерапевтична група: психолептици, други антипсихотици.
ATC код: N05AX13.
XEPLION съдържа рацемична смес от (+) - и ( -) - палиперидон.
Механизъм на действие
Палиперидон е селективен блокиращ агент с моноаминови ефекти, чиито фармакологични свойства са различни от тези на традиционните невролептици. Палиперидон се свързва силно със серотонинергичните и допаминергичните D2 5-НТ2 рецептори. Палиперидон също блокира алфа1-адренергичните рецептори и в по-малка степен хистаминергичните Н1- и алфа2-адренергичните рецептори. Фармакологичната активност на (+) и (-) енантиомерите на палиперидон е качествено и количествено сходна.
Палиперидон не се свързва с холинергични рецептори. Въпреки че палиперидон е силен антагонист на D2, за който се смята, че облекчава положителните симптоми на шизофрения, той причинява по -малко каталепсия и намалява двигателния капацитет в по -малка степен от традиционните невролептици. Централният доминиращ антагонизъм на серотонина може да намали тенденцията палиперидон да причинява екстрапирамидни странични ефекти.
Клинична ефикасност
Остро лечение на шизофрения
Ефикасността на XEPLION при остро лечение на шизофрения е установена в четири краткосрочни (едно 9-седмично и три 13-седмични) двойно-слепи, рандомизирани, плацебо-контролирани, фиксирани дози при хоспитализирани възрастни пациенти с остър екзацербация Критерии за DSM-IV за шизофрения. Фиксираните дози XEPLION в тези проучвания са прилагани на 1, 8 и 36 ден в 9-седмичното проучване, а също и на 64-ия ден в 13-седмичните проучвания. Не се изискват допълнителни допълнения. антипсихотици по време на остро лечение на шизофрения с XEPLION. Първичната крайна точка за ефикасност се дефинира като намаляване на общите резултати по скалата на позитивния и негативния синдром (PANSS), както е показано в таблицата по-долу. Скалата PANSS е един валидиран инструмент с много точки, състоящ се от пет измерения за оценка на положителни симптоми, отрицателни симптоми, концептуална дезорганизация, враждебност / възбуда n върху контролирани и тревожност / депресия. Функционирането беше оценено с помощта на скалата за лични и социални резултати (PSP). PSP е клинично утвърдена скала, която измерва личното и социалното функциониране в четири области: обществено полезни дейности (работа и учене), лични и социални взаимоотношения, грижа за себе си и смущаващо и агресивно поведение.
В 13-седмично проучване (n = 636), сравняващо три фиксирани дози XEPLION (първоначална инжекция с делтоид от 150 mg, последвана от 3 дози от седалището или делтоида от 25 mg / 4 седмици, 100 mg / 4 седмици или 150 mg / 4 седмици) с плацебо и трите дози XEPLION превъзхождат плацебо при подобряване на общия резултат на PANSS. В това проучване както групите от 100 mg / 4 седмици, така и 150 mg / 4 седмици, но не и 25 mg / 4 седмици, демонстрират статистическо превъзходство пред PSP резултата спрямо плацебо. Тези резултати подкрепят ефикасността и подобрението на PANSS с пълна продължителност и са наблюдавани в началото на 4-ия ден със значително отделяне от плацебо в групите XEPLION 25 mg и 150 mg от 8-ми ден.
Резултатите от другите проучвания предоставят статистически значими резултати в полза на XEPLION, с изключение на дозата от 50 mg в едно проучване (виж таблицата по -долу).
* За проучване R092670-PSY-3007, начална доза от 150 mg е приложена на първия ден на всички субекти в групите за лечение с XEPLION, последвана от определената доза след това.
Забележка: Отрицателната промяна в резултатите показва подобрение.
Поддържане на контрола на симптомите и забавяне на рецидив на шизофрения
Ефикасността на XEPLION за поддържане на контрола на симптомите и забавяне на рецидив на шизофрения е установена в по-дългосрочно, двойно-сляпо, плацебо-контролирано проучване с гъвкави дози, включващо 849 възрастни лица, които не са в напреднала възраст и отговарят на критериите DSM-IV за шизофрения. Това проучване включва открита фаза на остро лечение и стабилизиране от 33 седмици, плацебо-контролирана двойно-сляпа фаза на рандомизация за наблюдение на евентуален рецидив и открит удължен период от 52 седмици. В това проучване дозите на XEPLION включват 25, 50, 75 и 100 mg, прилагани месечно; дозата от 75 mg е била разрешена само в 52-седмичния отворен период на удължаване. Субектите първоначално са получавали гъвкави дози (25-100 mg) XEPLION по време на 9-седмичен преходен период, последван от 24-седмичен период на поддържане, при който субектите трябваше да имат PANSS резултат ≤ 75. Корекциите на дозата бяха разрешени само през първия 12 седмици от периода на поддръжка. Общо 410 стабилизирани пациенти бяха рандомизирани на XEPLION (средна продължителност 171 дни [диапазон от 1 ден до 407 дни]) или на плацебо (средна продължителност 105 дни [диапазон от 8 дни до 441 дни]), докато не се появят отново симптоми на шизофрения. двойно-сляпа фаза с променлива продължителност. Проучването е прекратено рано поради причини за ефикасност, тъй като се наблюдава значително по -дълго време до рецидив (стр
Педиатрична популация
Европейската агенция по лекарствата се отказа от задължението да представи резултатите от проучванията с XEPLION във всички подгрупи на педиатричната популация при шизофрения. Вижте точка 4.2 за информация относно педиатричната употреба.
05.2 "Фармакокинетични свойства
Абсорбция и разпределение
Палиперидон палмитат е пролекарството на естер на палмитат на палиперидон. Поради изключително ниската си разтворимост във вода, палиперидон палмитат се разтваря бавно след мускулно инжектиране, преди да се хидролизира до палиперидон и да се абсорбира в системната циркулация. След еднократна интрамускулна доза плазмените концентрации на палиперидон постепенно се повишават до достигане на пикови плазмени концентрации при медиана на Т от 13 дни. Освобождаването на активното вещество започва още на ден 1 и продължава поне 4 месеца.
След интрамускулно инжектиране на единични дози (25-150 mg) в делтоидния мускул се наблюдава средно 28% по-висок Cmax в сравнение с инжектирането в седалището.Двете първоначални интрамускулни инжекции с делтоид от 150 mg на ден 1 и 100 mg на ден 8 спомагат за бързо постигане на терапевтични концентрации. Профилът на освобождаване и режимът на дозиране на XEPLION водят до устойчиви терапевтични концентрации. Общата експозиция на палиперидон след прилагане на XEPLION е пропорционална на дозата в диапазон от 25-150 mg и по-малка от пропорционалната на дозата за C за дози над 50 mg. mg е 1,8 след приложение в задните части и 2,2 след приложение в делтоида.25-150 mg диапазон на дозата варира от 25 до 49 дни.
Абсолютната бионаличност на палиперидон палмитат след прилагане на XEPLION е 100%.
След прилагане на палиперидон палмитат (+) и (-) енантиомерите на палиперидон се превръщат, достигайки съотношение AUC (+) / (-) приблизително 1,6-1,8.
Свързването с плазмените протеини на рацемичния палиперидон е 74%.
Биотрансформация и елиминиране
След една седмица след прилагане на единична перорална доза от 1 mg 14C-палиперидон с незабавно освобождаване, 59% от дозата се екскретира непроменена в урината, което показва, че палиперидон не се метаболизира екстензивно в черния дроб. Приблизително 80% от приложената радиоактивност се открива в урината и 11% във фекалиите. In vivo Идентифицирани са четири метаболитни пътя, нито един от които не представлява повече от 6,5% от дозата: деалкилиране, хидроксилиране, дехидрогениране и разцепване на бензизоксазол. Въпреки че проучванията инвитро предполагат роля на CYP2D6 и CYP3A4 в метаболизма на палиперидон, няма доказателства in vivo че тези изоензими играят значителна роля в метаболизма на палиперидон. Популационните фармакокинетични анализи показват, че няма видима разлика във видимия клирънс на палиперидон след приложение на перорален палиперидон между обширни метаболизатори и лоши метаболизатори на субстрати на CYP2D6. Проучвания инвитро върху човешки чернодробни микрозоми показа, че палиперидон не инхибира съществено метаболизма на лекарствени продукти, метаболизирани от изоензимите на цитохром Р450, включително CYP1A2, CYP2A6, CYP2C8 / 9/10, CYP2D6, CYP2E1, CYP3A4 и CYP3A5.
Проучвания инвитро демонстрира, че палиперидон е P-gp субстрат и слаб инхибитор на P-gp при високи концентрации. Няма налични данни in vivo и клиничното значение е неизвестно.
Инжектиране на палиперидон палмитат с удължено освобождаване срещу палиперидон с орално освобождаване продължително
XEPLION е разработен за освобождаване на палиперидон за период от един месец, докато пероралният палиперидон с удължено освобождаване се прилага ежедневно. Режимът на началната фаза за XEPLION (150 mg / 100 mg в делтоидния мускул на ден 1 / ден 8) е разработен за бързо постигане на концентрации на палиперидон при стабилно състояние в началото на терапията без използване на никакви перорални добавки.
Като цяло, общите плазмени нива на началната фаза с XEPLION са били в границите на експозиция, наблюдавани при 6-12 mg перорален палиперидон с удължено освобождаване. Използването на схемата за начална фаза на XEPLION позволи на пациентите да останат в рамките на този 6-12 mg перорален период на експозиция на палиперидон дори в дните с ниска концентрация преди дозиране (Ден 8 и Ден 36). Поради разликата в средните фармакокинетични профили между двете лекарства, трябва да се внимава, когато се прави директно сравнение на техните фармакокинетични свойства.
Чернодробна недостатъчност
Палиперидон не се метаболизира екстензивно в черния дроб. Въпреки че XEPLION не е проучен при пациенти с чернодробно увреждане, не се налага коригиране на дозата при пациенти с леко до умерено чернодробно увреждане. В проучване с перорален палиперидон при лица с умерено чернодробно увреждане (клас В по Child-Plugh) плазмените концентрации на свободния палиперидон са подобни на тези при здрави индивиди. Не са провеждани проучвания с палиперидон при пациенти с тежко чернодробно увреждане.
Бъбречна недостатъчност
Разпределението на единична перорална доза палиперидон 3 mg таблетки с удължено освобождаване е проучено при лица с различна степен на бъбречна функция. Елиминирането на палиперидон намалява с намаляването на изчисления креатининов клирънс. Общият клирънс на палиперидон е намален средно с 32% при лица с леко увредена бъбречна функция (CrCl = 50 до
Възрастни граждани
Не се препоръчва коригиране на дозата въз основа само на възрастта. Възможно е обаче да се наложи коригиране на дозата поради свързано с възрастта намаляване на креатининовия клирънс (вж. Бъбречно увреждане по-горе и точка 4.2).
Тегло
Фармакокинетичните проучвания с палиперидон палмитат показват понякога по-ниски (10-20%) плазмени концентрации на палиперидон при пациенти с наднормено тегло или затлъстяване, отколкото при пациенти с нормално тегло (вж. Точка 4.2).
Състезание
Популационните фармакокинетични анализи на данни от проучвания с перорален палиперидон не показват разлики, свързани с расата, във фармакокинетиката на палиперидон след прилагане на XEPLION.
Секс
Не са наблюдавани клинично значими разлики между мъже и жени.
Дим
Въз основа на проучвания инвитро проведено с използване на човешки чернодробни ензими, палиперидон не е субстрат за CYP1A2; следователно не се очаква пушенето да повлияе на фармакокинетиката на палиперидон. Популационен фармакокинетичен анализ на данни с таблетки с удължено освобождаване на палиперидон показа малко по-ниска експозиция на палиперидон при пушачите, отколкото при непушачите. Малко вероятно е разликата да е клинично значима. Пушенето не е оценено за XEPLION.
05.3 Предклинични данни за безопасност
Проучванията за токсичност при многократно приложение на интрамускулно инжектиран палиперидон палмитат и перорално прилаган палиперидон при плъхове и кучета показват главно фармакологични ефекти, като седативни и пролактин-медиирани ефекти върху млечните и гениталните жлези. Възпалителна реакция на мястото на интрамускулно инжектиране е отбелязана при животни, лекувани с палиперидон палмитат. Понякога се е образувал абсцес.
В проучвания за репродукция на плъхове с перорален рисперидон, който в голяма степен се превръща в палиперидон при плъхове и хора, са отбелязани неблагоприятни ефекти върху теглото при раждане и преживяемостта на потомството. Не са наблюдавани ембриотоксичност или малформации след интрамускулно приложение на палиперидон палмитат при бременни плъхове до най -високата доза (160 mg / kg / ден), съответстваща на 4,1 пъти нивото на експозиция при хора при максималната препоръчителна доза от 150 mg. Други допаминови антагонисти, когато прилаган на бременни животни, предизвиква неблагоприятни ефекти върху ученето и двигателното развитие на потомството.
Палиперидон палмитат и палиперидон не са генотоксични. При орални проучвания за канцерогенност на рисперидон при плъхове и мишки са установени увеличения на аденомите на хипофизната жлеза (при мишки), ендокринните аденоми на панкреаса (при плъхове) и аденомите на млечната жлеза (и при двата вида). Канцерогенният потенциал на интрамускулно инжектиран палиперидон палмитат се оценява при плъхове. Наблюдава се статистически значимо увеличение на аденокарциномите на млечните жлези при женски плъхове при 10, 30 и 60 mg / kg / месец. Статистически значимо увеличение на аденомите и карциномите на млечните жлези е демонстрирано при мъже при 30 и 60 mg / kg / месец, което представлява 1,2 и 2,2 пъти нивото на експозиция при максималната препоръчителна доза за хора от 150 mg. Тези тумори могат да бъдат свързани с удължен допамин Антагонизъм на D2 рецептора и хиперпролактинемия. Значението на тези туморни находки при гризачи по отношение на човешкия риск е неизвестно.
06.0 ФАРМАЦЕВТИЧНА ИНФОРМАЦИЯ
06.1 Помощни вещества
Полисорбат 20
Полиетилен гликол 4000
Лимонена киселина монохидрат
Безводен ди-натриев хидроген фосфат
Натриев дихидроген фосфат монохидрат
Натриев хидроксид (за регулиране на рН)
Вода за инжекции
06.2 Несъвместимост
Този лекарствен продукт не трябва да се смесва с други лекарствени продукти.
06.3 Срок на валидност
2 години.
06.4 Специални условия на съхранение
Съхранявайте при температура не по -висока от 30 ° C.
06.5 Естество на непосредствената опаковка и съдържанието на опаковката
Предварително напълнена спринцовка (съполимер с цикличен олефин) с ограничител на буталото, крила на дръжката на спринцовката и заключваща капачка (бромобутилова гума) с предпазна игла 22G, 1 ½ инча (0.72 мм x 38.1 мм) и предпазна игла 23G, 1 инч (0.64 мм х 25,4 мм).
Опаковка:
Опаковката съдържа 1 предварително напълнена спринцовка и 2 игли
06.6 Инструкции за употреба и боравене
Неизползваното лекарство и отпадъците, получени от това лекарство, трябва да се изхвърлят в съответствие с местните разпоредби
07.0 Притежател на разрешението за търговия
Janssen-Cilag International NV, Turnhoutseweg 30,
B-2340 Beerse, Белгия.
08.0 НОМЕР НА РАЗРЕШЕНИЕТО ЗА ПОТРЕБЕНИЕ
EU/1/11/672/004
041004045
09.0 ДАТА НА ПЪРВО РАЗРЕШЕНИЕ ИЛИ ПОДНОВЯВАНЕ НА РАЗРЕШЕНИЕТО
04 март 2011 г.
10.0 ДАТА НА ПРЕГЛЕД НА ТЕКСТА
D.CCE март 2015 г.

















-e-ruscogenina.jpg)