Общност
Цианидът е химическият термин, който идентифицира всяко химично съединение, съдържащо циано групата (CN).
Циановата група е молекула, образувана от обединението на въглероден атом и азотен атом.

Примери за неорганичен цианид са циановодород, натриев цианид, калиев цианид и цианоген хлорид.
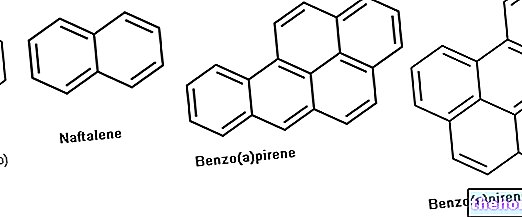
Примери за органичен цианид, от друга страна, са нитрилите, съдържащи се в зърната на различни плодове (кайсии, праскови, череши и др.).
Цианидите са химикали, които се използват широко в производството, от хартиената промишленост до металургията, пластмасите и др.
Какво е цианид?
Цианид е всяко химично съединение, съдържащо циано групата (CN).
Циано групата е резултат от обединението на въглероден атом (C на CN) с азотен атом (N на CN). Връзката, която обединява въглерода с азота, е тройна ковалентна връзка. Общият заряд в групата CN е отрицателен, следователно циано групата е анион.
ЦИАНИД КАТО ОТРОВА: НЕОРГАНИЧЕН ЦИАНИД
В обичайното въображение терминът цианид се отнася до мощна отрова със смъртоносни ефекти.
Химически цианидите, които действат като мощни отрови, са неорганични цианиди, като натриев цианид (NaCN), калиев цианид (KCN) и цианоген хлорид (ClCN).
ОТКЪДЕ ИНОРГАНИЧНИЯ ЦИАНИД?
Всеки вид неорганичен цианид произлиза от дисоциацията на циановодород (HCN или циановодород) или една от неговите соли (която от своя страна може да бъде цианид).
Циановодородът е неорганична молекула, резултат от обединението на циано група (CN) с водороден атом (H). Това е силно токсична слаба киселина и може да се счита за особен пример за неорганичен цианид.
Моля обърнете внимание: натриев цианид и калиев цианид са две соли на циановодород.
Цианоген хлоридът, от друга страна, е производно на сол на циановодород; за да бъдем точни, това е производно на натриев цианид.
ОРГАНИЧЕН ЦИАНИД
В природата цианоанионът CN също образува химични съединения с органични молекули (например: метилови групи и т.н.), което води до появата на видове органичен цианид.
Известни също като нитрили, органичните цианиди са слабо токсични или стават токсични само в определени случаи; те обаче са все по -малко отровни от неорганичните цианиди.

Имот
Свойствата на цианида зависят от това кои атоми са свързани с цианогрупата CN.
Циановодородната киселина е бледосиня или безцветна течност при стайна температура, докато е безцветен газ при високи температури. И в течна, и в газообразна форма има миризма, наподобяваща тази на горчиви бадеми.
Натриевият цианид и калиевият цианид се появяват като бели прахове и отделят - подобно на циановодорода - миризма, сравнима с тази на горчивите бадеми.
Цианоген хлоридът е безцветен втечнен газ, по -тежък от въздуха и със специфична остра миризма.
Къде е?
В природата, както и в зърната на някои плодове, цианидът присъства и в различни растителни видове; растенията го държат в листата и / или в кората и го използват, за да се защитят от тревопасни животни.
В допълнение към растенията, други живи същества, които произвеждат цианид (или вещества, съдържащи цианогрупата CN), са някои бактерии и някои гъби.
ЦИАНИД КАТО СГОРИТЕЛЕН ПРОДУКТ
Циановодородът е възможен продукт от горивните процеси.
За да бъдем точни, той присъства в отработените газове на двигатели с вътрешно горене, в цигарения дим, който се получава при изгарянето на последните и в изпаренията, получени от сливането на пластмасови материали на базата на акрилонитрил (органично съединение, съдържащо циано група CN).
Използва
В производството цианидът се използва широко. Всъщност хартиената промишленост (за производство на хартия), текстилната промишленост (за производство на тъкани и т.н.), индустрията за производство на пластмаса, фотографската индустрия (за производство на всички тези химични съединения за разработването на снимките), металургичната промишленост (за производство на стомана и желязо, за измиване на метали и за поцинковане), индустрията, която се занимава с пречистването на отпадъчни води и промишлеността за производство на пестициди (срещу паразити и др.) за различни видове среда.
По очевидни причини в отпадъчните продукти от всички гореспоменати дейности могат да се открият следи от цианид.
ПРОШЛИ ИЗПОЛЗВАНИЯ
В миналото циановодородът е намирал приложение за трагични цели.
Например по време на Втората световна война нацистка Германия го използва - под името Zyklon B - като токсичен агент в газовите камери на лагерите на смъртта.
Дифузия
Цианидът има способността да се разпространява във вода, почва и въздух (N.B .: във въздуха е под формата на газ).
Хората могат да влязат в контакт с цианид, като дишат замърсен въздух, пият замърсена вода, ядат заразена храна или докосват замърсена почва.
„Ежедневен“ източник на цианид - на който са изложени много хора - е цигареният дим.
Ефекти
След излагане, отнема малко време цианидът да навлезе в кръвния поток и да се разпространи по цялото тяло чрез кръвта.
Човешкото тяло реагира на наличието на цианид по различни начини, в зависимост от това дали дозите са много ниски или средно високи.
Когато дозите са много ниски, цианидът се трансформира, чрез поредица от клетъчни реакции, в тиоцианат, химично съединение, което е безвредно за здравето и което човешкото същество елиминира чрез урината. Освен това, винаги в ниски дози, цианидът се комбинира с витамин В12 и полученият бином имат благоприятен ефект както върху нервните клетки, така и върху кръвните клетки.
Когато, от друга страна, дозите са средни до високи, способността на човешкия организъм да трансформира цианида в тиоцианат се потиска (поради прекомерно натоварване) и въпросното токсично вещество не позволява на клетките да използват кислорода. "кислородът води до смъртта на самите клетки.
Сърцето, дихателната система и централната нервна система са най -засегнати от голямото излагане на цианид.
Моля обърнете внимание: трябва да се отбележи, за да се избегне съмнение, че хроничното излагане на много малки дози цианид може да има токсични ефекти, подобни на тези, предизвикани от излагане на средно високи дози.
ТОКСИЧНОСТ
Токсичните ефекти на цианида върху човешкото здраве зависят от три фактора: дозата на токсичното вещество, с което човек е влязъл в контакт, продължителността на експозиция и вида на цианида.
Обикновено излагането на междинни дози цианид включва:
- Ускоряване на дишането;
- Чувство на безпокойство;
- Виене на свят;
- Чувство за слабост;
- Главоболие
- Гадене и чувство на повръщане;
- Ускоряване на сърдечния ритъм.
Ако дозите на цианид са високи, гореспоменатите прояви са свързани със:
- Конвулсии;
- Хипотония;
- Забавяне на сърдечния ритъм
- Загуба на съзнание;
- Затруднено дишане и затруднено дишане, поради белодробни проблеми
- Сърдечен арест.
Ефектите от експозицията на цианид започват да се проявяват само след няколко секунди / минути.Дозата влияе главно върху скоростта на настъпване на ефектите.
Обикновено смъртта от излагане на цианид настъпва в резултат на тежка дихателна недостатъчност или сърдечен арест.
ДЪЛГОСРОЧНИ ЕФЕКТИ
Според няколко клинични проучвания, хората, които оцелеят след „масивна експозиция на цианиди, са склонни да развият постоянни неврологични проблеми, някои от които имитират симптоми, много подобни на тези на болестта на Паркинсон“.
ЛЕТАЛ ДОЗА
Когато дозите цианид са смъртоносни, експертите говорят за „смърт от отравяне с цианид“.
За натриев цианид и калиев цианид смъртоносната доза за хората е 200-300 mg; за циановодорода, от друга страна, леталната доза за хората е 50 mg.
Терапия
Излагането на токсични дози цианид представлява спешна медицинска помощ, която трябва да се лекува много бързо и по най -подходящия начин.
Като цяло първите терапевтични показания са:
- Отдалечете се възможно най -бързо от мястото / околната среда на експозиция и се преместете на незамърсено място;
- Свалете дрехите си, в случай че са замърсени, и ги поставете обратно в найлонов плик;
- Измивайте очите си на всеки 10-15 минути, ако изгорят;
- Измийте всяка част от кожата, която е влязла в контакт с цианида, със сапун и вода;
- Обадете се за медицинска помощ.
Когато пристигне медицинска помощ, те ще завършат лечението, осигурявайки кислород на съответното лице и противоотрова.
Антидотите срещу излагане на големи дози цианид са натриев тиосулфат, натриев нитрит и хидроксокобаламин.