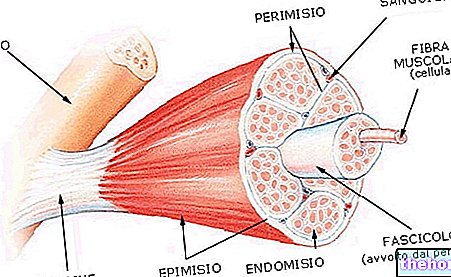
Структура и функции
Хемоглобинът е металопротеин, съдържащ се в червените кръвни клетки, отговорен за транспортирането на кислород в кръвния поток.Всъщност кислородът е само умерено разтворим във вода; следователно количествата, разтворени в кръвта (по -малко от 2% от общото количество), не са достатъчни, за да задоволят метаболитните нужди на тъканите. Следователно необходимостта от конкретен превозвач е очевидна.
В кръвния поток кислородът не може да се свърже директно и обратимо с протеините, както се случва вместо металите като мед и желязо.Не е изненадващо, че в центъра на всяка протеинова субединица от хемоглобин, обвита в протеинова обвивка, откриваме т.нар. група EME, с метално сърце, представено от железен атом в окислително състояние на Fe2 + (редуцирано състояние), което свързва кислорода по обратим начин.
Анализ на кръвта
- Нормални стойности на хемоглобина в кръвта: 13-17 g / 100 ml
При жените стойностите са средно 5-10% по-ниски, отколкото при мъжете.
Възможни причини за висок хемоглобин
- Полицитемия
- Удължен престой на високо ниво
- Хронични белодробни заболявания
- Сърдечно заболяване
- Кръвен допинг (използване на еритропоетин и производни или вещества, които имитират тяхното действие)
Възможни причини за нисък хемоглобин
- Анемии
- Дефицит на желязо (недостиг на желязо)
- Обилно кървене
- Карциноми
- Бременност
- Таласемия
- Изгаряния
Следователно съдържанието на кислород в кръвта се определя чрез сумиране на малкото количество, разтворено в плазмата с фракцията, свързана с хемоглобиновото желязо.
Повече от 98% от кислорода в кръвта е свързан с хемоглобина, който от своя страна циркулира в кръвния поток, разпределен в червените кръвни клетки.
Като се има предвид централната роля на този метал, синтезът на хемоглобин изисква адекватен прием на желязо в храната. Около 70% от желязото в организма всъщност се съдържа в хемогрупите на хемоглобина.
Хемоглобинът се състои от 4 субединици, които са структурно много сходни с миоглобина *.
* Докато хемоглобинът пренася кислород от белите дробове до тъканите, миоглобинът пренася кислорода, освободен от хемоглобина в различните клетъчни органели, които го използват (например митохондриите).

Хемоглобинът е голям и сложен металопротеин, характеризиращ се с четири глобуларни протеинови вериги, съответно увити около хем група, която съдържа Fe2 +.
Следователно за всяка молекула хемоглобин откриваме четири хем групи, увити в относителната глобуларна протеинова верига. Тъй като във всяка молекула на хемоглобина има четири железни атома, всяка молекула на хемоглобина може да свърже четири кислородни атома към себе си, според обратимата реакция:
Hb + 4O2 ← → Hb (O2) 4
Както е известно на повечето, задачата на хемоглобина е да поеме кислород в белите дробове, да го освободи до клетките, които се нуждаят от него, да вземе въглероден диоксид от тях и да го освободи в белите дробове, където чилото започва отново.
По време на преминаването на кръв в капилярите на белодробните алвеоли, хемоглобинът свързва кислорода със себе си, който впоследствие се освобождава в тъканите в периферната циркулация. Този обмен възниква, защото връзките на кислорода с желязото от групата EME са лабилни и чувствителни към много фактори, най -важният от които е напрежението или частичното налягане на кислорода.
Свързване на кислорода с хемоглобина и ефекта на Бор
В белите дробове плазменото кислородно напрежение се увеличава поради дифузията на газ от алвеолите към кръвта (↑ PO2); това повишаване кара хемоглобина да се свързва жадно с кислорода; обратното се случва в периферните тъкани, където концентрацията на разтворен кислород в кръвта намалява (↓ PO2) и парциалното налягане на въглеродния диоксид се увеличава (↑ CO2); това предизвиква хемоглобин да отделя кислород и да се зареди с CO2. Опростяване на концепцията, доколкото е възможно, колкото повече въглероден диоксид присъства в кръвта, толкова по -малко кислород остава свързан с хемоглобина.
Въпреки че количеството кислород, физически разтворен в кръвта, е много ниско, той играе основна роля. Всъщност това количество влияе силно върху силата на връзката между кислорода и хемоглобина (както и представлява „важна референтна стойност за регулиране на белодробната вентилация).
Обобщавайки всичко с графика, количеството кислород, свързано с хемоглобина, нараства по отношение на рО2 след сигмоидна крива:

Фактът, че регионът на плато е толкова голям, поставя важна граница на безопасност при максималното насищане на хемоглобина по време на преминаването в белите дробове. дори частично налягане на кислород, равно на 70 mmHg (типична поява на някои заболявания или престой на голяма надморска височина), процентите на наситен хемоглобин остават близо до 100%.
В района на максимален наклон, когато частичното напрежение на кислорода падне под 40 mmHg, способността на хемоглобина да свързва кислорода рязко спада.
В условия на покой, PO2 във вътреклетъчните течности е приблизително 40 mmHg; на това място, поради законите на газовете, кислородът, разтворен в плазмата, се дифундира към по -бедните тъкани на О2, преминавайки през капилярната мембрана.Следствие на това плазменото напрежение на О2 пада допълнително и това благоприятства освобождаването на кислород от хемоглобина. . При интензивни физически натоварвания, от друга страна, кислородното напрежение в тъканите пада до 15 mmHg или по -малко, в резултат на което кръвта се изчерпва значително с кислород.
Както беше казано, в условия на покой важно количество кислороден хемоглобин напуска тъканите, оставайки на разположение в случай на нужда (например за справяне с внезапно увеличаване на метаболизма в някои клетки).
Плътната линия, показана на изображението по -горе, се нарича крива на дисоциация на хемоглобина; обикновено се определя in vitro при рН 7,4 и при температура 37 ° С.
Ефектът на Бор има последици както върху приема на О2 на белодробно ниво, така и върху освобождаването му на тъканно ниво.
Когато има повече разтворен въглероден диоксид под формата на бикарбонат, хемоглобинът освобождава по -лесно кислорода и се зарежда с въглероден диоксид (под формата на бикарбонат).

Същият ефект се получава при подкисляване на кръвта: колкото повече намалява рН на кръвта и толкова по -малко кислород остава свързан с хемоглобина; не е изненадващо, че в кръвта въглеродният диоксид се разтваря главно под формата на въглена киселина, която се дисоциира.



В чест на своя откривател, ефектът на рН или въглероден диоксид върху дисоциацията на кислорода е известен като ефекта на Бор.
Както се очакваше, в кисела среда хемоглобинът отделя кислород по -лесно, докато в основна среда връзката с кислорода е по -силна.

Други фактори, способни да променят афинитета на хемоглобина към кислорода, включват температурата. По -специално, афинитетът на хемоглобина към кислорода намалява с повишаване на телесната температура. Това е особено изгодно през зимните и пролетните месеци, тъй като температурата на белодробната кръв (в контакт с въздухът от външната среда) е по -нисък от този, достигнат в тъканите, където следователно се улеснява отделянето на кислород.

2.3 дифосфоглицератът е междинен продукт в гликолизата, който влияе върху афинитета на хемоглобина към кислорода. увеличаване на 2,3 дифосфоглицерата, например при анемия, сърдечно-белодробна недостатъчност и по време на престоя на голяма надморска височина.
По принцип ефектът от 2,3 бисфосфоглицерат е сравнително бавен, особено в сравнение с бързата реакция на промените в рН, температурата и парциалното налягане на въглеродния диоксид.

Ефектът на Бор е много важен по време на интензивна мускулна работа; в такива условия всъщност в най -изложените на стрес тъкани има локално повишаване на температурата и налягането на въглеродния диоксид, следователно и на киселинността на кръвта. Както е обяснено по -горе, всичко това благоприятства отделянето на кислород към тъканите, измествайки кривата на дисоциация на хемоглобина надясно.

.jpg)