Активни съставки: Сунитиниб
SUTENT 12,5 mg твърди капсули
SUTENT 25 mg твърди капсули
SUTENT 37,5 mg твърди капсули
SUTENT 50 mg твърди капсули
Показания Защо се използва Sutent? За какво е?
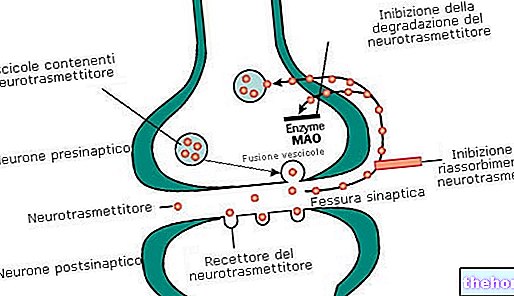
Sutent съдържа активното вещество сунитиниб, което е инхибитор на протеин киназата. Използва се за лечение на рак, като предотвратява активността на специфична група протеини, за които е известно, че участват в растежа и разпространението на раковите клетки.
Sutent ще Ви бъде предписан само от лекар, който има опит в употребата на лекарства против рак.
Sutent се използва за лечение на възрастни със следните видове рак:
- Стомашно -чревен стромален рак (GIST), вид рак на стомаха и червата, в случаите, когато иматиниб (друго противораково лекарство) вече не действа или не може да се приема.
- Метастатичен рак на бъбреците (MRCC), вид рак на бъбреците, който се е разпространил в други части на тялото.
- Невроендокринни тумори на панкреаса (pNETs) (тумори на клетките на панкреаса, произвеждащи хормони), които са прогресиращи или нерезектируеми
. Ако не сте сигурни как действа Sutent или защо това лекарство е предписано на Вас, попитайте Вашия лекар.
Противопоказания Когато Sutent не трябва да се използва
Не приемайте Sutent:
- Ако сте алергични към сунитиниб или към някоя от останалите съставки на това лекарство (изброени в точка 6).
Предпазни мерки при употреба Какво трябва да знаете, преди да приемете Sutent
Кажете на Вашия лекар, преди да приемете Sutent:
- Ако имате високо кръвно налягане. Sutent може да причини повишаване на кръвното Ви налягане.Вашият лекар може да провери кръвното Ви налягане, докато приемате Sutent и ще се наложи да приемате лекарства за понижаване на кръвното Ви налягане, ако е необходимо.
- Ако имате или сте имали кръвни нарушения, проблеми с кървене или синини. Лечението със Sutent може да носи повишен риск от кървене, промени в броя на определени кръвни клетки, чийто дефицит води до анемия или влияе върху способността на кръвта да се съсирва. Рискът от кървене може да бъде по -висок, ако приемате варфарин или аценокумарол, лекарства, които разреждат кръвта, за да предотвратят образуването на кръвни съсиреци.Уведомете Вашия лекар, ако получите кървене, докато приемате Sutent.
- Ако имате проблеми със сърцето. Sutent може да причини сърдечни проблеми. Уведомете Вашия лекар, ако се чувствате много уморени, имате задух или имате подути стъпала и глезени.
- Ако получите анормални промени в сърдечния ритъм. Sutent може да причини промени в сърдечния ритъм. Докато се лекувате със Sutent, Вашият лекар може да Ви направи електрокардиограма, за да оцени степента на тези промени. Кажете на Вашия лекар, ако се чувствате замаяни, припаднали или имате необичайни сърдечни удари, докато приемате Sutent.
- Ако наскоро сте имали проблеми с кръвни съсиреци във вените и / или артериите (видове кръвоносни съдове), включително инсулт, инфаркт, емболия или тромбоза. Свържете се незабавно с Вашия лекар, ако получите симптоми като стягане или болка в гърдите, болка в ръцете, гърба, шията или челюстта, задух, изтръпване или слабост от едната страна на тялото, треперене при ходене, болка по време на лечението със Sutent. Главоболие или замаяност.
- Ако имате проблеми с щитовидната жлеза. Sutent може да причини проблеми с щитовидната жлеза. Кажете на Вашия лекар, ако се уморите по -лесно, докато приемате Sutent, обикновено се чувствате по -студени от другите хора или гласът Ви намалява. Функцията на щитовидната жлеза трябва да се проверява преди да приемате Sutent и редовно, докато приемате лекарството. Ако щитовидната жлеза не произвежда достатъчно хормони на щитовидната жлеза, може да се наложи прием на заместващ хормон на щитовидната жлеза.
- Ако имате или сте имали проблеми с панкреаса или жлъчния мехур. Уведомете Вашия лекар, ако получите някой от следните признаци и симптоми: болка в стомаха (горната част на корема), гадене, повръщане и треска, които могат да бъдат причинени от възпаление на панкреаса или жлъчния мехур.
- Ако имате или някога сте имали чернодробни проблеми. Уведомете Вашия лекар, ако по време на лечението със Sutent изпитате някой от следните признаци и симптоми на чернодробни проблеми: сърбеж, пожълтяване на кожата или очите, потъмняване на урината и болка или дискомфорт в горната дясна част на стомаха. Вашият лекар трябва провеждане на тестове за проверка на чернодробната функция преди и по време на лечението със Sutent и според клиничната целесъобразност.
- Ако имате или сте имали бъбречни проблеми. Лекарят ще следи функцията на бъбреците.
- Ако Ви предстои операция или наскоро сте претърпели операция. Sutent може да повлияе на начина на зарастване на раните Ви. Като цяло, ако Ви предстои операция, ще трябва да спрете употребата на Sutent. Вашият лекар ще реши кога да започне отново Sutent лечение.
- Препоръчително е да започнете стоматологичен преглед преди започване на лечението със Sutent.
- ако имате или сте имали болка в устата, зъбите и / или челюстта, подуване или рани в устата, изтръпване или усещане за тежест в челюстта или разхлабване на зъбите, незабавно уведомете Вашия лекар и зъболекар.
- ако сте подложени на инвазивно стоматологично лечение или стоматологична операция, кажете на Вашия лекар, че се лекувате със Sutent, особено ако приемате интравенозно бифосфонати или сте ги приемали преди това. Бисфосфонатите са лекарства, използвани за предотвратяване на костни усложнения, които може да са предписани за друг медицински проблем.
- Ако имате или някога сте имали нарушения на кожата и подкожната тъкан. „Гангренозна пиодерма“ (болезнена язва на кожата) или „некротизиращ фасциит“ (бързо разпространяваща се „инфекция на кожата / меките тъкани, която може да бъде фатална) може да възникне по време на лечението с това лекарство. Прекратяване на лечението. Сериозни кожни реакции (Stevens-Johnson синдром, токсична епидермална некролиза, еритема мултиформе) са съобщени при употребата на сунитиниб, първоначално се появява на багажника като червеникави петна с формата на мишена или кръгли петна, често с мехури в центъра. Реакцията може да прогресира до широко разпространено образуване на мехури или лющене на кожата и може да бъде фатално. Ако развиете обрив или някой от тези кожни симптоми, незабавно се консултирайте с лекар.
- Ако имате или сте имали гърчове. Информирайте Вашия лекар възможно най -скоро, ако имате високо кръвно налягане, главоболие, загуба на зрение.
- Ако имате диабет. Нивата на кръвната захар трябва да се проверяват редовно при пациенти с диабет, за да се види дали дозата на лекарствата за диабет трябва да се промени, за да се сведе до минимум рискът от ниска кръвна захар.
Деца и юноши
Sutent не е показан за пациенти под 18 години. Sutent не е проучен при деца и юноши.
Взаимодействия Кои лекарства или храни могат да променят ефекта на Sutent
Уведомете Вашия лекар или фармацевт, ако приемате, наскоро сте приемали или е възможно да приемете други лекарства, включително тези, закупени без рецепта и тези без рецепта.
Някои лекарства могат да променят нивата на Sutent в организма. Трябва да уведомите Вашия лекар, ако приемате лекарства, които съдържат следните активни вещества:
- кетоконазол, итраконазол - използва се за лечение на гъбични инфекции
- еритромицин, кларитромицин, рифампицин - използвани за лечение на инфекции
- ритонавир - използва се за лечение на СПИН
- дексаметазон - кортикостероид, използван при няколко състояния
- фенитоин, карбамазепин, фенобарбитал - използва се за лечение на епилепсия и други неврологични състояния
- билкови препарати, съдържащи жълт кантарион (Hypericum perforatum) - използвани за лечение на депресия и тревожност
Достатъчно с храна и напитки
По време на лечението със Sutent трябва да се избягва приемът на сок от грейпфрут.
Предупреждения Важно е да знаете, че:
Бременност и кърмене
Ако сте бременна или подозирате, че сте бременна, моля уведомете Вашия лекар.
Sutent не трябва да се използва по време на бременност, освен ако не е строго необходимо. Вашият лекар ще обсъди с Вас възможните рискове от Sutent лечение по време на бременност.
Ако е възможна бременност, трябва да използвате надежден метод за контрацепция, докато се лекувате със Sutent.
Ако кърмите, моля уведомете Вашия лекар. Не трябва да кърмите, докато се лекувате със Sutent.
Шофиране и работа с машини
Ако се чувствате замаяни или необичайно уморени, бъдете особено внимателни, когато шофирате или работите с машини.
Доза, метод и време на приложение Как да използвате Sutent: Дозировка
Винаги приемайте това лекарство точно както Ви е казал Вашият лекар.
Ако се съмнявате, консултирайте се с Вашия лекар. Вашият лекар ще Ви предпише подходящата доза, в зависимост от вида рак, който трябва да лекувате. Ако се лекувате за GIST или MRCC, обичайната доза е 50 mg веднъж дневно, която трябва да се приема в продължение на 28 дни (4 седмици), последвана от 14 дни (2 седмици) почивка (без лекарства), на цикли от 6 седмици. Ако се лекувате за pNET, обичайната доза е 37,5 mg веднъж дневно, без период на почивка. Вашият лекар ще определи дозата, от която се нуждаете, и кога да спрете лечението с Sutent. Sutent може да се приема със или без храна.
Предозиране Какво да направите, ако сте приели твърде много Sutent
Ако сте приели повече от необходимата доза Sutent
Ако случайно сте приели твърде много капсули, говорете незабавно с Вашия лекар. Може да се наложи медицинска помощ
Ако сте пропуснали да приемете Sutent
Не вземайте двойна доза, за да компенсирате пропуснатата доза.
Странични ефекти Какви са страничните ефекти на Sutent
Както всички лекарства, това лекарство може да предизвика нежелани реакции, въпреки че не всеки ги получава.
Свържете се незабавно с Вашия лекар, ако получите някоя от тези сериозни нежелани реакции (вижте също Какво трябва да знаете, преди да приемете Sutent):
Сърдечни проблеми. Уведомете Вашия лекар, ако се чувствате много уморени, имате задух или имате подути стъпала и глезени. Това може да са симптоми на сърдечни проблеми като сърдечна недостатъчност и проблеми със сърдечния мускул (кардиомиопатия).
Проблеми с белите дробове или дишането. Уведомете Вашия лекар, ако почувствате кашлица, болка в гърдите, внезапна поява на задух или кашлица с кръв. Това може да са симптоми на белодробна емболия, която възниква, когато кръвни съсиреци пътуват до белите дробове.
Бъбречни проблеми. Уведомете Вашия лекар, ако получите „променена честота или отсъствие на уриниране, което може да бъде симптоми на“ бъбречна недостатъчност.
Кървене. Уведомете незабавно Вашия лекар, ако получите някой от следните симптоми или сериозен проблем с кървенето, докато приемате Sutent: подут, болезнен стомах (корем); повръщане с кръв; тъмни, лепкави изпражнения; главоболие или промени в психичното състояние, кашляне на кръв или храчки с кръв от белите дробове или дихателните пътища.
Унищожаване на тумора, причиняващо перфорация на червата. Кажете на Вашия лекар, ако имате силна болка в червата, треска, гадене, повръщане, кръв в изпражненията или промени в навиците на червата.
Други нежелани реакции, които могат да възникнат при Sutent са:
Много чести нежелани реакции (могат да засегнат повече от 1 на 10 души)
- Намаляване на броя на тромбоцитите, червените кръвни клетки и / или белите кръвни клетки (напр. Неутрофили).
- Недостиг на въздух
- Високо кръвно налягане.
- Прекомерна умора, загуба на сила.
- Подуване, причинено от течност под кожата и около очите, дълбок алергичен обрив.
- Болка / дразнене в устата, болезненост / възпаление / сухота в устата, нарушения на вкуса, стомашно разстройство, гадене, повръщане, диария, запек, коремна болка / подуване, загуба / намаляване на апетита.
- Намалена активност на щитовидната жлеза (хипотиреоидизъм).
- Замайване
- Главоболие.
- Кървене от носа.
- Болки в гърба, болки в ставите.
- Болка в ръцете и краката.
- Пожълтяване на кожата / обезцветяване на кожата, прекомерна пигментация на кожата, обезцветяване на косата, обрив по дланите и ходилата, обрив, суха кожа.
- Кашлица.
- Треска.
- Трудно заспиване.
Чести нежелани реакции (могат да засегнат 1 до 10 на 100 души)
- Образуване на съсиреци в кръвоносните съдове.
- Недостатъчно кръвоснабдяване на сърдечния мускул, поради запушване или свиване на коронарните артерии.
- Болка в гърдите.
- Намалено количество кръв, изпомпвано от сърцето.
- Задържане на течности също около белите дробове.
- Инфекции.
- Намалено ниво на кръвната захар. Ако имате признаци и симптоми на ниска кръвна захар: Информирайте Вашия лекар възможно най -скоро, ако почувствате умора, сърцебиене, изпотяване, глад и загуба на съзнание.
- Загуба на протеин в урината, което понякога води до подуване.
- Грипен синдром.
- Анормални кръвни тестове, включително нивата на чернодробните и панкреатичните ензими.
- Високи нива на пикочна киселина в кръвта.
- Хемороиди, ректална болка, кървене от венците, затруднено преглъщане или невъзможност за преглъщане.
- Парене или болезнено усещане в езика, възпаление на лигавицата на храносмилателния тракт, излишни газове в стомаха или червата.
- Отслабване.
- Мускулно -скелетна болка (болка в мускулите и костите), мускулна слабост, мускулна умора, мускулни болки, мускулни спазми.
- Сухота в носа, запушване на носа.
- Прекомерно разкъсване.
- Промени в чувствителността на кожата, суха кожа, сърбеж, лющене и възпаление на кожата, образуване на мехури, акне, обезцветяване на ноктите, косопад.
- Анормални усещания в крайниците.
- Прекомерно намаляване / увеличаване на чувствителността, особено при допир.
- Парене в стомаха.
- Дехидратация.
- Зачервяване на лицето.
- Промяна в цвета на урината.
- Депресия.
- Втрисане.
Нечести нежелани реакции (могат да засегнат 1 до 10 на 1000 души)
- Инфекции на меките тъкани, включително в аногениталната област, потенциално животозастрашаващи. Свържете се незабавно с Вашия лекар, ако получите симптоми на инфекция около рана на кожата, включително треска, болка, зачервяване, подуване или оттичане на гной или кръв.
- Удар.
- Инфаркт, причинен от прекъснато или намалено кръвоснабдяване на сърцето.
- Промени в електрическата активност на сърцето или променен сърдечен ритъм.
- Течност около сърцето (перикарден излив).
- Чернодробна недостатъчност.
- Болка в стомаха (корема), причинена от „възпаление на панкреаса.
- Унищожаване на тумора, причиняващо перфорация на червата.
- Възпаление (подуване и зачервяване) на жлъчния мехур със или без свързани камъни.
- Ненормален комуникационен канал между две телесни кухини или с кожата.
- Болка в устата, зъбите и / или челюстта, подуване или дразнене в устата, изтръпване или усещане за тежест в челюстта или разхлабване на зъбите. Това може да са признаците и симптомите на увреждане на челюстната кост (остеонекроза). Информирайте незабавно Вашия лекар и зъболекар, ако получите някой от тези признаци и симптоми.
- Прекомерното производство на хормони на щитовидната жлеза води до повишен метаболизъм. Проблеми с зарастването на рани след операция.
- Увеличаване на мускулния ензим в кръвта (креатин фосфокиназа).
- Неподходяща и прекомерна реакция към алергени.
Редки нежелани реакции (могат да засегнат 1 до 10 на 10 000 души)
- Тежки реакции на кожата и / или лигавиците (синдром на Stevens-Johnson, токсична епидермална некролиза, мултиформен еритем).
- Синдром на туморна лиза (TLS) - TLS обхваща набор от метаболитни усложнения, които могат да възникнат по време на лечението на рак. Те са причинени от продуктите на разпадане на засегнатите ракови клетки и могат да включват: гадене, задух, неравномерен сърдечен ритъм, мускулни крампи, конвулсии, мътна урина и умора, свързани с анормални резултати от лабораторни изследвания (високи нива на калий, пикочна киселина и фосфорна киселина и ниски нива на калций в кръвта), което може да доведе до промени в бъбречната функция и остра бъбречна недостатъчност.
- Ненормално разграждане на мускулите, което може да причини бъбречни проблеми (рабдомиолиза).
- Нарушена мозъчна функция, която може да доведе до различни симптоми, като главоболие, объркване, припадъци и загуба на зрение (синдром на обратима обратна левкоенцефалопатия).
- Болезнена язва на кожата (гангренозна пиодермия).
- Възпаление на черния дроб (хепатит).
- Възпаление на щитовидната жлеза.
Докладване на странични ефекти
Ако получите някакви нежелани реакции, говорете с Вашия лекар.Това включва всички възможни нежелани реакции, които не са изброени в тази листовка. Можете също да съобщите нежелани реакции директно чрез националната система за докладване, изброена в допълнение V. Чрез съобщаване на странични ефекти можете да помогнете за предоставяне на повече информация за безопасността на това лекарство.
Срок на годност и задържане
- Съхранявайте това лекарство на място, недостъпно за деца.
- Не използвайте това лекарство след срока на годност, отбелязан върху картонената опаковка и върху етикета след "Годен до:" Срокът на годност се отнася до последния ден от месеца.
- Този лекарствен продукт не изисква специални условия за съхранение.
- Не използвайте това лекарство, ако забележите, че опаковката е повредена или показва признаци на подправяне.
Не изхвърляйте никакви лекарства през отпадъчни води или битови отпадъци. Попитайте Вашия фармацевт как да изхвърлите лекарства, които вече не използвате. Това ще помогне за опазването на околната среда.
Какво съдържа Sutent
Сутентни 12,5 mg твърди капсули
Активната съставка е сунитиниб. Всяка капсула съдържа сунитиниб малат, еквивалентен на 12,5 mg сунитиниб.
Другите съставки са:
- Съдържание на капсулата: манитол (Е421), кроскармелоза натрий, повидон (К-25) и магнезиев стеарат.
- Обвивка на капсулата: желатин, червен железен оксид (E172) и титанов диоксид (E171).
- Мастило: шеллак, пропилен гликол, натриев хидроксид, повидон и титанов диоксид (Е171).
Сутентни 25 mg твърди капсули
Активната съставка е сунитиниб. Всяка капсула съдържа сунитиниб малат, еквивалентен на 25 mg сунитиниб.
Другите съставки са:
- Съдържание на капсулата: манитол (Е421), кроскармелоза натрий, повидон (К-25) и магнезиев стеарат.
- Обвивка на капсулата: желатин, титанов диоксид (E171), жълт железен оксид (E172), червен железен оксид (E172), черен железен оксид (E172).
- Мастило: шеллак, пропилен гликол, натриев хидроксид, повидон и титанов диоксид (E171)
Сутентен 37,5 mg твърди капсули
Активната съставка е сунитиниб. Всяка капсула съдържа сунитиниб малат, еквивалентен на 37,5 mg сунитиниб.
Другите съставки са:
- Съдържание на капсулата: манитол (Е421), кроскармелоза натрий, повидон (К-25) и магнезиев стеарат.
- Обвивка на капсулата: желатин, титанов диоксид (E171), жълт железен оксид (E172).
- Мастило: шеллак, пропилен гликол, калиев хидроксид, черен железен оксид (Е172).
Сутентен 50 mg твърди капсули
Активната съставка е сунитиниб. Всяка капсула съдържа сунитиниб малат, еквивалентен на 50 mg сунитиниб.
Другите съставки са:
- Съдържание на капсулата: манитол (Е421), кроскармелоза натрий, повидон (К-25) и магнезиев стеарат.
- Обвивка на капсулата: желатин, титанов диоксид (E171), жълт железен оксид (E172), червен железен оксид (E172) и черен железен оксид (E172).
- Мастило: шеллак, пропилен гликол, натриев хидроксид, повидон и титанов диоксид (Е171).
Описание на това как изглежда Sutent и съдържанието на опаковката
Sutent 12,5 mg се предлага като твърди желатинови капсули с оранжева капачка и тяло, с "Pfizer" в бяло мастило върху капачката и "STN 12,5 mg" върху тялото, съдържащо цветни гранули. Жълто-оранжево.
Sutent 25 mg се предлага като твърди желатинови капсули с карамелена капачка и оранжево тяло, с "Pfizer" с бяло мастило върху капачката и "STN 25 mg" върху тялото, съдържащо цветни гранули. Жълто-оранжево.
Sutent 37,5 mg се предлага като твърди желатинови капсули с жълта капачка и тяло, с "Pfizer" с черно мастило върху капачката и "STN 37,5 mg" върху тялото, съдържащо цветни гранули. Жълто-оранжево.
Sutent 50 mg се предлага под формата на твърди желатинови капсули с капачка и тяло в цвят карамел, с "Pfizer" с бяло мастило върху капачката и "STN 50 mg" върху тялото, съдържащи жълто-оранжеви гранули. Предлага се в бутилки от 30 капсули и перфорирани блистери за единична доза, съдържащи 28 х 1 капсули.
Не всички опаковки могат да бъдат пуснати на пазара.
Източник на листовката: AIFA (Италианска агенция по лекарствата). Съдържание, публикувано през януари 2016 г. Наличната информация може да не е актуална.
За да имате достъп до най-актуалната версия, препоръчително е да получите достъп до уебсайта на AIFA (Италианска агенция по лекарствата). Отказ от отговорност и полезна информация.
01.0 ИМЕ НА ЛЕКАРСТВЕНИЯ ПРОДУКТ
SUTENT 12,5 MG ТВЪРДИ КАПСУЛИ
02.0 КАЧЕСТВЕН И КОЛИЧЕСТВЕН СЪСТАВ
Всяка капсула съдържа сунитиниб малат, съответстващ на 12,5 mg сунитиниб.
За пълния списък на помощните вещества вижте точка 6.1.
03.0 ЛЕКАРСТВЕНА ФОРМА
Твърда капсула.
Желатинови капсули с оранжева капачка и тяло, маркирани с бяло мастило "Pfizer" на капачката, "STN 12,5 mg" върху тялото и съдържащи жълто-оранжеви гранули.
04.0 КЛИНИЧНА ИНФОРМАЦИЯ
04.1 Терапевтични показания
Стромален тумор на стомашно -чревния тракт (GIST)
SUTENT е показан за лечение на нерезектируем и / или метастатичен стомашно -чревен стромален рак (GIST) при възрастни след неуспех на лечението с иматиниб поради резистентност или непоносимост.
Метастатичен бъбречно -клетъчен карцином (MRCC)
SUTENT е показан за лечение на напреднал / метастатичен бъбречно -клетъчен карцином (MRCC) при възрастни.
Невроендокринни тумори на панкреаса (pNET)
SUTENT е показан за лечение на добре диференцирани, нерезектируеми или метастатични невроендокринни тумори на панкреаса (pNETs) при прогресиращо заболяване при възрастни.
Опитът с SUTENT като лекарство от първа линия е ограничен (вж. Точка 5.1).
04.2 Дозировка и начин на приложение
Лечението със сунитиниб трябва да се започне от лекар с опит в прилагането на противоракови средства.
Дозировка
За GIST и MRCC препоръчителната доза SUTENT е 50 mg, която трябва да се приема перорално веднъж дневно в продължение на 4 последователни седмици, последвана от 2 седмици почивка (график 4/2), за да се проведе пълен курс от 6 седмици.
За pNET препоръчителната доза SUTENT е 37,5 mg, която трябва да се приема перорално веднъж дневно, без планиран период на почивка.
Корекция на дозата
Безопасност и поносимост
За GIST и MRCC може да се направи промяна на дозата на стъпки от 12,5 mg въз основа на индивидуалната безопасност и поносимост на пациента. Дневната доза не трябва да надвишава 75 mg, нито да се намалява под 25 mg.
За pNET могат да бъдат направени промени в дозата на стъпки от 12,5 mg въз основа на индивидуалната безопасност и поносимост на пациента. Максималната доза, приложена във фаза 3 pNET проучване, е 50 mg на ден.
Може да се наложи да се спре приема на някои дози въз основа на безопасността и поносимостта на отделния пациент.
Инхибитори / индуктори на CYP3A4
Едновременното приложение на сунитиниб с мощни индуктори на CYP3A4, като рифампицин, трябва да се избягва (вж. Точки 4.4. И 4.5). Ако това не е възможно, може да се наложи дозата на сунитиниб да се увеличава на стъпки от 12,5 mg (до 87,5 mg / ден за GIST и MRCC или 62,5 mg / ден за pNET) въз основа на внимателно проследяване на поносимостта.
Едновременното приложение на сунитиниб с мощни инхибитори на CYP3A4, като например кетоконазол, трябва да се избягва (вж. Точки 4.4 и 4.5). Ако това не е възможно, може да се наложи дозата на сунитиниб да се намали до минимална доза от 37,5 mg на ден за GIST и MRCC или 25 mg на ден за pNET, въз основа на внимателно проследяване на поносимостта.
Трябва да се обмисли изборът на алтернативен съпътстващ лекарствен продукт без или с минимален потенциал да индуцира или инхибира CYP3A4.
Специални популации
Педиатрична популация
Безопасността и ефикасността на сунитиниб при пациенти на възраст под 18 години не са установени.
Няма налични данни.
Няма индикации за специфична употреба на сунитиниб при деца от раждането до 6 -годишна възраст при лечение на нерезектабилен и / или метастатичен GIST след неуспех на лечението с иматиниб поради резистентност или непоносимост. Няма индикации за специфична употреба на сунитиниб при педиатричната популация при лечение на MRCC и при лечение на добре диференцирани, нерезектируеми или метастатични pNETs в прогресията на заболяването.
Употребата на сунитиниб в педиатричната популация не се препоръчва.
Пациенти в старческа възраст (≥ 65 години))
Приблизително една трета от пациентите, включени в клинични изпитвания, които са получавали сунитиниб, са на възраст 65 години или по -големи.
Чернодробно увреждане
Не се изисква първоначална корекция на дозата, когато сунитиниб се прилага при пациенти с леко или умерено чернодробно увреждане (стадия А и В по Child-Pugh). Употребата на сунитиниб при лица с тежко чернодробно увреждане (стадий С по Child-Pugh) не е проучена, поради което не се препоръчва употребата му при пациенти с чернодробно увреждане (вж. Точка 5.2).
Бъбречна недостатъчност
Не се налага първоначално коригиране на дозата, когато сунитиниб се прилага при пациенти с бъбречно увреждане (умерено до тежко) или бъбречно заболяване в краен стадий (ESRD), подложени на хемодиализа. Следващите корекции на дозата трябва да се направят въз основа на безопасността и поносимостта на отделния пациент (вж. Точка 5.2).
Начин на приложение
SUTENT е за перорално приложение. Може да се приема със или без храна.
Ако не се приеме доза, не трябва да се дава допълнителна доза. На следващия ден пациентът трябва да приеме обичайната предписана доза.
04.3 Противопоказания
Свръхчувствителност към активното вещество или към някое от помощните вещества, изброени в точка 6.1.
04.4 Специални предупреждения и подходящи предпазни мерки при употреба
Едновременното приложение със силни индуктори на CYP3A4 трябва да се избягва, тъй като може да намали плазмената концентрация на сунитиниб (вж. Точки 4.2 и 4.5).
Едновременното приложение с мощни инхибитори на CYP3A4 трябва да се избягва, тъй като това може да увеличи плазмената концентрация на сунитиниб (вж. Точки 4.2 и 4.5).
Нарушения на кожата и тъканите
Обезцветяването на кожата, което може да се дължи на цвета на активното вещество (жълто), е много честа нежелана реакция, възникваща при приблизително 30% от пациентите.Пациентите трябва да бъдат предупредени, че по време на лечението със сунитиниб могат да обезцветят косата или Други възможни дерматологични ефекти могат да включват сухота, удебеляване или напукване на кожата, мехури или случаен обрив по дланите или ходилата.
Горепосочените реакции не са кумулативни, като цяло са обратими и обикновено не водят до преустановяване на лечението. Съобщавани са случаи на гангренозна пиодермия, обикновено обратима след прекратяване на лекарството. Съобщавани са сериозни кожни реакции, включително случаи на мултиформен еритем ( EM) и случаи, приписвани на синдрома на Stevens-Johnson (SJS) и токсичната епидермална некролиза (NET), някои от тях са фатални. сунитиниб трябва да се прекрати. едновременно лечение с кортикостероиди или антисептици тамини.
Кръвоизлив и кървене, причинени от тумори
От постмаркетинговия опит са съобщени хеморагични събития, някои с фатален изход, включително стомашно-чревни, дихателни, уринарни и мозъчни кръвоизливи.
Епизоди на кървене се наблюдават при 18% от пациентите, лекувани със сунитиниб, в сравнение със 17% от пациентите в групата на плацебо в проучване на GIST фаза 3. Пациентите с MRCC на сунитиниб, които никога преди не са лекувани със сунитиниб, съобщават за събития с кървене в 39% от случаите в сравнение с 11% на пациенти, лекувани с IFN-α. Седемнадесет (4,5%) пациенти на сунитиниб в сравнение с 5 (1,7%) пациенти на IFN-α са имали епизоди на кървене от степен 3 или по-висока. Двадесет и шест процента от пациентите, получаващи сунитиниб за цитокин-рефрактерна MRCC, съобщават за епизоди на кървене.Кървене, с изключение на епистаксис, се наблюдава при 21,7% от пациентите, лекувани със сунитиниб, в сравнение с 9,85% от пациентите в групата на плацебо във фаза 3 pNET проучване. Рутинната оценка на това събитие трябва да включва пълна кръвна картина и физически преглед.
Епистаксисът е най -честата нежелана хеморагична реакция, която се съобщава при приблизително половината от пациентите със солидни тумори, които съобщават за кървене. Някои от тези епизоксични епизоди са били сериозни, но много рядко са били фатални.
Съобщавани са събития с туморен кръвоизлив, понякога свързани с туморна некроза; някои от тези кръвоизливи са фатални.
В клинични изпитвания "туморен кръвоизлив е настъпил при приблизително 2% от пациентите с ГИСТ. Тези събития могат да настъпят внезапно и в случай на рак на белия дроб могат да се проявят под формата на" тежка и животозастрашаваща хемоптиза или като белодробен кръвоизлив. Случаи на белодробен кръвоизлив, някои с фатален изход, са наблюдавани в клинични изпитвания и са докладвани също след пускане на пазара при пациенти, лекувани със сунитиниб за MRCC, GIST и рак на белия дроб. SUTENT не е одобрен за употреба при пациенти с рак на белия дроб.
Пациентите на едновременно лечение с антикоагуланти (напр. Варфарин, аценокумарол) могат да бъдат периодично проследявани чрез пълна кръвна картина (тромбоцити), коагулационни фактори (PT / INR) и физически преглед.
Стомашно -чревни нарушения
Диария, гадене / повръщане, коремна болка, диспепсия и стоматит / болки в устата са най -често съобщаваните стомашно -чревни нежелани реакции; Съобщавани са и случаи на езофагит (вж. Точка 4.8).
Поддържащите грижи за стомашно-чревни нежелани реакции, изискващи лечение, могат да включват лекарства с антиеметични, антидиарейни или антиацидни свойства.
Сериозни, понякога фатални стомашно-чревни усложнения, включително стомашно-чревна перфорация, са настъпили при пациенти с интраабдоминално злокачествено заболяване, лекувани със сунитиниб. В проучването GIST фаза 3 фатално стомашно -чревно кървене се наблюдава при 0,98% от пациентите, лекувани с плацебо.
Хипертония
Хипертонията е много честа нежелана реакция, докладвана в клиничните проучвания. Дозата на сунитиниб е намалена или временно преустановено нейното приложение при приблизително 2,7% от пациентите, при които се е появила хипертония. При никой от тези пациенти сунитиниб не е преустановен окончателно. Тежка хипертония (> 200 mmHg систоличен или 110 mmHg диастоличен) се наблюдава при 4,7% от пациентите със солидни тумори.При MRCC и преди това нелекувани пациенти, случаи на хипертония са докладвани при 33,9% от пациентите на сунитиниб в сравнение с 3,6% от пациентите на IFN-α. тежка хипертония се е появила при 12% от нелекуваните преди това пациенти в групата на сунитиниб и при по-малко от 1% от тези от групата на IFN-α. Във фаза 3 pNET проучване, хипертония е докладвана при 26,5% от пациентите, приемащи сунитиниб, в сравнение с 4,9% от пациентите в групата на плацебо. Епизодите на тежка хипертония се наблюдават при пациенти с pNET при 10%. От пациентите, лекувани със сунитиниб и 3% от тези, лекувани с плацебо.Пациентите трябва да бъдат изследвани за хипертония и да бъдат наблюдавани по подходящ начин. Препоръчва се временно спиране на лечението при пациенти с тежка неконтролирана хипертония с медикаментозно лечение. Лечението може да се възобнови, когато хипертонията е адекватно контролирана.
Хематологични нарушения
Абсолютно намаление на броя на неутрофилите от 3 и 4 степен се наблюдава при 10% и 1,7% от пациентите, включени съответно във фаза 3 GIST проучване, и при 16% и 1,6% от пациентите, включени в проучването. Фаза 3 MRCC и при 13 % и 2,4% от пациентите, включени във фаза 3 pNET проучване. Намаляване на броя на тромбоцитите от 3 и 4 степен се съобщава съответно при 3,7% и 0,4% от пациентите, включени във фаза 3 GIST проучване, при 8,2% и 1,1% от пациентите, включени във фаза 3 MRCC проучване и при 3,7% и 1,2% от пациентите, включени в проучването фаза 3 на pNETs.
Горепосочените събития не са кумулативни, като цяло са обратими и обикновено не водят до преустановяване на лечението. включително кръвоизлив, свързан с тромбоцитопения и неутропенични инфекции.
Наблюдавано е, че анемията се проявява както в ранните, така и в късните етапи на лечението със сунитиниб; Съобщавани са степени 3 и 4.
Пълна кръвна картина трябва да се извършва в началото на всеки цикъл на лечение при пациенти, получаващи сунитиниб.
Сърдечни патологии
При пациенти, лекувани със сунитиниб, са докладвани сърдечно -съдови събития, някои от които фатални, включително сърдечна недостатъчност, кардиомиопатия, миокардна исхемия и миокарден инфаркт. Тези данни показват, че сунитиниб увеличава риска от кардиомиопатия. При лекуваните пациенти не са идентифицирани специфични допълнителни рискови фактори за кардиомиопатия, причинена от сунитиниб, освен специфичния ефект на лекарството.
В клинични проучвания, намаляване на фракцията на изтласкване на лявата камера (LVEF) ≥ 20% и под долната граница на нормата се наблюдава при приблизително 2% от лекуваните със сунитиниб пациенти с GIST, 4% от пациентите с MRCC, рефрактерни на цитокини, лекувани със сунитиниб и при 2 % от пациентите с GIST, лекувани с плацебо. Тези понижения на LVEF не изглеждат прогресивни и често се подобряват при продължаване на лечението. В проучването, проведено при пациенти с MRCC и никога преди това не лекувани, 27% от пациентите, лекувани със сунитиниб и 15% от тези, лекувани с IFN-α, са имали стойност на LVEF под долната граница на нормата. За двама пациенти (
При пациенти с ГИСТ епизоди на „сърдечна недостатъчност“, „застойна сърдечна недостатъчност“ или „лявокамерна недостатъчност“ са докладвани при 1,2% от пациентите, лекувани със сунитиниб и при 1% от пациентите, лекувани с плацебо. В основното проучване във фаза 3 по GIST (n = 312), свързани с лечението фатални сърдечни реакции са настъпили при 1% от пациентите в двете проучвани групи (сунитиниб и плацебо). Във фаза 2 на проучване на пациенти с цитокин-рефрактерен MRCC 0,9 % от пациентите съобщават за фатален миокарден инфаркт, свързан с лечението, а при проучване на фаза 3 на пациенти с MRCC, които никога не са били лекувани, 0,6 % от пациентите в рамото на IFN-α и 0% от пациентите в рамото на сунитиниб съобщават за фатални сърдечни събития. Във фаза 3 pNET проучване, един пациент (1%), приемащ сунитиниб, е имал фатална сърдечна недостатъчност, свързана с лечението. Възможна връзка между инхибирането на рецептора на тирозин киназата (RTK) и сърдечната функция е неясна.
Пациентите, които са съобщили за сърдечни събития, в рамките на 12 месеца преди приложението на сунитиниб, като например миокарден инфаркт (включително тежка / нестабилна стенокардия), коронарна / периферна байпасна операция, симптоматична ХСН, цереброваскуларно събитие или преходна исхемична атака или белодробна емболия, са изключени от клинични изпитвания със сунитиниб. Не е известно дали пациентите с такива съпътстващи състояния могат да бъдат изложени на повишен риск от развитие на лекарствена дисфункция на лявата камера.
Трябва да се извършва внимателно наблюдение за клинични признаци и симптоми на застойна сърдечна недостатъчност, особено при пациенти със сърдечни рискови фактори и / или с анамнеза за коронарна артериална болест.
Лекарите се съветват да преценят този риск спрямо потенциалните ползи от лекарството. Тези пациенти трябва да бъдат внимателно наблюдавани за клинични признаци и симптоми на застойна сърдечна недостатъчност по време на лечението със сунитиниб. Изходните и периодичните оценки на фракцията на изтласкване на лявата камера също трябва да се имат предвид, когато пациентът се лекува със сунитиниб. При пациенти без сърдечни рискови фактори все още трябва да се обмисли оценка на фракцията на изтласкване на камерата на изходно ниво.
При наличие на клинични прояви на ХСН се препоръчва преустановяване на лечението със сунитиниб. Приложението на сунитиниб трябва да се прекъсне и / или да се намали дозата при пациенти без клинични данни за застойна сърдечна недостатъчност, но с намаляване на фракцията на изтласкване между 20% и 50% от изходното ниво.
Удължаване на QT интервала
Данни от предклинични проучвания (инвитро И in vivo), проведени с дози, по -високи от препоръчаните при хора, показват, че сунитиниб може да инхибира процесите на сърдечна реполяризация (напр. удължаване на QT интервала).
Увеличаването на QTc интервала до повече от 500 msec е настъпило със скорост от 0,5%, а промени от изходното ниво с повече от 60 msec са настъпили при 1,1% от 450 пациенти със солидни тумори; и двата параметъра се признават за потенциално значими вариации. При концентрации, съответстващи на приблизително два пъти терапевтични концентрации, е установено, че сунитиниб удължава QTcF интервала (коригиран съгласно формулата на Frederica).
Удължаването на QT интервала е проучено в проучване, включващо 24 пациенти, на възраст 20-87 години, с напреднали злокачествени заболявания.Резултатите от това проучване показват, че сунитиниб има ефект върху QTc интервала (дефиниран като плацебо-коригирана средна промяна> 10 msec, с горна граница от 90% CI> 15 msec) при терапевтична концентрация (ден 3), използвайки 24-часовия изходен корекционен метод, и при концентрации над терапевтичните (ден 9), като се използват двата корекционни метода в началото. Нито един пациент не е докладвал QTc стойност> 500 msec. Въпреки че е наблюдаван ефект върху QTcF интервала на 3-ия ден 24 часа след дозирането (т.е. с очакваната терапевтична плазмена концентрация след препоръчителната начална доза от 50 mg) с 24-часовия изходен корекционен метод, клиничното значение на тази находка е неясно .
Използвайки изчерпателни серийни оценки на ЕКГ, съответстващи на терапевтични експозиции или експозиции над терапевтичните, при никой от пациентите в оценените или ITT популации не е наблюдавано удължаване на „тежкия“ QTc интервал (следователно равен или по -голям от
Степен 3 на CTCAE версия 3.0).
При терапевтични плазмени концентрации средната максимална промяна в QTcF интервала (коригирана по формулата на Frederica) от изходното ниво е 9,6 msec (90% CI 15,1 msec). При терапевтични концентрации, съответстващи на приблизително два пъти терапевтичните концентрации, максималната промяна в QTcF интервала спрямо изходното ниво беше 15,4 msec (90% CI 22,4 msec).
Моксифлоксацин (400 mg), използван като положителна контрола, показва средна максимална промяна в QTcF интервала спрямо изходното ниво от 5,6 msec. Никой субект не съобщава за ефект върху QTc интервала по -голям от степен 2 (CTCAE версия 3.0).
Удължаването на QT интервала може да причини повишен риск от камерни аритмии, включително Torsade de Pointes.
Сунитиниб трябва да се използва с повишено внимание при пациенти с анамнеза за удължаване на QT интервала, при пациенти, лекувани с антиаритмици, или с лекарствени продукти, които могат да удължат QT интервала, или при пациенти със съществуващи сърдечни заболявания, брадикардия или аномалии.Едновременното приложение на сунитиниб с мощни инхибитори на CYP3A4 трябва да бъде ограничено поради възможното повишаване на плазмените концентрации на сунитиниб (вж. Точки 4.2 и 4.5).
Венозни тромбоемболични събития
Свързани с лечението венозни тромбоемболични събития са наблюдавани при приблизително 1,0% от пациентите със солидни тумори, лекувани със сунитиниб в клинични проучвания, включително проучванията GIST и MRCC.
Във фаза 3 на GIST проучване, седем пациенти (3%), получаващи сунитиниб, и нито един пациент в плацебо групата са имали венозни тромбоемболични събития; петима от седемте пациенти са имали дълбока венозна тромбоза степен 3 (DVT) и двама са имали дълбока венозна тромбоза степен 1 или 2. Четири от тези седем пациенти, лекувани за GIST, са прекратени след наблюдение на DVT.
Тринадесет пациенти (3%), лекувани със сунитиниб в проучването MRCC фаза 3 и никога преди това не лекувани, а четирима пациенти (2%) от двете цитокин-рефрактерни проучвания MRCC съобщават за венозни тромбоемболични събития. Девет от тези пациенти са имали венозни тромбоемболични събития. A " белодробна емболия, един с степен 2 и осем с степен 4. Осем от тези пациенти са имали ДВТ, един с степен 1, два с степен 2, четири с степен 3 и един с степен 4. При пациент с белодробна емболия в проучването MRCC , рефрактерни на цитокини, дозата се спира.
От нелекуваните преди това пациенти с MRCC на IFN-α, шест (2%) съобщават за венозни тромбоемболични събития, един пациент (белодробна емболия, всички степен 4.
Венозни тромбоемболични събития са докладвани за 1 (1,2%) пациент в рамото на сунитиниб и 5 (6,1%) пациенти в рамото на плацебо във фаза 3 pNET проучване. Два от тези субекти, лекувани с плацебо, съобщават за ДВТ, един от степен 2 и един от степен 3.
Не са наблюдавани случаи с фатален изход при основните проучвания на GIST, MRCC и pNET. В постмаркетинговия режим на продукта са наблюдавани случаи с фатален изход (вж. Респираторни събития и точка 4.8).
Артериални тромбоемболични събития
Съобщавани са случаи на артериални тромбоемболични събития (АТЕ), понякога фатални, при пациенти, лекувани със сунитиниб. Най -честите събития включват мозъчно -съдов инцидент, преходна исхемична атака и церебрална исхемия. Рисковите фактори, свързани с артериални тромбоемболични събития, в допълнение към съществуващото злокачествено заболяване и на възраст над 65 години, включват хипертония, захарен диабет и предишно тромбоемболично събитие.
Дихателни събития
Пациентите, които са имали „белодробна емболия през последните 12 месеца, са изключени от клиничните изпитвания със сунитиниб.
При пациенти, получаващи сунитиниб в основните проучвания фаза 3, белодробни събития (диспнея, плеврален излив, белодробна емболия или белодробен оток) са наблюдавани при приблизително 17,8% от пациентите с GIST, при приблизително 26,7% от тези с MRCC и при 12% от пациенти с pNET.
Приблизително 22,2% от пациентите със солидни тумори, включително GIST и MRCC, лекувани със сунитиниб в клинични проучвания, съобщават за белодробни събития.
Случаи на белодробна емболия са наблюдавани при приблизително 3,1% от пациентите с GIST и приблизително 1,2% от пациентите с MRCC, лекувани със сунитиниб в проучвания фаза 3 (вж. Точка 4.4. - Венозни тромбоемболични събития). Не са наблюдавани случаи на белодробна емболия при пациенти с pNET лекувани със сунитиниб в проучването фаза 3. В постмаркетинговия период са наблюдавани редки случаи с фатален изход (вж. точка 4.8).
Дисфункция на щитовидната жлеза
Препоръчва се оценка на функцията на щитовидната жлеза чрез измерване на изходните лабораторни стойности при всички пациенти. Пациентите с предшестващ хипотиреоидизъм или хипертиреоидизъм трябва да бъдат лекувани съгласно стандартната клинична практика преди започване на лечението със сунитиниб. По време на лечението със сунитиниб трябва да се извършва рутинна проверка на функцията на щитовидната жлеза на всеки 3 месеца. Освен това, всички пациенти трябва да бъдат внимателно наблюдавани по време на лечението за възможни признаци и симптоми на дисфункция на щитовидната жлеза, а пациентите, които развият някакви признаци и / или симптоми, показателни за дисфункция на щитовидната жлеза, трябва да се подложат на лабораторни изследвания на функцията на щитовидната жлеза, както се очаква клинично. Пациентите, които развият дисфункция на щитовидната жлеза, трябва да бъдат лекувани съгласно стандартната клинична практика.
Наблюдавано е хипотиреоидизъм в началото или в края на лечението със сунитиниб.
Хипотиреоидизъм е докладван като нежелана реакция при 7 пациенти (4%), получаващи сунитиниб в двете проучвания на MRCC, проведени при цитокинови огнеупорни пациенти; при 61 пациенти (16%), получаващи сунитиниб и при три пациенти (
Освен това се съобщава за повишаване на TSH при 4 пациенти (2%), лекувани от цитокин-рефрактерна MRCC. Като цяло 7% от популацията на MRCC съобщават клинични или лабораторни данни за свързан с лечението хипотиреоидизъм. Придобит хипотиреоидизъм се наблюдава при 6,2% от пациентите в проучването GIST, приемащи сунитиниб, в сравнение с 1% в групата на плацебо. Във фаза 3 pNET проучване се съобщава за хипотиреоидизъм при 6 пациенти (7,2%), получаващи сунитиниб, и при един пациент (1,2%), получаващи плацебо.
Функцията на щитовидната жлеза е проспективно проследена в две проучвания при пациенти с рак на гърдата; SUTENT не е одобрен за лечение на рак на гърдата. В едно проучване се съобщава за хипотиреоидизъм при 15 пациенти (13,6%), лекувани със сунитиниб и при 3 субекта (2,9%), лекувани със стандартна терапия.Повишен кръвен TSH е докладван при 1 субект. (0,9%), лекувани със сунитиниб и при нито един субект лекувани със стандартна терапия.Хипертиреоидизъм не е докладван при никой от пациентите, лекувани със сунитиниб и е докладван при 1 субект (1,0%), който е получил стандартна терапия.В другото проучване хипотиреоидизъм е докладван при общо 31 субекта (13%), лекувани със сунитиниб и 2 пациенти (0,8%), лекувани с капецитабин. Повишен кръвен TSH е докладван при 12 пациенти (5,0%), лекувани със сунитиниб, и при нито един пациент, лекуван с капецитабин. Хипертиреоидизъм е докладван при 4 субекта (1,7%), лекувани със сунитиниб, и при нито един пациент, лекуван с капецитабин. Намален кръвен TSH е докладван при 3 субекта (1,3%), лекувани със сунитиниб, и при нито един пациент. Лекуван с капецитабин. 2 субекта (0,8%), лекувани със сунитиниб и при 1 субект (0,4%), лекувани с капецитабин. Увеличението на Т3 е съобщено при 1 пациент (0,8%), лекуван със сунитиниб и при нито един пациент, лекуван с капецитабин.
Случаи на хипертиреоидизъм, някои последвани от хипотиреоидизъм, и случаи на тиреоидит се съобщават рядко в клинични проучвания и във фазата на пускане на пазара на продукта.
Панкреатит
Наблюдавано е повишаване на серумната липаза и амилазна активност при пациенти с няколко солидни тумора, получаващи сунитиниб. Увеличаването на активността на серумната липаза е преходно и като цяло не е свързано с признаци и симптоми на панкреатит при лица със солидни тумори от различен тип.
Нечесто се наблюдава панкреатит (
Съобщавани са случаи на сериозни панкреатични събития, някои с фатален изход.
Ако се появят симптоми на панкреатит, лечението със сунитиниб трябва да се преустанови и на пациентите да се осигури подходяща поддържаща помощ. В проучването на фаза 3 pNET не са докладвани събития, свързани с лечението на панкреатит.
Хепатотоксичност
При пациенти, лекувани със сунитиниб, е наблюдавана хепатотоксичност. Наблюдавани са случаи на чернодробна недостатъчност, понякога с фатален изход, при чернодробна функция (аланин трансаминаза [ALT], аспартат трансаминаза [AST], нива на билирубин). Признаци или симптоми на чернодробна недостатъчност, лечението със сунитиниб трябва да се преустанови и на пациентите да се осигури подходяща поддържаща медицинска помощ.
Хепатобилиарни нарушения
Лечението със сунитиниб може да бъде свързано с холецистит, включително алитичен холецистит и енфтематозен холецистит. В основни клинични проучвания честотата на холецистит е 0,5%.
В постмаркетинговия период са докладвани случаи на холецистит.
Бъбречна функция
Съобщавани са случаи на бъбречно увреждане, бъбречна недостатъчност и / или остра бъбречна недостатъчност, в някои случаи с фатален изход.
Рисковите фактори, свързани с бъбречно увреждане / недостатъчност при пациенти, получаващи сунитиниб, включват, в допълнение към вече съществуващ бъбречно-клетъчен карцином: напреднала възраст, захарен диабет, съществуващо бъбречно увреждане, сърдечна недостатъчност, хипертония, сепсис, дехидратация / хиповолемия и рабдомиолиза.
Безопасността от продължаване на лечението със сунитиниб при пациенти с умерена до тежка протеинурия не е системно оценявана.
Съобщавани са случаи на протеинурия и редки случаи на нефротичен синдром. Препоръчва се изходен анализ на урината и пациентите трябва да бъдат наблюдавани за възможно развитие или влошаване на протеинурията.
Лечението със сунитиниб трябва да се преустанови при пациенти с нефротичен синдром.
Фистули
Ако се образува фистула, лечението със сунитиниб трябва да се преустанови. Има ограничена информация за продължително лечение със сунитиниб при пациенти с фистули.
Нарушаване на процеса на зарастване на рани
Съобщавани са случаи на нарушено заздравяване на рани по време на терапията със сунитиниб. Не са провеждани официални клинични проучвания за ефекта на сунитиниб върху зарастването на рани. По предпазни причини се препоръчва временно да се прекъсне терапията със сунитиниб при пациенти, подложени на тежка операция. Клиничният опит по отношение на времето, необходимо за възобновяване на терапията след тежка операция, е ограничен. Следователно решението за възобновяване на терапията със сунитиниб след тежка операция трябва да се основава на клиничната преценка за възстановяване от операцията.
Остеонекроза на долната / долната челюст
Съобщавани са случаи на остеонекроза на челюстта при пациенти, лекувани със SUTENT. В повечето от докладваните случаи пациентите са получавали предишно или едновременно лечение с интравенозни бисфосфонати, при които остеонекрозата на челюстта е идентифициран риск.
Инвазивните стоматологични интервенции също са идентифицирани като рисков фактор. Преди лечението със SUTENT трябва да се обмисли стоматологичен преглед и подходяща превантивна стоматологична помощ. Ако е възможно, трябва да се избягват инвазивни стоматологични интервенции при пациенти, които преди това са приемали или приемат интравенозни бисфосфонати (вж. Точка 4.8).
Свръхчувствителност / ангиоедем
Ако възникне оток поради реакция на свръхчувствителност, лечението със сунитиниб трябва да се преустанови и да се приложи стандартно медицинско лечение.
Нарушения на нервната система
Нарушения на вкуса
Дисгевзия е докладвана при приблизително 28% от пациентите, получаващи сунитиниб по време на клинични изпитвания.
Конвулсии
В клинични проучвания със сунитиниб и постмаркетингови случаи са наблюдавани случаи на гърчове при лица със или без радиологични данни за мозъчни метастази. Освен това има ограничен брой съобщения (главоболие, намалена бдителност, нарушена умствена функция и загуба на зрение, включително кортикална слепота, трябва да бъдат контролирани с медицинско лечение, включително контрол на хипертонията. Препоръчва се временно спиране на сунитиниб; след отзвучаване на в този случай лечението може да бъде възобновено по преценка на лекуващия лекар.
Синдром на туморна лиза (TLS)
Случаи на синдром на туморен лизис (TLS), някои с фатален изход, рядко са наблюдавани в клинични проучвания и са докладвани след пускане на пазара при пациенти, лекувани със сунитиниб. Рисковите фактори за TLS включват висока туморна тежест, съществуваща хронична бъбречна недостатъчност, олигурия, дехидратация, хипотония и кисела урина. Тези пациенти трябва да бъдат внимателно наблюдавани и лекувани според клиничните показания; за тези пациенти трябва да се има предвид профилактична хидратация.
Инфекции
Съобщавани са случаи на сериозни инфекции, със или без неутропения, включително някои случаи с фатален изход.
Инфекциите, които най -често се наблюдават при лечение със сунитиниб, са инфекции, характерни за онкологично болните, като респираторни, пикочни пътища, кожа и сепсис.
Съобщавани са редки, понякога фатални случаи на некротизиращ фасциит, включително този на перинеума. Лечението със сунитиниб трябва да се преустанови при пациенти, при които се развие некротизиращ фасциит, и да се започне незабавно подходящо лечение.
Хипогликемия
Има съобщения за понижаване на кръвната захар по време на лечението със сунитиниб, някои от тях клинично симптоматични и изискващи хоспитализация поради загуба на съзнание. В случай на симптоматична хипогликемия, лечението със сунитиниб трябва временно да се преустанови. Нивата на кръвната захар трябва да се проверяват редовно при пациенти с диабет, за да се прецени дали дозата на лекарствата за диабет трябва да се коригира, за да се сведе до минимум рискът от хипогликемия.
04.5 Взаимодействия с други лекарствени продукти и други форми на взаимодействие
Проучвания за взаимодействия са провеждани само при възрастни.
Лекарства, които могат увеличавам плазмени концентрации на сунитиниб
При здрави доброволци едновременното прилагане на еднократна доза сунитиниб с кетоконазол, силен инхибитор на CYP3A4, води до увеличаване на комбинираните Cmax [сунитиниб + първичен метаболит] съответно с 49% и AUC0-∞ съответно с 49% и 51%.
Приложение на сунитиниб със силни инхибитори на CYP3A4 (напр. Ритонавир , итраконазол, еритромицин, кларитромицин, сок от грейпфрут) може да повиши концентрациите на сунитиниб.
Следователно трябва да се избягва комбинация с инхибитори на CYP3A4 или да се обмисли алтернативен лекарствен продукт без или с минимален потенциал за инхибиране на CYP3A4.
Ако това не е възможно, може да се наложи дозата на SUTENT да бъде намалена до минимум 37,5 mg / ден за GIST и MRCC или 25 mg / ден за pNET, въз основа на внимателно проследяване на поносимостта (вж. Точка 4.2).
Лекарства, които могат намалете плазмени концентрации на сунитиниб
При здрави доброволци едновременното приложение на единична доза сунитиниб и индуктор на CYP3A4 рифампицин води до намаляване на комбинираните [сунитиниб + първичен метаболит] Cmax и AUC0-∞ съответно с 23% и 46%.
Приложение на сунитиниб със силни индуктори на CYP3A4 (напр. Дексаметазон, фенитоин, карбамазепин, рифампицин, фенобарбитал или билкови препарати, съдържащи жълт кантарион /Hypericum perforatum) може да намали концентрациите на сунитиниб. Следователно трябва да се избягва връзката с индукторите на CYP3A4 или трябва да се обмисли алтернативен лекарствен продукт без или с минимален потенциал да индуцира CYP3A4. Ако това е невъзможно, дозата на SUTENT може да се увеличи на стъпки от 12, 5 mg до 87,5 mg / ден за GIST и MRCC или 62,5 mg / ден за pNET) въз основа на внимателно проследяване на поносимостта (вж. точка 4.2).
04.6 Бременност и кърмене
Бременност
Не са провеждани проучвания при бременни жени, получаващи сунитиниб. Проучванията при животни показват репродуктивна токсичност, включително малформации на плода (вж. Точка 5.3).
SUTENT не трябва да се използва по време на бременност или при жени, които не използват ефективни мерки за контрацепция, освен ако потенциалните ползи не оправдават потенциалния риск за плода. Ако SUTENT се използва по време на бременност или ако пациентът забременее по време на лечението със SUTENT, пациентът трябва да бъде информиран за потенциалните рискове за плода.
Жените с детероден потенциал трябва да бъдат посъветвани да използват ефективна контрацепция и да избягват забременяване, когато се лекуват със SUTENT.
Време за хранене
Сунитиниб и / или неговите метаболити се екскретират в млякото на плъхове. Не е известно дали сунитиниб или неговият основен активен метаболит се екскретира в кърмата. Тъй като активните вещества обикновено се екскретират в кърмата и като се имат предвид възможните сериозни нежелани реакции при кърмачета, жените не трябва да кърмят по време на лечението със SUTENT.
Плодовитост
Предклиничните данни показват, че фертилитетът при мъжете и жените може да бъде нарушен от лечението със сунитиниб (вж. Точка 5.3).
04.7 Ефекти върху способността за шофиране и работа с машини
Не са провеждани проучвания за ефектите върху способността за шофиране и работа с машини.Пациентите трябва да бъдат информирани за възможната поява на замаяност по време на лечението със сунитиниб.
04.8 Нежелани реакции
Обобщение на профила на безопасност
Най-сериозните нежелани реакции, свързани със лечението със сунитиниб, някои са фатални, са бъбречна недостатъчност, сърдечна недостатъчност, белодробна емболия, стомашно-чревна перфорация и кръвоизливи (напр. Дихателни, стомашно-чревни, свързани с тумори, кръвоизливи в урината и мозъка).
Най -честите нежелани реакции от всяка степен (докладвани от пациенти в ключови клинични изпитвания за RCC, GIST и pNET) включват намален апетит, нарушения на вкуса, хипертония, умора, стомашно -чревни нарушения (напр. Диария, гадене, стоматит, диспепсия и повръщане), промяна в цвета на синдрома на кожата и палмарно-плантарна еритродизестезия. Тези симптоми могат да намалят при продължаване на лечението. По време на лечението може да възникне хипотиреоидизъм. Хематологичните нарушения (напр. Неутропения, тромбоцитопения и анемия) са сред най -честите нежелани лекарствени реакции.
Смъртоносни нежелани събития, различни от изброените в точка 4.4. или в точка 4.8 и считани за евентуално свързани със сунитиниб, включват множествена органна недостатъчност, дисеминирана интраваскуларна коагулация, перитонеален кръвоизлив, надбъбречна недостатъчност, пневмоторакс, шок и внезапна смърт.
Таблица на нежеланите реакции
Нежеланите реакции, съобщени от пациенти с GIST, MRCC и pNET в обединен набор от данни от 7115 пациенти, са изброени по-долу и категоризирани по системо-органен клас, честота и тежест (NCI-CTCAE). Съобщават се и постмаркетингови нежелани реакции, установени в клинични проучвания. В рамките на всеки честотен клас се съобщават нежелани реакции в низходящ ред по тежест.
Честотите са дефинирани, както следва: много чести (≥1 / 10), чести (≥1 / 100a
Таблица 1 - Нежелани реакции, съобщени в клинични проучвания
Следните термини са групирани:
назофарингит и орален херпес
b Бронхит, инфекция на долните дихателни пътища, пневмония и инфекция на дихателните пътища
c Абсцес, абсцес на крайниците, анален абсцес, абсцес на венците, абсцес на черния дроб, абсцес на панкреаса, перинеален абсцес, периректален абсцес, ректален абсцес, подкожен абсцес и зъбен абсцес
d Езофагеална кандидоза и орална кандидоза
и целулит и кожна инфекция
f Сепсис и септичен шок
g Абдомен абсцес, коремен сепсис, дивертикулит и остеомиелит
h Намален апетит и анорексия
i Дисгевзия, агеузия и промяна на вкуса
j Остър коронарен синдром, стенокардия, нестабилна стенокардия, запушване на коронарната артерия, миокардна исхемия
k Намаляване / аномалия на фракцията на изтласкване
l Остър миокарден инфаркт, миокарден инфаркт, безшумен миокарден инфаркт
m Орофарингеална и фаринголарингеална болка
n Стоматит и афтозен стоматит
o Болки в корема, болки в долната и горната част на корема
p Стомашно -чревна и чревна перфорация
q Холецистит и алитен холецистит
r Жълта кожа, обезцветяване на кожата и нарушения на пигментацията
s Псориазиформен дерматит, ексфолиативен обрив, обрив, еритематозен обрив, фоликуларен обрив, генерализиран обрив, макулен обрив, макуло-папулозен обрив, папулен обрив и сърбящ обрив
t Кожна реакция и кожна патология
u Патология на ноктите и обезцветяване на ноктите
v Умора и астения
w Оток на лицето, оток и периферен оток
x Амилаза и повишена амилаза
* Включва фатални събития
Описание на идентифицираните нежелани реакции
Инфекции и инвазии: Съобщавани са случаи на сериозни инфекции (със или без неутропения), включително случаи с фатален изход. Съобщавани са случаи на некротизиращ фасциит, понякога фатален, който също може да засегне перинеума (вж. Също точка 4.4).
Нарушения на кръвта и лимфната система: Съобщавани са случаи на тромботична микроангиопатия. В тези случаи се препоръчва временно спиране на SUTENT; след разрешаване на тези събития, лечението може да бъде възобновено по преценка на лекуващия лекар.
Нарушения на имунната система: Съобщавани са реакции на свръхчувствителност, включително ангиоедем.
Нарушения на нервната система: Съобщавани са няколко случая, някои фатални, при пациенти с гърчове и рентгенологични данни за обратим синдром на задната левкоенцефалопатия (RPLS) (вж. Също точка 4.4).
Нарушения на метаболизма и храненето: Съобщава се за по -висока честота на хипогликемични събития при пациенти с pNET в сравнение с пациенти с MRCC и GIST. Въпреки това, много от нежеланите събития, наблюдавани в клиничните изпитвания, не се считат за свързани с изследваното лечение.
Хепатобилиарни нарушения: Съобщава се за чернодробна дисфункция и може да включва аномалии на чернодробните функционални тестове, хепатит или чернодробна недостатъчност.
Нарушения на кожата и подкожната тъкан: Съобщавани са случаи на гангренозна пиодермия, обикновено обратими след преустановяване на лечението (вж. Също точка 4.4).
Нарушения на опорно -двигателния апарат и съединителната тъкан: Съобщавани са случаи на миопатия и / или рабдомиолиза, някои свързани с остра бъбречна недостатъчност. Пациентите с признаци или симптоми на мускулна токсичност трябва да бъдат лекувани в съответствие със стандартната медицинска практика.
Съобщавани са случаи на образуване на фистула, понякога свързани с туморна некроза и регресия, в някои случаи с фатален изход.
Съобщавани са случаи на остеонекроза на челюстта при пациенти, лекувани със SUTENT, много от които настъпват при пациенти, които са разпознали рискови фактори за остеонекроза на челюстта, особено експозиция на интравенозни бисфосфонати и / или анамнеза за зъбни заболявания, изискващи инвазивни стоматологични интервенции (вж. също раздел 4.4).
Докладване на предполагаеми нежелани реакции
Съобщаването на предполагаеми нежелани реакции, настъпили след разрешаване на лекарствения продукт, е важно, тъй като позволява непрекъснато проследяване на съотношението полза / риск на лекарствения продукт. От медицинските специалисти се изисква да съобщават всички предполагаеми нежелани реакции чрез националната система за докладване в „приложение V .
04.9 Предозиране
Няма специфичен антидот за предозиране със сунитиниб и лечението на предозирането трябва да включва общи поддържащи мерки. тези случаи настъпилите нежелани реакции са в съответствие с известния профил на безопасност на сунитиниб.
05.0 ФАРМАКОЛОГИЧНИ СВОЙСТВА
05.1 Фармакодинамични свойства
Фармакотерапевтична група: антинеопластични средства, инхибитори на протеин киназата.
ATC код: LO1XE04.
Механизъм на действие
Сунитиниб инхибира множество рецептори на тирозин киназа (RTK), които участват в растежа на тумора, туморната неоангиогенеза и метастатичната прогресия на рака. Сунитиниб е идентифициран като инхибитор на рецепторите на растежен фактор, получени от тромбоцити (PDGFRα и PDGFRβ), рецептори на съдовия ендотелен растежен фактор (VEGFR1, VEGFR2 и VEGFR3), рецептор на стволови клетки (KIT), рецептор на тирозин киназа на FLT3 (Подобно на Fms тирозин киназа 3), CSF-1R рецептора (рецептор на колония стимулиращ фактор (CSF-1R)) и рецептора на неутрофичен фактор, получен от глиал (RET). Основният метаболит показва активност, сравнима с тази на сунитиниб при биохимични и клетъчни тестове.
Клинична ефикасност и безопасност
Безопасността и клиничната ефикасност на сунитиниб са проучени при лечението на пациенти с GIST, резистентни към иматиниб (т.е. тези пациенти, които са прогресирали по време или след лечението с иматиниб) или с непоносимост към иматиниб (т.е. тези, които са имали значителна токсичност по време на лечението с иматиниб което предотвратява продължаването на лечението), при лечението на пациенти с MRCC и при лечението на пациенти с неоперабилен pNET.
Ефикасността се основава на време до прогресия на тумора и увеличаване на преживяемостта при пациенти с GIST, преживяемост без прогресия и обективна реакция при пациенти, които преди това не са били лекувани с MRCC и MRCC, рефрактерни към терапията с MRCC, съответно. Цитокини, и на преживяемост без прогресия при пациенти с pNET.
Стромални тумори на стомашно -чревния тракт (GIST)
Първоначално отворено ескалиращо проучване е проведено при пациенти с GIST след неуспех на иматиниб (средна максимална дневна доза 800 mg) поради резистентност или непоносимост. Записани са 97 пациенти с различни дозировки и режими на дозиране; 55 пациенти са лекувани със SUTENT 50 mg съгласно препоръчителния 4-седмичен лекарствен и двуседмичен график за отнемане на лекарството (график 4/2).
В това проучване средното време до прогресия TTP е 34.0 седмици (95% CI = 22.0-46.0 седмици).
Рандомизирано, двойно-сляпо, плацебо-контролирано проучване от фаза 3 на сунитиниб е проведено при пациенти с GIST, които са имали непоносимост или са имали прогресия на заболяването по време или след лечение с иматиниб (средна максимална дневна доза 800 mg). В това проучване 312 пациенти (2: 1) са рандомизирани да бъдат лекувани с 50 mg сунитиниб или плацебо, перорално веднъж дневно според схемата 4/2 до прогресия на заболяването или оттегляне от проучването по „друга причина (207 пациенти са получили сунитиниб и 105 плацебо).
Първичната крайна точка на ефикасността на проучването е TTP, определена като времето от рандомизацията до първото документиране на обективната прогресия на тумора. ), когато е оценен от изследователя, и 27,3 седмици (95% CI = 16,0-32,1 седмици), когато е оценен от Комитета за независим преглед и е статистически по-добър от 5,1-седмичния TTP, получен с плацебо (95% CI = 4,4-10,1 седмици, стр
Независима комисия за преглед. Разликата в общата преживяемост е статистически в полза на сунитиниб [коефициент на опасност: 0,491 95% (CI 0,290-0,831)]; рискът от смърт е 2 пъти по -висок при пациентите на плацебо групата, отколкото при тези на рамото на сунитиниб.
След междинния анализ на ефикасността и безопасността, по препоръка на независимия DSMB, проучването е заслепено и на пациентите в плацебо групата е предложено да преминат към открито лечение със сунитиниб.
Общо 255 пациенти са били лекувани със сунитиниб във фазата на открито лечение на проучването, включително 99 пациенти, първоначално лекувани с плацебо.
Анализът на първичните и вторичните крайни точки в откритата фаза на проучването потвърди резултатите, получени по време на междинния анализ, както е показано в таблицата по-долу.
Таблица 2 - Обобщение на крайните точки за ефикасност (ITT популация)
Средната обща преживяемост (ОС) в ITT популацията е съответно 72.7 седмици и 64.9 седмици (HR 0.876, 95% CI 0.679 - 1.129, р = 0.306) в рамото на лечение със сунитиниб и плацебо. В този анализ плацебо групата включва тези пациенти, рандомизирани на плацебо и впоследствие преминали към открито лечение със сунитиниб.
Метастатичен бъбречно -клетъчен карцином (MRCC) при нелекувани преди това пациенти
Проведено е рандомизирано, многоцентрово, международно проучване от фаза 3, за да се оцени ефикасността и безопасността на сунитиниб в сравнение с интерферон IFN-α при нелекувани преди това пациенти с MRCC. Седемстотин и петдесет пациенти бяха рандомизирани 1: 1 в групите за лечение; повтарящи се 6-седмични цикли. Всеки цикъл се състои от 4 седмици с 50 mg на ден перорално, последвани от 2 седмици без приемане на лекарството (схема 4/2) или с IFN-α, приложен през устата подкожно в доза от 3 милиона единици (MU ) първата седмица, 6 MU през втората седмица и от третата седмица нататък в доза от 9 MU според лечение от 3 последователни дни всяка седмица.
Средната продължителност на лечението е 11,1 месеца (диапазон: 0,4 - 46,1) за лечение със сунитиниб и 4,1 месеца (диапазон 0,1 - 45,6) за лечение с IFN -α. Тежки нежелани събития, свързани с лечението (TRSAEs), са докладвани при 23,7% от пациентите, получаващи сунитиниб, и 6,9% от пациентите, получаващи IFN-α. Въпреки това, процентът на прекратяване поради нежелани събития е 20% за сунитиниб и 23% за IFN-α. Прекратяването на лечението е настъпило при 202 пациенти (54%) в групата на сунитиниб и 141 пациенти (39%) в групата на IFN-α.
Намаляването на дозата се наблюдава при 194 пациенти (52%), лекувани със сунитиниб и 98 пациенти (27%), лекувани с IFN-α. Пациентите са били лекувани до прогресиране на заболяването или оттегляне от проучването. Първичната крайна точка за ефикасност е преживяемостта без прогресия (PFS).
Планиран междинен анализ показа статистически значимо предимство за SUTENT пред IFN-α. В това проучване средната PFS за групата на сунитиниб е 47,3 седмици в сравнение с 22,0 седмици за групата IFN-α; коефициентът на опасност е 0,415 (95% CI: 0,320-0,539, р-стойност
Лечението със сунитиниб е свързано с по-дълга преживяемост от лечението с IFN-α. Средната обща преживяемост е 114,6 седмици за рамото на сунитиниб (95% ДИ: 100,1 - 142,9 седмици) и 94,9 седмици за рамото на IFN -α (95% ДИ: 77,7 - 117,0 седмици) с коефициент на опасност от 0,821 (95% CI: 0,673-1,001; р = 0,0510 въз основа на нестратифициран логаритмичен тест).
Преживяемостта без прогресия (PFS) и общата преживяемост (OS), наблюдавани при намерението да се лекува (ITT) популация и определени чрез радиологична лабораторна оценка, са обобщени в следните таблици:
Обобщение на крайните точки за ефикасност (ITT популация)
Цитокин-огнеупорен метастатичен бъбречно-клетъчен карцином (MRCC)
Проведено е проучване фаза 2 със SUTENT при пациенти, неподатливи на предишна цитокинова терапия, лекувани с интерлевкин-2 или IFN-α. 63 пациенти са получавали перорална начална доза от 50 mg сунитиниб веднъж дневно в продължение на 4 последователни седмици, последвана от 2-седмичен период на почивка за завършване на пълен 6-седмичен курс (схема на лечение 4/2). Основната крайна точка за ефикасност е обективният процент на отговор (Обективен
Процент на отговор (ORR)) според критериите RECIST (Критерии за оценка на отговора при солидни тумори).
В това проучване обективният процент на отговор е 36,5% (95% CI 24,7% -49,6%), а средното време до прогресия (TTP) е 37,7 седмици (95% CI 24,0-46,4 седмици).
Открито, едноцентрово, многоцентрово, потвърждаващо проучване за оценка на ефикасността и безопасността на сунитиниб е проведено при пациенти с MRCC, рефрактерни на предишна цитокинова терапия. Сто и шест пациенти са получили поне една доза от 50 сунитиниб. Mg в рамката на схемата 4/2.
Първичната крайна точка за ефикасност на това проучване е процентът на ORR.Вторичните крайни точки включват TTP, продължителността на отговора (DR) и общата преживяемост (OS).
В това проучване ORR е 35,8% (95% CI 26,8% -47,5%). DR и средната OS все още не бяха достигнати.
Невроендокринни тумори на панкреаса (pNET)
Отворено, многоцентрово, подкрепящо проучване фаза 2 оценява ефикасността и безопасността на монотерапията със сунитиниб при 50 mg дневни дози по схема 4/2 [4 седмици лечение, 2 седмици почивка] при пациенти с неработещ pNET В кохорта от 66 пациенти с рак на островковите клетки на панкреаса, крайната точка на първичен отговор е 17%.
Проведено е основна фаза 3, многоцентрово, международно, рандомизирано, двойно-сляпо, плацебо-контролирано проучване на монотерапия със сунитиниб при пациенти с неоперабилен pNET.
Пациентите, които трябваше да са документирали прогресия на заболяването въз основа на RECIST в рамките на предходните 12 месеца, бяха рандомизирани (1: 1) да получават 37,5 mg сунитиниб веднъж дневно без планиран период на отнемане (n = 86) или плацебо (n = 85) .
Първичната крайна точка беше оценката на преживяемостта без прогресия (PFS) при пациенти, приемащи сунитиниб спрямо тези, получаващи плацебо. Други крайни точки бяха OS, процент на ORR, докладвани от пациентите резултати) и безопасност.
От гледна точка на демографските характеристики, групите пациенти, лекувани със сунитиниб и плацебо, са сравними. В допълнение, 49% от пациентите, лекувани със сунитиниб и 52% от пациентите, получаващи плацебо, са имали нефункциониращи тумори, а 92% от пациентите в двете ръце са имали чернодробни метастази. Проучването позволява използването на аналози на соматостатин. 66% от пациентите, лекувани със сунитиниб и 72% от пациентите, лекувани с плацебо, преди това са били лекувани със системна терапия. Освен това 24% от пациентите в групата на сунитиниб и 22% от пациентите в плацебо група е получавала соматостатинови аналози. Клинично значимо предимство на сунитиниб PFS в сравнение с плацебо е наблюдавано при оценката на изследователя. Средната PFS е била 11,4 месеца в рамото на сунитиниб в сравнение с 5, 5 месеца в рамото на плацебо [съотношение на опасност: 0,418 (95% CI 0,263 , 0.662), р-стойност = 0.0001]; подобни резултати бяха наблюдавани, когато бяха използвани оценки на туморния отговор, базирани на приложението на RECIST за измервания на тумора, извършени от изследователите, за да се определи прогресията на заболяването, както е показано в Таблица 3. А коефициент на опасност в полза на сунитиниб се наблюдава във всички подгрупи, оценени за изходни характеристики, включително анализ по брой предишни системни терапии. Общо 29 пациенти в рамото на сунитиниб и 24 в групата на плацебо не са получавали предходни системни терапии; при тези пациенти там "коефициент на опасност за PFS е 0,365 (95% CI 0,156, 0,857), р = 0,0156.
По подобен начин сред 57 пациенти в рамото на сунитиниб (включително 28 с 1 предходна системна терапия и 29 с 2 или повече системни терапии) и 61 пациенти в рамото на плацебо (включително 25 с 1 предходна системна терапия и 36 с 2 или повече системни терапии ) l "коефициент на опасност за PFS беше 0.456 (95% CI 0.264, 0.787), р = 0.0036.
Анализ на чувствителността на PFS е извършен, когато PFS се основава на измерванията на тумора от изследователя и когато всички субекти, цензурирани по причини, различни от прекратяването на проучването, се считат за PFS събития. Този анализ даде консервативна оценка на ефекта от лечението със сунитиниб и потвърди първичния анализ, демонстрирайки "коефициент на опасност 0,507 (95% CI 0,350, 0,733), р = 0,000193. Основното проучване при панкреатична NET е прекратено преждевременно въз основа на препоръката на независим Комитет за оценка на лекарствата, а основната крайна точка се основава на оценката на изследователя: и двете състояния може да са повлияли на оценката на ефекта от лечението.
За да се изключи пристрастието в оценката на изследователите на PFS, беше извършен независим, заслепен централен преглед на диагностичните образи; този преглед подкрепя оценката на изследователя, както е показано в таблица 3.
Таблица 3 - Резултати от ефикасността от фаза 3 pNET проучване
CI = доверителен интервал, HR = Коефициент на опасност, NA = Неприложимо, NR = не е достигнато
двустранен не-стратифициран тест с ранг на лог
b Точен тест на Fisher
Общата цифра на преживяемост не е била зряла, когато е извършен анализът. Има 9 смъртни случая в рамото със сунитиниб и 21 смъртни случая в рамото на плацебо. Наблюдава се статистически значима разлика в обективния процент на отговор на сунитиниб в сравнение с плацебо.
В случаите на прогресия на заболяването, пациентите бяха информирани за лечението, което получават, а на пациентите, приемащи плацебо, беше предложена възможността да бъдат включени в различно открито удължено проучване със сунитиниб. Поради ранното приключване на проучването, останалите пациенти бяха информирани за лечението, което получават, и им беше предложен достъп до открито удължено проучване със сунитиниб. Общо 59 пациенти в плацебо групата бяха лекувани със сунитиниб в проучването. на удължаване.
Резултатите от въпросника за качеството на живот на Европейската организация за изследване и лечение на рак (EORTC QLQ-C30) показаха, че общото свързано със здравето качество на живот и петте функционални области (физическа, ролева, когнитивна, емоционална и социални) са запазени при пациенти, получаващи сунитиниб, в сравнение с тези, получаващи плацебо, с малко симптоматични странични ефекти.
Педиатрична популация
Европейската агенция по лекарствата е отложила задължението да представи резултатите от проучванията със SUTENT в една или повече подгрупи от педиатричната популация за лечение на GISTs (вж. Точка 4.2 за информация относно педиатричната употреба).
Европейската агенция по лекарствата се отказа от задължението да представи резултатите от проучванията със SUTENT във всички подгрупи на педиатричната популация за лечение на бъбречни и бъбречни тазови карциноми (с изключение на нефробластома, нефробластоматоза, саркома прозрачна клетка, мезобластна нефрома, бъбречна медулария карцином и рабдоиден тумор на бъбрека) (вж. точка 4.2 за информация относно педиатричната употреба).
Европейската агенция по лекарствата се отказа от задължението да представи резултатите от проучванията със SUTENT във всички подгрупи на педиатричната популация за лечение на гастроентеропанкреатични невроендокринни тумори (с изключение на невробластома, невроганглиобластома, феохромоцитома) (вж. Точка 4.2 за информация относно педиатричната употреба) ).
05.2 "Фармакокинетични свойства
Фармакокинетиката на сунитиниб е оценена при 135 здрави доброволци и при 266 пациенти със солидни тумори. Фармакокинетиката е сходна при всички тествани популации пациенти със солиден тумор и при здрави доброволци.
В рамките на схемите на дозиране от 25-100 mg, площта под кривата (AUC) и Cmax се увеличават пропорционално на дозата. При многократно ежедневно приложение сунитиниб се натрупва 3-4 пъти, а основният активен метаболит се натрупва 7-10 пъти. Стационарни концентрации на сунитиниб и неговия основен активен метаболит се постигат в рамките на 10-14 дни. До 14 ден комбинираните плазмени концентрации на сунитиниб и неговия основен активен метаболит са 62.9 - 101 ng / mL и представляват прогнозни целеви концентрации въз основа на предклинични данни за инхибиране на рецепторното фосфорилиране. инвитро и да доведат до намаляване на туморния застой / растеж in vivo.
Основният активен метаболит съставлява 23-37% от общата експозиция на лекарството. Не се наблюдават значителни промени във фармакокинетиката на сунитиниб или на основния активен метаболит при многократни курсове веднъж дневно или повторно при тестваните режими на дозиране.
Абсорбция
След перорално приложение на сунитиниб, пикови концентрации (Cmax) обикновено се наблюдават в рамките на 6-12 часа (Tmax) от приема на лекарството.
Храната няма ефект върху бионаличността на сунитиниб.
Разпределение
Свързването на сунитиниб и неговия основен активен метаболит с човешки плазмени протеини в тестовете в vitro те бяха съответно 95% и 90%, без „видима зависимост от концентрацията.
Привидният обем на разпределение (Vd) на сунитиниб е голям - 2,230 l - което показва разпределение в тъканите.
Метаболитни взаимодействия
Изчислените Ki стойности инвитро за всички изследвани изоформи на цитохром (CYP) (CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4 / 5 и CYP4A9 / 11) показва, че е малко вероятно сунитиниб и неговият основен клинично активен метаболит да е a метаболизма на други активни вещества, които могат да се метаболизират от тези ензими.
Биотрансформация
Сунитиниб се метаболизира предимно от CYP3A4, изоформата на цитохром Р450, който произвежда неговия основен активен метаболит, десетил сунитиниб, който допълнително се метаболизира от същия изоензим.
Едновременното приложение на сунитиниб и силни индуктори или инхибитори на CYP3A4 трябва да се избягва, тъй като плазмените нива на сунитиниб могат да се променят (вж. Точки 4.4 и 4.5).
Елиминиране
Екскрецията се осъществява главно чрез изпражнения (61%) и бъбречното елиминиране на непромененото активно вещество и неговите метаболити представлява 16% от приложената доза. Сунитиниб и неговият основен активен метаболит са основните съединения, идентифицирани в плазмата, урината и изпражненията и представляват съответно 91,5%, 86,4%и 73,8%от радиоактивността, открита в събраните проби. Малки метаболити са идентифицирани в урината и изпражненията, но обикновено не се откриват в плазмата. Общият орален клирънс (CL / F) е 34-62 L / h.
След перорално приложение при здрави доброволци, елиминационният полуживот на сунитиниб и неговия основен активен метаболит десетил е приблизително 40-60 часа и 80-110 часа съответно.
Специални популации
Чернодробно увреждане: Сунитиниб и неговият основен метаболит се метаболизират предимно от черния дроб. Системната експозиция след еднократна доза сунитиниб е сходна при лица с леко или умерено чернодробно увреждане (стадии А и В по Child-Pugh) в сравнение с лица с нормална чернодробна функция. SUTENT не е проучен при пациенти с тежко чернодробно увреждане (стадий С по Child-Pugh).
Проучванията за рак изключват пациенти с ALT или AST> 2.5 x ULN (горна граница на нормата) или ако тези стойности са> 5.0 x ULN поради чернодробни метастази.
Бъбречна недостатъчност: Популационните фармакокинетични анализи показват, че видимият клирънс на сунитиниб (CL / F) не е повлиян от креатининовия клирънс в разглеждания диапазон (42-347 ml / min). Системните експозиции след една единична доза сунитиниб са сходни при пациенти с тежко бъбречно увреждане ( CLcr80 ml / min). Въпреки че сунитиниб и неговият основен метаболит не се изчистват чрез хемодиализа при пациенти с ESRD, общата системна експозиция е 47% по -ниска за сунитиниб и 31% за неговия основен метаболит в сравнение с лица с нормална бъбречна функция.
Тегло, състояние на изпълнение: Фармакокинетичните анализи на населението показват, че не са необходими корекции на началната доза за теглото и състоянието на Източна кооперативна онкологична група (ECOG).
Пол на принадлежност: Наличните данни показват, че женските могат да имат 30% по -нисък видим клирънс на сунитиниб (CL / F) от мъжете; тази разлика обаче не изисква корекции на началната доза.
05.3 Предклинични данни за безопасност
Проучванията за токсичност при многократни дози при плъхове и маймуни с продължителност до 9 месеца показват, че основните ефекти върху целевите органи са в стомашно -чревния тракт (повръщане и диария при маймуни); надбъбречните жлези (задръстване на кората и / или кръвоизлив при плъхове и маймуни, с некроза, последвана от фиброза при плъхове); кръвта и лимфната система (хипоцелуларност на костния мозък и лимфоидно изчерпване на тимуса, далака и лимфните възли); екзокринният панкреас (дегранулация на ацинарни клетки с единична клетъчна некроза); слюнчените жлези (ацинарна хипертрофия); костни стави (удебеляване на растежната плоча); матката (атрофия) и яйчниците (намаляване на развитието на фоликулите). Всички резултати са настъпили с клинично значими нива на плазмена експозиция на сунитиниб. Други ефекти, наблюдавани в проучванията, включват: удължаване на QTc интервала, намаляване на фракцията на изтласкване на лявата камера (LVEF) и тестисите тубуларна атрофия, увеличени мезангиални клетки в бъбреците, кръвоизлив в стомашно -чревния тракт и лигавицата на устната кухина и хипертрофия на клетките на предната част на хипофизата. ендометриума) и плочата на костния растеж (удебеляване на епифиза или дисплазия на хрущяла) са свързани с фармакологичното действие на сунитиниб. Повечето от тези събития са обратими след преустановяване на лечението за 2-6 седмици.
Генотоксичност
Генотоксичният потенциал на сунитиниб е оценен in vitro и in vivo. Сунитиниб не показва мутагенен ефект върху бактериите, използвайки метаболитното активиране, осигурено от черния дроб на плъхове. Сунитиниб не индуцира структурни хромозомни аберации в човешки периферни лимфоцити инвитро. Полиплоидия (аберации в броя на хромозомите) е наблюдавана в човешки периферни лимфоцити в vitro, както в присъствието, така и в отсъствието на метаболитно активиране. Сунитиниб не показва кластогенен потенциал в костния мозък на плъх in vivo. Основният активен метаболит не е оценен за генотоксичен потенциал.
Канцерогенност
В едномесечното проучване за установяване на диапазона на дозите (0, 10, 25, 75 или 200 mg / kg / ден), в който rasH2 трансгенни мишки са хранени с перорална сонда чрез дозиране дневно и непрекъснато дозата, когато се прилага, при са наблюдавани най -високите дози (200 mg / kg / ден) карцином и хиперплазия на жлезите на Brunner на дванадесетопръстника.
Проведено е 6-месечно проучване за оценка на канцерогенността при rasH2 трансгенни мишки, хранени с перорална епруветка чрез дозиране на приложената доза дневно (0, 8, 25, 75 [намалена до 50] mg / kg / ден). При дози ≥25 mg / kg / ден, прилагани в продължение на 1 или 6 месеца (≥7,3 пъти над AUC, наблюдавана при пациенти, получаващи препоръчителната дневна доза [RDD]), се наблюдават гастродуоденални карциноми, повишена честота на фона. стомашната лигавица.
В 2-годишно проучване за оценка на канцерогенността при плъхове (0, 0,33, 1 или 3 mg / kg / ден), когато сунитиниб се прилага в 28-дневни цикли, последвани от 7-дневни периоди без приложение, е установено увеличение на честотата на феохромоцитом и медуларна хиперплазия на надбъбречната жлеза при мъжки плъхове, които са получавали доза от 3 mg / kg / ден в продължение на повече от 1 година (≥ 7,8 пъти AUC при пациенти, получаващи RDD).Карциномът на жлезата на Brunner се появява в дванадесетопръстника при дози ≥ 1 mg / kg / ден при жени, при дози от 3 mg / kg / ден при мъже и лигавичната клетъчна хиперплазия се забелязва в стомашните жлези при равни дози. При 3 mg / kg / ден при мъже; тези събития са настъпили съответно при дози от 0,9, 7,8 и 7,8 пъти от AUC при пациенти, получаващи RDD. Значението на тези неопластични находки, наблюдавани при проучвания за канцерогенност на мишки (rasH2) и плъхове за хора, лекувани със сунитиниб, е несигурно.
Репродуктивна токсичност и токсичност за развитието
При проучвания за репродуктивна токсичност не са наблюдавани ефекти върху фертилитета при мъже или жени. Проучванията за токсичност при многократни дози, проведени при плъхове и маймуни, показват ефекти върху фертилитета при жените под формата на фоликуларна атрезия, дегенерация на жълтото тяло, ендометриални промени в матката и намаляване на теглото на матката и яйчниците до нива на клинично значими системна експозиция. Наблюдавани са ефекти върху фертилитета при мъжки плъхове под формата на тубуларна атрофия в тестисите, намалени сперматозоиди в епидидимиса и колоидно изчерпване в простатата и семенните мехурчета при нива на плазмена експозиция 25 пъти над системната експозиция при хора.
При плъхове ембрионално-феталната смъртност е довела до значително намаляване на броя на живите плодове, увеличен брой резорбции, увеличени загуби след имплантацията и обща загуба на потомство при 8 от 28 бременни женски при нива на плазмена експозиция 5,5 пъти над системната експозиция при хора . При зайци намаляването на теглото на бременната матка и броя на живите плодове са причинени от увеличаването на феталната резорбция, загубите след имплантацията и общите загуби на потомството при 4 от 6 бременни женски при 3-кратни нива на плазмена експозиция. Системна експозиция при хората. Лечението със сунитиниб при плъхове по време на органогенезата води до ефекти върху развитието при дози ≥ 5 mg / kg / ден, състоящи се от повишена честота на скелетни малформации на плода, характеризиращи се главно със забавено осификация на гръдните / лумбалните прешлени и възникващи при нива на плазмена експозиция 5.5 пъти човешката системна експозиция. При зайци ефектите върху развитието се състоят от повишена честота на цепнатина на устната при нива на плазмената експозиция, приблизително равни на тези, наблюдавани в клиниката, и цепнатина на устната и цепнатината на небцето при нива на плазмена експозиция 2,7 пъти от системната експозиция при хора.
Ефектите на сунитиниб (0,3; 1,0; 3,0 mg / kg / ден) върху пре- и постнаталното развитие са оценени в проучване при бременни женски плъхове. Повишаването на телесното тегло на майката по време на бременност и лактация е намалено при дози> 1 mg / kg / ден, но не се наблюдава репродуктивна токсичност при майката до дози от 3 mg / kg / ден (прогнозна експозиция> 2, 3 пъти AUC, установена при пациенти получаване на RDD). Намалено тегло на потомството се наблюдава при дози от 3 mg / kg / ден в периода преди и след отбиването. Не се наблюдава токсичност за развитието при дози от 1 mg / kg / ден (експозиция приблизително ≥0,9 пъти AUC, наблюдавана при пациенти, получаващи RDD).
06.0 ФАРМАЦЕВТИЧНА ИНФОРМАЦИЯ
06.1 Помощни вещества
Съдържание на капсулата
Манитол (E421)
Натриева кроскармелоза
Повидон (K-25)
Магнезиев стеарат
Черупка на капсулата
Желе
Червен железен оксид (E172)
Титанов диоксид (E171)
Мастило
Шеллак
Пропиленгликол
Натриев хидроксид
Повидон
Титанов диоксид (E171)
06.2 Несъвместимост
Не е от значение.
06.3 Срок на валидност
3 години.
06.4 Специални условия на съхранение
Този лекарствен продукт не изисква специални условия за съхранение.
06.5 Естество на непосредствената опаковка и съдържанието на опаковката
Бутилки от полиетилен с висока плътност (HDPE), с полипропиленово затваряне, съдържащи 30 твърди капсули.
Прозрачни поли (хлоротрифлуороетилен) / PVC блистери с перфорирани единични дози и с алуминиево фолио с лак за термоуплътняване, съдържащ 28 х 1 твърди капсули.
Не всички опаковки могат да бъдат пуснати на пазара.
06.6 Инструкции за употреба и боравене
Няма специални инструкции.
07.0 Притежател на разрешението за търговия
Пфайзер ООД
Рамсгейт Роуд
Сандвич, Кент CT13 9NJ
Великобритания
08.0 НОМЕР НА РАЗРЕШЕНИЕТО ЗА ПОТРЕБЕНИЕ
EU/1/06/347/001
037192022
EU/1/06/347/004
09.0 ДАТА НА ПЪРВО РАЗРЕШЕНИЕ ИЛИ ПОДНОВЯВАНЕ НА РАЗРЕШЕНИЕТО
Дата на първо разрешаване: 19 юли 2006 г.
Дата на последното подновяване: 09 януари 2012 г.
10.0 ДАТА НА ПРЕГЛЕД НА ТЕКСТА
11.0 ЗА РАДИОЛЕКАТИ, ПЪЛНИ ДАННИ ЗА ВЪТРЕШНАТА ДОЗИМЕТРИЯ НА РАДИАЦИЯТА
12.0 ЗА РАДИОЛЕКАТИ, ДОПЪЛНИТЕЛНИ ПОДРОБНИ ИНСТРУКЦИИ ЗА ПЪРВИЧНА ПОДГОТОВКА И КОНТРОЛ НА КАЧЕСТВОТО