Редактирано от д -р Джовани Чета
ECM обикновено се описва като съставен от няколко големи класа биомолекули:
- Структурни протеини (колаген и еластин)
- Специализирани протеини (фибрилин, фибронектин, ламинин и др.)
- Протеогликани (агрегани, синдекани) и глузаминогликани (хиалуронани, хондроитин сулфати, хепаран сулфати и др.)
Структурни протеини
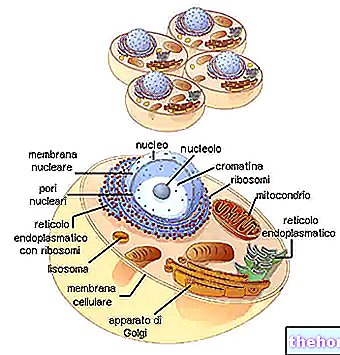
Колагените образуват най -представеното семейство гликопротеини в животинското царство. Те са най -присъстващите протеини в извънклетъчния матрикс (но не и най -важният) и са основните съставки на собствените съединителни тъкани (хрущяли, кости, фасции, сухожилия, връзки).
Има най -малко 16 различни вида колаген, от които типове I, II и III са най -присъстващи на нивото на типичните фибрили (тип IV образува един вид ретикулум, който представлява основния компонент на базалните ламини).
Колагените се синтезират предимно от фибробласти, но епителните клетки също са в състояние да ги синтезират.
Колагеновите влакна непрекъснато взаимодействат с огромно количество други молекули от извънклетъчния матрикс, съставлявайки биологичен континуум, основополагащ за живота на клетката. Свързаните колагени във фибрилите играят преобладаваща роля при образуването и поддържането на структури, способни да устоят на силите на напрежение, е почти нееластичен (глюкозамингликаните изпълняват действие на устойчивост на компресия). По някакъв начин колагенът се произвежда и метаболизира отново в зависимост от механичното натоварване и неговите виско-еластични свойства включват, както ще видим в параграф „Вискоеластичност на фасцията ", голямо влияние върху стойката на човека. Като допълнителна демонстрация на способността на колагена да се променя според влиянието на околната среда, приемайки напр. с различна степен на твърдост, еластичност и устойчивост, има колагени, дефинирани с термина FACIT (Fibril Associated Collagen with Interrupt Triple спирали), способни да функционират функционално като протеогликани (описани в параграф „Глюкозаминогликани и протеогликани“).
Колагеновите влакна, благодарение на покритието си от PG / GAG (протеогликани / глюкозаминогликани) притежават свойства на биосензори и биопроводници: относителните електрически заряди водят до по -голяма способност да свързват вода и обмен на йони, следователно и по -голям електрически капацитет.
Знаем, че всяка механична сила, способна да генерира структурна деформация, натоварва междумолекулните връзки, произвеждайки лек електрически поток, т.е. пиезоелектрически ток (Атенщад, 1969). В такива случаи колагеновите влакна разпределят положителните заряди върху изпъкналата си повърхност и отрицателните върху вдлъбнатата, като по този начин се трансформират в полупроводници (те позволяват потока на електрони по тяхната еднопосочна повърхност). Тъй като пиезоелектричната енергия (както и пироелектричната енергия, генерирана от термични напрежения) се неутрализира от циркулиращите йони за много кратко време (приблизително 10-7-10-9 секунди), подреждането на PG / GAG върху сигнала е от решаващо значение за разпространението на сигналната повърхност на фибрилите, като например да действа като "повторители" на електрическия импулс. По -специално, надлъжна периодичност от прибл. 64 nm (което под оптичния микроскоп изглежда като ивица) позволява скорост на разпространение на импулса, равна на около 64 m / s (съответстваща на скоростта на проводимост на бързите нервни влакна) - Rengling, 2001. Силният диполярен момент на колагеновите фибрили и техният резонансен капацитет (свойство, общо за всички пептидни структури), както и ниската диелектрична константа на MEC, улесняват предаването на електромагнитни сигнали. Следователно триизмерната и повсеместна колагенова мрежа също притежава особената характеристика за провеждане на биоелектрични сигнали в трите измерения на пространството, базирани на относителното подреждане между колагенови фибрили и клетки, в аферентна посока (от ECM към клетките) или, обратно, еферентно.
Всичко това представлява MEC-клетъчна комуникационна система в реално време и такива електромагнитни биосигнали могат да доведат до важни биохимични промени, например в костите, остеокластите не могат да „смилат“ пиезоелектрично заредена кост (Oschman, 2000).
И накрая, трябва да се подчертае, че не е изненадващо, че клетката произвежда непрекъснато и със значителен разход на енергия (приблизително 70%) материал, който задължително трябва да бъде изхвърлен, най -вече чрез изключително съхранение на протоколаген (биологичен прекурсор на колаген) в специфични везикули (Albergati, 2004).
По -голямата част от гръбначните тъкани изискват едновременно наличие на две жизненоважни характеристики: здравина и еластичност. Истинска мрежа от еластични влакна, разположена вътре в ECM на тези тъкани, позволява да се върнете към първоначалните условия след силни издърпвания.Еластичните влакна са в състояние да увеличат разтегливостта на орган или част от него с поне пет пъти. Дълги, нееластични колагенови влакна са разпръснати между еластичните влакна с прецизна задача да ограничат "прекомерната деформация, дължаща се на сцеплението на тъканите. L"еластин представлява основният компонент на еластичните влакна. Това е изключително хидрофобен протеин, с дължина около 750 аминокиселини, тъй като колагенът е богат на пролин и глицин, но за разлика от колагена, той не е гликиран и съдържа много остатъци от хидроксипролин, а не хидроксилизин. Еластинът се появява като истинска биохимична мрежа с неправилна триизмерна форма, съставена от влакна и ламели, които проникват в ECM на всички съединителни тъкани.Намира се в особено голямо количество в кръвоносните съдове с еластични характеристики (това е протеинът на ECM повече присъства в артериите и представлява повече от 50% от общото сухо тегло на аортата), в лигаментите, в белите дробове и в кожата. В дермата, противно на това, което се случва с колагена, плътността и обемът на еластин са склонни да се увеличават с течение на времето, но старият еластин обикновено изглежда подут, почти подут, често с фрагментиран вид и с намаляване на компонента. "Аморфен" (Pasquali Rochetti et al, 2004). Гладкомускулните клетки и фибробластите са основните производители на неговия предшественик, тропоеластин, секретиран в извънклетъчните пространства.
Други статии на тема „Колаген и еластин, колагенови влакна в извънклетъчния матрикс“
- Извънклетъчен матрикс
- Фибронектин, глюкозаминогликани и протеогликани
- Значението на извънклетъчния матрикс в клетъчното равновесие
- Промени в извънклетъчния матрикс и патологии
- Съединителна тъкан и извънклетъчен матрикс
- Дълбока фасция - съединителна тъкан
- Фасциални механорецептори и миофибробласти
- Биомеханика на дълбоките фасции
- Поза и динамичен баланс
- Тенсегрити и спираловидни движения
- Долни крайници и движение на тялото
- Поддръжка на седалището и стоматогнатичен апарат
- Клинични случаи, промени в позата
- Клинични случаи, стойка
- Постурална оценка - клиничен случай
- Библиография - От извънклетъчната матрица до стойката. Дали свързващата система е нашият истински Deus ex machina?