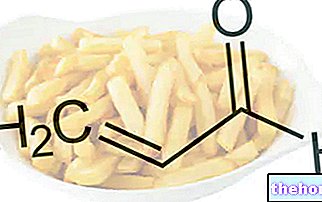
на калций и неорганични киселини, като например азотна киселина, солна киселина или сярна киселина. По -долу е химическата реакция, която включва използването на последната киселина:
Ca3 (PO4) 2 + 3 H2SO4 → 3 CaSO4 + 2 H3PO4
Термичният процес, от друга страна, включва получаване на фосфорен анхидрид, започвайки от елементарен фосфор. След като се образува, анхидридът трябва да се хидратира, докато се получи ортофосфорна киселина, както е показано в следната реакция:
P2O5 + 3 H2O → 2 H3PO4
Този последен процес обикновено води до по -чиста ортофосфорна киселина от мокрия процес.
околната среда, тя изглежда като бяло твърдо вещество, което се топи при температура от около 42 ° C.
Въпреки това, фосфорната киселина обикновено се продава под формата на концентриран 85% воден разтвор. Това е безцветен, без мирис и нелетлив разтвор, но корозивен и с доста плътна, почти "сиропирана" консистенция.
Освен че е разтворима във вода, ортофосфорната киселина е разтворима и в етанол. Тя не е нито експлозивна, нито запалима, но поради корозивността си върху кожата и лигавиците, с нея обаче трябва да се работи много внимателно.
за да се подобри адхезията на циментиращите материали за капсули, мостове, фасети, пломби и др. В този контекст, ортофосфорната киселина обикновено се използва в 37% разтвори.