Активни съставки: Тенофовир дизопроксил
Viread 33 mg / g гранули
Предлагат се опаковъчни вложки Viread за размери на опаковките:- Viread 123 mg филмирани таблетки
- Viread 163 mg филмирани таблетки
- Viread 204 mg филмирани таблетки
- Viread 245 mg филмирани таблетки
- Viread 33 mg / g гранули
Показания Защо се използва Viread? За какво е?
Viread съдържа активното вещество тенофовир дизопроксил. Това активно вещество е антиретровирусно или антивирусно лекарство, което се използва за лечение на HIV инфекция. Виреад за лечение на HIV инфекция винаги трябва да се използва в комбинация с други лекарства.
Viread 33 mg / g гранули е лечение за инфекция с ХИВ (вирус на човешкия имунодефицит). Той е показан за:
- възрастни
- деца и юноши на възраст от 2 до по -малко от 18 години, които вече са били лекувани с други лекарства срещу ХИВ, които вече не са напълно ефективни поради развитието на резистентност или са причинили странични ефекти
Viread 33 mg / g гранули е също лечение за хроничен хепатит В, инфекция с HBV (вирус на хепатит В). Той е показан за:
- възрастни
- юноши на възраст от 12 до под 18 години
Не трябва да имате HIV инфекция, за да се лекувате с Viread за HBV.
Това лекарство не е лек за HIV инфекция. Все още можете да получите инфекции или други заболявания, свързани с HIV инфекция, докато приемате Viread. Можете също да предадете ХИВ или HBV на други, така че е важно да вземете предпазни мерки, за да избегнете заразяване на други хора.
Противопоказания Когато Viread не трябва да се използва
Не приемайте Viread
- Ако сте алергични към тенофовир, тенофовир дизопроксил фумарат или към някоя от останалите съставки на това лекарство, изброени в точка 6.
Ако това се отнася за Вас, незабавно уведомете Вашия лекар и не приемайте Viread.
Предпазни мерки при употреба Какво трябва да знаете, преди да приемете Viread
Говорете с Вашия лекар или фармацевт, преди да приемете Viread.
- Внимавайте да не предадете инфекцията на други хора. Все още можете да предадете ХИВ, докато приемате това лекарство, въпреки че рискът се намалява от ефекта на антиретровирусната терапия. Обсъдете с Вашия лекар необходимите предпазни мерки, за да избегнете предаването на това лекарство. Инфекция към други хора. Viread не намалява риска от предаване на HBV на други хора чрез сексуален контакт или заразяване с кръв. Трябва да продължите да предприемате предпазни мерки, за да избегнете това.
- Уведомете Вашия лекар или фармацевт, ако сте имали бъбречно заболяване или ако тестовете са показали бъбречни проблеми. Viread не трябва да се дава на подрастващи, които вече имат бъбречни проблеми. Преди да започнете лечението, Вашият лекар може да назначи кръвни изследвания, за да оцени бъбречната Ви функция. Viread може да повлияе на бъбреците по време на лечението. Вашият лекар може да назначи кръвни изследвания по време на лечението, за да следи как работят бъбреците Ви. Бъбреци. Ако сте възрастен, Вашият лекар може да Ви посъветва да приемате таблетките по -рядко.Не намалявайте предписаната доза, освен ако Вашият лекар не Ви каже.
Viread не трябва да се приема с други лекарства, които могат да увредят бъбреците Ви (вижте Други лекарства и Viread). Ако това е неизбежно, лекарят ще следи бъбречната функция на бебето веднъж седмично.
- Костни проблеми. Някои възрастни пациенти с ХИВ, приемащи комбинирана антиретровирусна терапия, могат да развият костно заболяване, наречено остеонекроза (смърт на костната тъкан, причинена от липса на кръвоснабдяване на костите). Продължителността на комбинираната антиретровирусна терапия, употребата на кортикостероиди, консумацията на алкохол, тежка имуносупресия, по -висок индекс на телесна маса, наред с други, може да бъде част от многобройните рискови фактори за развитието на това заболяване. Признаци на остеонекроза са сковаността на ставите, болките (особено в бедрата, коленете и раменете) и затрудненото движение. Свържете се с Вашия лекар, ако забележите някой от тези симптоми.
Костни проблеми (понякога водещи до фрактури) също могат да възникнат поради увреждане на тубуларните клетки на бъбреците (вж. Точка 4, Възможни странични ефекти).
- Уведомете Вашия лекар, ако някога сте имали чернодробни проблеми, включително хепатит.Пациентите с чернодробни проблеми, включително хроничен хепатит В или С, които се лекуват с антиретровирусни лекарства, имат по-висок риск от сериозни и животозастрашаващи чернодробни усложнения. Ако имате хепатит В, Вашият лекар внимателно ще прецени най -добрия режим на лечение за Вас. Ако сте имали чернодробно заболяване или хроничен хепатит В, Вашият лекар може да Ви назначи кръвни изследвания за проследяване на чернодробната Ви функция.
- Внимавайте за инфекции. Ако имате напреднал ХИВ (СПИН) и имате „инфекция, може да развиете симптоми на„ инфекция и възпаление или влошаване на симптомите на съществуваща инфекция, когато започнете лечение с Viread. Тези симптоми може да показват, че имунната система на вашето тяло е борба с инфекцията. Проверете за признаци на възпаление или инфекция веднага след като започнете да приемате Viread. Ако забележите признаци на възпаление или инфекция, незабавно уведомете Вашия лекар.
В допълнение към опортюнистичните инфекции, автоимунни нарушения (състояние, което възниква, когато имунната система атакува здравата телесна тъкан) могат да възникнат и след като започнете да приемате лекарства за лечение на HIV инфекция. Автоимунни нарушения могат да възникнат много месеци след започване на лечението. Ако забележите някакви симптоми на инфекция или други симптоми като мускулна слабост, първоначална слабост в ръцете и краката, които се издигат до тялото на тялото, сърцебиене, тремор или хиперактивност, моля информирайте незабавно Вашият лекар да поиска необходимото лечение.
- Уведомете Вашия лекар или фармацевт, ако сте над 65 години. Viread не е проучен при пациенти на възраст над 65 години. Ако сте над тази възраст и Ви е предписан Viread, Вашият лекар ще Ви наблюдава отблизо.
Деца и юноши
Гранули Viread 33 mg / g са показани само за:
- ХИВ-1 инфектирани деца и юноши на възраст от 2 до по-малко от 18 години, които вече са били лекувани с други лекарства срещу ХИВ, които вече не са напълно ефективни поради развитието на резистентност или които са причинили нежелани ефекти
- юноши на възраст от 12 до под 18 години, заразени с HBV
Гранули Viread 33 mg / g не са подходящи за следните категории:
- не е показан при HIV -инфектирани деца под 2 -годишна възраст
- не е показан при деца под 12 години, заразени с HBV (вирус на хепатит В)
За дозировката вижте точка 3, Как да приемате Viread.
Взаимодействия Кои лекарства или храни могат да променят ефекта на Viread
Уведомете Вашия лекар или фармацевт, ако приемате, наскоро сте приемали или е възможно да приемете други лекарства.
- Когато започвате Viread, не спирайте приема на антивирусни лекарства, предписани от Вашия лекар, ако имате както HBV, така и HIV инфекция.
- Не трябва да приемате Viread, ако вече приемате други лекарства, съдържащи тенофовир дизопроксил фумарат или тенофовир алафенамид. Не приемайте Viread с лекарства, съдържащи адефовир дипивоксил (лекарство, използвано за лечение на хроничен хепатит В).
- Особено важно е да уведомите Вашия лекар, ако приемате други лекарства, които могат да увредят бъбреците Ви. Те включват:
- аминогликозиди, пентамидин или ванкомицин (за бактериална инфекция)
- амфотерицин В (за гъбична инфекция)
- фоскарнет, ганцикловир или цидофовир (за вирусна инфекция)
- интерлевкин-2 (за лечение на рак)
- адефовир дипивоксил (за HBV)
- такролимус (за потискане на имунната система)
- нестероидни противовъзпалителни средства (НСПВС, използвани за облекчаване на болки в костите или мускулите)
- Други лекарства, които съдържат диданозин (за HIV инфекция): Приемът на Viread с други антивирусни лекарства, които съдържат диданозин, може да повиши нивата на диданозин в кръвта и да намали броя на CD4 клетките. Когато лекарства, съдържащи тенофовир дизопроксил фумарат и диданозин, се приемат заедно, има има редки съобщения за възпаление на панкреаса и лактатна ацидоза (излишък на млечна киселина в кръвта), което понякога води до смърт. Вашият лекар ще трябва внимателно да прецени дали да Ви лекува с тенофовир и диданозин в комбинация.
- Също така е важно да уведомите Вашия лекар, ако приемате ледипасвир / софосбувир за лечение на инфекция с „хепатит С“.
Viread с храна и напитки
Гранулите Viread трябва да се смесват с малко мека храна, която не трябва да се дъвче (напр. Кисело мляко, ябълково пюре, бебешка храна) .Ако се дъвче, сместа, съдържаща гранулите, има силно горчив вкус.
Предупреждения Важно е да знаете, че:
Бременност и кърмене
Ако сте бременна или кърмите, мислите, че може да сте бременна или планирате бременност, посъветвайте се с Вашия лекар или фармацевт, преди да приемете това лекарство.
- Не трябва да приемате Viread по време на бременност, освен ако не е специално обсъдено с Вашия лекар. Въпреки че има ограничени клинични данни за употребата на Viread при бременни жени, той обикновено не се използва, освен ако не е строго необходимо.
- Опитайте се да избегнете забременяване, докато се лекувате с Viread. Трябва да използвате ефективна контрацепция, за да избегнете бременност.
- Ако знаете, че сте бременна или планирате да забременеете, попитайте Вашия лекар за потенциалните ползи и рискове от антиретровирусната терапия за Вас и бебето.
- Ако вече сте приемали Viread по време на бременността, Вашият лекар може редовно да изисква кръвни изследвания и други диагностични тестове, за да следи развитието на бебето. При деца, чиито майки са приемали НИОТ по време на бременност, ползата от защитата срещу ХИВ надвишава риска от странични ефекти.
- Не кърмете, докато се лекувате с Viread. Причината е, че активната съставка на това лекарство се екскретира в кърмата.
- Ако сте жена, заразена с HIV или HBV, се препоръчва да не кърмите, за да избегнете предаването на вирусите на бебето чрез мляко.
Шофиране и работа с машини
Viread може да причини замаяност. Ако се чувствате замаяни, докато приемате Viread, не шофирайте, не карайте колело и не използвайте никакви инструменти или машини.
Гранулите Viread съдържат манитол
Манитолът може да има леко слабително действие.
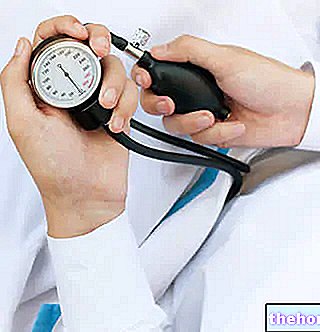
Доза, метод и време на приложение Как да използвате Viread: Дозировка
- Винаги приемайте това лекарство точно както Ви е казал Вашият лекар или фармацевт. Ако се съмнявате, консултирайте се с Вашия лекар или фармацевт.
Препоръчителната доза е:
- Възрастни и юноши на възраст от 12 до под 18 години, с тегло най -малко 35 kg: 245 mg, еквивалентно на 7,5 лъжички гранули, веднъж дневно.
- Деца на възраст от 2 до под 12 години: дневната доза при деца зависи от телесното тегло. Вашият лекар ще определи правилната доза гранули Viread въз основа на теглото на Вашето дете.
Гранулите Viread трябва да се дозират с предоставената мерителна чаша:
Всяка мерителна лъжица за ниво доставя 1 g гранули, които съдържат 33 mg тенофовир дизопроксил (като фумарат).
- Напълнете мерителната чаша до ръба.
- Използвайте острието на чист нож, за да изгладите излишния гранулат.
- За ½ лъжичка:
- Напълнете мерителната чаша до марката "½" отстрани.
- Изсипете правилния брой равни лъжички гранулат в купа.
- Гранулите трябва да се смесват с мека храна, която не трябва да се дъвче, например кисело мляко, ябълково пюре, бебешка храна. Една равнина лъжичка гранули трябва да се смеси с една супена лъжица (15 мл) мека храна. Не смесвайте гранулите с течни вещества.
- Гранулите, смесени с храната, трябва да се поглъщат незабавно.
- Всеки път трябва да се вземе цялата приготвена смес.
- Винаги приемайте препоръчаната от Вашия лекар доза. Това се прави, за да се гарантира, че лекарствата са напълно ефективни и да се намали рискът от развитие на резистентност към лечението. Не променяйте дозата си, освен ако Вашият лекар не Ви каже.
- Ако сте възрастен и имате бъбречни проблеми, Вашият лекар може да Ви предпише намаляване на дневната доза гранули.
- Ако имате HBV, Вашият лекар може да Ви предложи тест за ХИВ, за да провери дали имате и HBV, и ХИВ.
Консултирайте се в листовката на другите антиретровирусни препарати за насоки относно приема на тези лекарства.
и забрави да вземеш Viread
Важно е да не пропуснете доза Viread. Ако сте забравили една доза, изчислете колко време е минало, след като сте я пропуснали.
- Ако са минали по -малко от 12 часа, откакто обикновено го приемате, вземете го възможно най -скоро и след това вземете следващата си доза в обичайното време.
- Ако са минали повече от 12 часа от обичайната Ви доза, не приемайте забравената доза. Изчакайте и приемайте редовно следващата доза. Не вземайте двойна доза, за да компенсирате пропуснатата таблетка.
Ако се почувствате зле в рамките на 1 час след приема на Viread, вземете друга таблетка. Не трябва да приемате друга „таблетка, ако сте повръщали повече от един“ час след приема на Viread.
Ако спрете приема на Viread
Не спирайте приема на Viread без да се консултирате с Вашия лекар.Спирането на Viread може да намали ефективността на предписаната от Вашия лекар терапия.
Ако имате хепатит В инфекция или ХИВ и хепатит В заедно (коинфекция), особено важно е да не спирате лечението с Viread, без първо да се свържете с Вашия лекар. Viread. Може да се наложи да повторите кръвните изследвания няколко месеца след спиране на лечението. При пациенти с напреднало чернодробно заболяване или цироза не се препоръчва преустановяване на лечението, тъй като това може да доведе до влошаване на хепатита при някои пациенти.
- Говорете с Вашия лекар, преди да „спрете“ Viread по някаква причина, особено ако сте имали страничен ефект или ако имате друго заболяване.
- Докладвайте незабавно на Вашия лекар всички нови или необичайни симптоми, наблюдавани след спиране на лечението, особено симптоми, които обикновено са свързани с инфекция с хепатит В.
- Свържете се с Вашия лекар, преди да рестартирате гранули Viread.
Ако имате някакви допълнителни въпроси относно употребата на това лекарство, попитайте Вашия лекар или фармацевт.
Предозиране Какво да направите, ако сте приели твърде много Viread
Ако случайно сте приели твърде много Viread, можете да увеличите риска от развитие на възможни нежелани реакции при това лекарство (вижте точка 4, Възможни нежелани реакции). Свържете се с Вашия лекар или най -близкия център за спешна помощ. Вземете бутилката с гранули със себе си, за да можете лесно да опишете какво сте взели.
Странични ефекти Какви са страничните ефекти на Viread
По време на лечението с ХИВ може да има повишаване на теглото и нивата на липидите и глюкозата в кръвта.Това е отчасти свързано с възстановяването на здравето и начина на живот, а в случай на липиди в кръвта, понякога същите лекарства срещу ХИВ. Лекарят ще провери детето за тези промени.
Както всички лекарства, това лекарство може да предизвика нежелани реакции, въпреки че не всеки ги получава.
Възможни сериозни нежелани реакции: Незабавно уведомете Вашия лекар
- Лактатната ацидоза (излишъкът на млечна киселина в кръвта) е рядък (може да засегне до 1 на 1 000 души), но сериозен страничен ефект, който може да бъде фатален. Следните нежелани реакции могат да бъдат признаци на лактатна ацидоза:
- дълбоко и бързо дишане
- сънливост
- гадене, повръщане и болки в стомаха
Ако смятате, че детето ви има лактатна ацидоза, незабавно се свържете с Вашия лекар.
Други възможни сериозни странични ефекти
Следните нежелани реакции са необичайни (засягат до 1 на всеки 100 лекувани пациенти):
- болка в корема (корема), причинена от възпаление на панкреаса
- увреждане на определени клетки в бъбреците (тубуларни клетки)
Следните нежелани реакции са редки (засягат до 1 на всеки 1000 лекувани пациенти):
- бъбречно възпаление, обилна урина и жажда
- промени в урината и болки в гърба, причинени от бъбречни проблеми, включително бъбречна недостатъчност
- омекотяване на костите (с болки в костите и понякога счупвания), което може да възникне от увреждане на бъбречните тубуларни клетки
- мастен черен дроб
Ако смятате, че детето Ви има някоя от тези сериозни нежелани реакции, моля, свържете се с Вашия лекар.
По -чести странични ефекти
Следните нежелани реакции са много чести (възникват при най -малко 10 на всеки 100 лекувани пациенти):
- диария, повръщане, гадене, замаяност, обрив, чувство на слабост
Лабораторните тестове също показаха:
- намаляване на фосфатите в кръвта
Други възможни странични ефекти
Следните нежелани реакции са чести (засягат до 10 на всеки 100 лекувани пациенти):
- чревни газове
Лабораторните тестове също показаха:
- проблеми с черния дроб
Следните нежелани реакции са необичайни (засягат до 1 на всеки 100 лекувани пациенти):
- мускулен срив, мускулна болка или мускулна слабост
Лабораторните тестове също показаха:
- намаляване на калия в кръвта
- повишаване на креатинина в кръвта
- проблеми с панкреаса
Разрушаване на мускулите, омекотяване на костите (с болки в костите и понякога счупвания), мускулни болки, мускулна слабост и намален калий или фосфат в кръвта могат да възникнат от увреждане на клетките на бъбречните тубули.
Следните нежелани реакции са редки (засягат до 1 на всеки 1000 лекувани пациенти):
- болка в корема (корема), причинена от възпаление на черния дроб
- подуване на лицето, устните, езика или гърлото
Докладване на странични ефекти
Ако получите някакви нежелани реакции, говорете с Вашия лекар или фармацевт.Това включва всички възможни нежелани реакции, които не са изброени в тази листовка. Можете също да съобщите нежелани реакции директно чрез националната система за докладване, изброена в допълнение V. Чрез съобщаване на странични ефекти можете да помогнете да предоставите повече информация за безопасността на това лекарство.
Срок на годност и задържане
Съхранявайте това лекарство на място, недостъпно за деца.
Не използвайте това лекарство след срока на годност, отбелязан върху бутилката и картонената опаковка след {EXP}. Срокът на годност се отнася до последния ден от този месец.
Да не се съхранява над 25 ° C.
Не изхвърляйте никакви лекарства през отпадъчни води или битови отпадъци. Попитайте Вашия фармацевт как да изхвърлите лекарства, които вече не използвате. Това ще помогне за опазването на околната среда.
Друга информация
Какво съдържа Viread
- Активното вещество е тенофовир. Един грам гранули Viread съдържа 33 mg тенофовир дизопроксил (като фумарат).
- Другите съставки са етилцелулоза (E462), хидроксипропилцелулоза (E463), манитол (E421) и силициев диоксид (E551). Вижте точка 2 "Гранули Viread съдържа манитол".
Как изглежда Viread и какво съдържа опаковката
Това лекарство се състои от бели покрити гранули. Гранулите се доставят в бутилка, съдържаща 60 g гранули, с мерителна чаша, доставена с опаковката.
Източник на листовката: AIFA (Италианска агенция по лекарствата). Съдържание, публикувано през януари 2016 г. Наличната информация може да не е актуална.
За да имате достъп до най-актуалната версия, препоръчително е да получите достъп до уебсайта на AIFA (Италианска агенция по лекарствата). Отказ от отговорност и полезна информация.
01.0 ИМЕ НА ЛЕКАРСТВЕНИЯ ПРОДУКТ
VIREAD 33 MG / G ГРАНУЛИ
02.0 КАЧЕСТВЕН И КОЛИЧЕСТВЕН СЪСТАВ
Всяка лъжичка доставя един грам гранули, който съдържа 33 mg тенофовир дизопроксил (като фумарат).
Помощно вещество с известни ефекти: един грам гранули съдържа 622 mg манитол.
За пълния списък на помощните вещества вижте точка 6.1.
03.0 ЛЕКАРСТВЕНА ФОРМА
Гранулиран.
Бял покрит гранулат, с маскиран вкус.
04.0 КЛИНИЧНА ИНФОРМАЦИЯ
04.1 Терапевтични показания
HIV-1 инфекция
Viread 33 mg / g гранули е показан, в комбинация с други антиретровирусни лекарствени продукти, за лечение на педиатрични пациенти на възраст от 2 до
Viread 33 mg / g гранули е показан и в комбинация с други антиретровирусни лекарствени продукти при възрастни, инфектирани с HIV-1, за които твърдата фармацевтична форма не е подходяща.
При възрастни доказателствата в полза на Viread при инфекция с HIV-1 се основават на резултатите от проучване при нелекувани пациенти, което включва пациенти с висок вирусен товар (> 100 000 копия / ml) и проучвания, в които Viread е бил добавено към оптимизирана фонова терапия (предимно тройна терапия) при пациенти, лекувани преди това с антиретровирусни лекарствени продукти, които са показали недостатъчен ранен вирусологичен отговор (
Изборът да се използва Viread за лечение на HIV-1 инфектирани пациенти с предишен опит с антиретровирусно лечение трябва да се основава на резултатите от индивидуални тестове за вирусна резистентност и / или предишни терапии.
Хепатит В инфекция
Гранули Viread 33 mg / g са показани за лечение на хроничен хепатит В при възрастни, за които твърда лекарствена форма не е подходяща, с:
• компенсирано чернодробно заболяване, с данни за активна вирусна репликация, постоянно повишени нива на серумната аланин аминотрансфераза (ALT) и хистологични данни за активно възпаление и / или фиброза (вж. Точка 5.1)
• данни за резистентен към ламивудин вирус на хепатит В (вж. Точки 4.8 и 5.1).
• декомпенсирано чернодробно заболяване (вж. Точки 4.4, 4.8 и 5.1).
Viread 33 mg / g гранули е показан и при лечение на хроничен хепатит В при юноши на възраст от 12 до
• компенсирано чернодробно заболяване и доказателства за активно имунно заболяване, т.е. активна вирусна репликация, постоянно повишен серумен ALT и хистологични данни за активно възпаление и / или фиброза (вж. Точки 4.4, 4.8 и 5.1).
04.2 Дозировка и начин на приложение
Терапията трябва да се започне от лекар с опит в областта на лечението на HIV инфекцията и / или в лечението на хроничен хепатит В.
Дозировка
ХИВ-1: Препоръчителната доза е 6,5 mg тенофовир дизопроксил (като фумарат) на килограм телесно тегло веднъж дневно, приемано с храна. Вижте Таблица 1.
Налични са ограничени клинични данни относно дозата от 6,5 mg / kg гранули. & EGRAVE; следователно е необходимо внимателно да се следи ефикасността и безопасността на тази доза.
Таблица 1: Дозировка за педиатрични пациенти на възраст от 2 до
Viread се предлага и под формата на 123 mg, 163 mg и 204 mg филмирани таблетки за инфектирани с HIV-1 педиатрични пациенти на възраст от 6 до
Viread се предлага и под формата на 245 mg филмирани таблетки за лечение на HIV-1 инфекция и хроничен хепатит В при юноши на възраст 12 години и с тегло ≥ 35 kg.
Възрастни и юноши на възраст 12 години и препоръчителната доза Viread за лечение на HIV инфекция или за лечение на хроничен хепатит В е 245 mg, еквивалентно на 7,5 лъжички гранули, веднъж дневно, приемани през устата с храна.
Viread се предлага и под формата на 245 mg филмирани таблетки за лечение на HIV-1 инфекция и хроничен хепатит В при възрастни.
Хроничен хепатит В: оптималната продължителност на лечението е неизвестна. Прекратяването на лечението може да се обмисли в следните случаи:
• При HBeAg позитивни пациенти без цироза, лечението трябва да се провежда най-малко 6-12 месеца след потвърждаване на HBe сероконверсия (загуба на HBeAg и HBV ДНК с анти-HBe) или до сероконверсия на HBs или в случай на загуба на ефикасност (вж. Параграф 4.4). Серумните нива на ALT и HBV ДНК трябва да се проследяват редовно след прекратяване на лечението за късни вирусологични рецидиви.
• При пациенти с отрицателен HBeAg без цироза, лечението трябва да се извършва поне до сероконверсия на HBs или докато има данни за загуба на ефикасност. При продължително лечение над 2 години се препоръчва редовната оценка на целесъобразността на избраната терапия.
Пропусната доза
Ако пациентът пропусне доза Viread в рамките на 12 часа от обичайното време, той трябва да приеме Viread възможно най -скоро с храна и да продължи с обичайната схема на дозиране. Ако пациентът пропусне доза Viread за повече от 12 часа и почти е време за следващата доза, не трябва да приемате пропуснатата доза и просто да продължите с обичайната си схема на дозиране.
Ако пациентът повръща в рамките на 1 час след приема на Viread, той трябва да приеме друга доза. Ако пациентът повръща повече от 1 час след приема на Viread, не е необходимо да приема друга доза.
Специални популации
По-стари хора
Няма налични данни, на които да се основава препоръчителната доза за пациенти на възраст над 65 години (вж. Точка 4.4).
Бъбречна недостатъчност
Тенофовир се елиминира чрез бъбречна екскреция и експозицията на тенофовир се увеличава при пациенти с бъбречна дисфункция.
Възрастни
Данни за безопасност и ефикасност на тенофовир дизопроксил фумарат при възрастни пациенти с умерено и тежко бъбречно увреждане (креатининов клирънс, креатининов клирънс между 50 и 80 ml / min). Следователно тенофовир дизопроксил фумарат трябва да се използва само при възрастни пациенти с бъбречни проблеми, ако се счита, че потенциалните ползи от лечението надвишават потенциалните рискове. Корекции на дозата на тенофовир дизопроксил (като фумарат) 33 mg / g гранули се препоръчват при пациенти с креатининов клирънс
Леко бъбречно увреждане (креатининов клирънс между 50 и 80 mL / min)
Малко данни от клинични проучвания подкрепят прилагането на доза веднъж дневно от 245 mg тенофовир дизопроксил (като фумарат), еквивалентна на 7,5 лъжички гранули, при пациенти с леко бъбречно увреждане.
Дневни корекции на дозата на тенофовир дизопроксил (като фумарат) 33 mg / g гранули се препоръчват при пациенти с умерено (креатининов клирънс между 30 и 49 ml / min) или тежко бъбречно увреждане (фармакокинетичен креатининов клирънс при еднократна доза при HIV отрицателни лица и при Инфектирани с HBV субекти с различна степен на бъбречно увреждане, включително в краен стадий на бъбречно заболяване, изискващо хемодиализа. Тези данни за фармакокинетично моделиране не са потвърдени от клинични проучвания. Следователно клиничният отговор към лечението и бъбречната функция трябва да бъдат внимателно проследявани при тези пациенти (вж. 4.4 и 5.2).
Умерено бъбречно увреждане (креатининов клирънс между 30 и 49 ml / min)
Препоръчва се да се прилагат 132 mg (4 лъжички) тенофовир дизопроксил (като фумарат) 33 mg / g гранули веднъж дневно.
Тежко бъбречно увреждане (креатининов клирънс
За пациенти с креатининов клирънс от 20-29 ml / min: веднъж дневно се препоръчва прилагане на 65 mg (2 лъжички) тенофовир дизопроксил (като фумарат) 33 mg / g гранули.
За пациенти с креатининов клирънс 10-19 ml / min: препоръчват се 33 mg (1 лъжичка) тенофовир дизопроксил (като фумарат) 33 mg / g гранули веднъж дневно.
Пациенти на хемодиализа: 16,5 mg (0,5 лъжички) тенофовир дизопроксил (като фумарат) 33 mg / g гранули могат да се прилагат след приключване на всяка 4-часова сесия на хемодиализа.
Тези корекции на дозата не са потвърдени в клинични проучвания. Следователно, клиничният отговор към лечението и бъбречната функция трябва да се следят внимателно (вж. Точки 4.4 и 5.2).
Не могат да се направят препоръки за дозиране при пациенти, които не са на хемодиализа с креатининов клирънс
Педиатрични пациенти
Употребата на тенофовир дизопроксил фумарат не се препоръчва при педиатрични пациенти с бъбречно увреждане (вж. Точка 4.4).
Чернодробно увреждане
Не се налага коригиране на дозата при пациенти с чернодробно увреждане (вж. Точки 4.4 и 5.2).
Ако терапията с Viread е преустановена при пациенти с хроничен хепатит В със или без ХИВ коинфекция, такива пациенти трябва да бъдат наблюдавани внимателно за обостряне на хепатит (вж. Точка 4.4).
Педиатрична популация
Безопасността и ефикасността на тенофовир дизопроксил фумарат при HIV-1 инфектирани деца под 2 години не са установени. Няма налични данни.
Безопасността и ефикасността на тенофовир дизопроксил фумарат при деца с хроничен хепатит В на възраст от 2 до
Начин на приложение
Гранулите Viread трябва да се дозират с предоставената мерителна чаша. Едно ниво лъжичка доставя 1 g гранули, които съдържат 33 mg тенофовир дизопроксил (като фумарат). Гранулите Viread трябва да се смесват в контейнер с мека храна, която не е необходимо да се дъвче, например кисело мляко, ябълково пюре, бебешка храна. Една равнина лъжичка гранули трябва да се смеси с една супена лъжица (15 мл) мека храна. Сместа трябва да се поглъща незабавно и изцяло. Гранулите Viread не трябва да се смесват с течни вещества.
Viread трябва да се приема веднъж дневно, перорално, с храна.
04.3 Противопоказания
Свръхчувствителност към активното вещество или към някое от помощните вещества, изброени в точка 6.1.
04.4 Специални предупреждения и подходящи предпазни мерки при употреба
Общо взето
Тестове за HIV антитела трябва да се предложат на всички пациенти, заразени с HBV, преди започване на терапия с тенофовир дизопроксил фумарат (вижте долния раздел Съпътстваща инфекция с HIV-1 и хепатит В).
ХИВ-1
Въпреки че е доказано, че ефективната вирусна супресия с антиретровирусна терапия значително намалява риска от предаване по полов път, не може да се изключи остатъчен риск. Трябва да се вземат предпазни мерки за предотвратяване на предаването в съответствие с националните насоки.
Хроничен хепатит В
Пациентите трябва да бъдат уведомени, че не е доказано, че тенофовир дизопроксил фумарат предотвратява риска от предаване на HBV на трети страни чрез сексуален контакт или заразяване с кръв. Трябва да продължите да предприемате подходящи предпазни мерки.
Едновременното приложение с други лекарствени продукти
• Viread не трябва да се прилага едновременно с други лекарствени продукти, съдържащи тенофовир дизопроксил фумарат.
• Viread не трябва да се прилага едновременно с адефовир дипивоксил.
• Не се препоръчва едновременното приложение на тенофовир дизопроксил фумарат и диданозин. Едновременното приложение на тенофовир дизопроксил фумарат и диданозин води до 40-60% увеличение на системната експозиция на диданозин, което може да увеличи риска от свързани с диданозин нежелани реакции (вж. Точка 4.5). Рядко са докладвани панкреатит и ацидоза. Едновременното приложение на тенофовир дизопроксил фумарат и диданозин в дневна доза от 400 mg се свързва със значително намаляване на броя на CD4 клетките, вероятно поради „вътреклетъчно взаимодействие, което повишава нивата на фосфорилиран диданозин (активен). Намаляването на дозата на диданозин, прилаган едновременно с тенофовир дизопроксил фумарат до 250 mg, е свързано с „висока честота на вирусологични неуспехи“ в много комбинации, тествани за лечение на HIV-1 инфекция.
Тройна терапия с нуклеозиди / нуклеотиди
Когато тенофовир дизопроксил фумарат се прилага на пациенти с ХИВ в комбинация с ламивудин и абакавир, както и ламивудин и диданозин в схеми веднъж дневно, се наблюдава „висок процент на вирусологични неуспехи и ранно начало на резистентност.
Бъбречни и костни ефекти при възрастното население
Ефекти върху бъбреците
Тенофовир се елиминира главно от бъбреците. Съобщавани са случаи на бъбречна недостатъчност, бъбречно увреждане, повишен креатинин, хипофосфатемия и проксимална тубулопатия (включително синдром на Фанкони) при употребата на тенофовир дизопроксил фумарат в клиничната практика (вж. Точка 4.8).
Мониторинг на бъбречната функция
Препоръчва се измерване на креатининовия клирънс при всички пациенти преди започване на терапия с тенофовир дизопроксил фумарат, докато бъбречната функция (креатининов клирънс и серумен фосфат) трябва да се следи след две до четири седмици лечение, след три месеца лечение и на всеки три до шест месеца след това при пациенти без бъбречни рискови фактори Необходимо е по -често проследяване на бъбречната функция при пациенти с риск от бъбречно увреждане.
Управление на бъбречната функция
В случай на серумна глюкоза и концентрации на калиев фосфат в кръвта и глюкоза в урината (вж. Точка 4.8, проксимална тубулопатия). Трябва да се обмисли и прекратяване на терапията с тенофовир дизопроксил фумарат при възрастни пациенти с намален креатининов клирънс.
Едновременното приложение и риск от бъбречна токсичност
Използването на тенофовир дизопроксил фумарат трябва да се избягва, ако пациентът се лекува или наскоро е приемал нефротоксични лекарствени продукти (напр. Аминогликозиди, амфотерицин В, фоскарнет, ганцикловир, пентамидин, ванкомицин, цидофовир или интерлевкин-2). "Едновременна употреба на тенофовир диско фумарат и нефротоксични средства не могат да бъдат избегнати.Бъбречната функция трябва да се следи седмично.
След започване на многократни или високи дози нестероидни противовъзпалителни средства (НСПВС) са докладвани случаи на остра бъбречна недостатъчност при пациенти, лекувани с тенофовир дизопроксил фумарат, които имат рискови фактори за бъбречна дисфункция. Ако тенофовир дизопроксил фумарат се прилага едновременно до НСПВС бъбречната функция трябва да се следи адекватно.
Съобщава се за по-висок риск от бъбречно увреждане при пациенти, приемащи тенофовир дизопроксил фумарат в комбинация с ритонавир или повишен с кобицистат протеазен инхибитор. При тези пациенти е необходимо внимателно проследяване на бъбречната функция (вж. Точка 4.5). При пациенти с бъбречни рискови фактори, едновременното приложение на тенофовир дизопроксил фумарат с повишен протеазен инхибитор трябва да бъде внимателно обмислено.
Клинична оценка на тенофовир дизопроксил фумарат не е провеждана при пациенти, лекувани с лекарствени продукти, секретирани по същия бъбречен път, включително транспортиране на протеини чрез транспортьори на органични аниони 1 и 3 на човека (транспортиращ органичен анион на човека -hOAT) или MRP 4 (например цидофовир, лекарство с известни нефротоксични свойства). Тези бъбречни транспортери на протеини могат да бъдат отговорни за тубуларната секреция и отчасти за бъбречното елиминиране на тенофовир и цидофовир. Следователно, фармакокинетиката на тези лекарствени продукти, които се секретират по същия бъбречен път, включително протеиновия транспортер hOAT 1 и 3 или MRP 4 могат да бъдат променени, ако се прилагат в комбинация. Освен ако не е строго необходимо, едновременната употреба на тези лекарства, които се секретират по същия бъбречен път, не се препоръчва, но ако такава употреба е неизбежна, бъбречната функция трябва да се следи ежеседмично (вж. точка 4.5) .
Бъбречна недостатъчност
Бъбречната безопасност с тенофовир дизопроксил думарат е проучена само в много ограничена степен при възрастни пациенти с нарушена бъбречна функция (креатининов клирънс
Възрастни пациенти с креатининов клирънс
Има ограничени данни за безопасност и ефикасност на тенофовир дизопроксил фумарат при пациенти с бъбречно увреждане. Следователно тенофовир дизопроксил фумарат трябва да се използва само ако може да се прецени, че потенциалните ползи от лечението надвишават потенциалните рискове. При пациенти с умерено или тежко бъбречно увреждане (креатининов клирънс
Ефекти на костно ниво
В контролирано клинично проучване, проведено в продължение на 144 седмици, при пациенти, заразени с ХИВ, при които тенофовир дизопроксил фумарат е сравнен със ставудин в комбинация с ламивудин и ефавиренц при възрастни пациенти, които не са били предварително лекувани с антиретровирусни средства, се наблюдава леко намаляване на костната минерална плътност.минерална плътност на костите, BMD) в тазобедрената става и гръбначния стълб и в двете групи. Намаляването на BMD в гръбначния стълб и промените от изходното ниво в костните биомаркери бяха значително по-големи в групата с тенофовир дизопроксил фумарат на 144. седмица. до 96 -та седмица. Това обаче не увеличава риска от фрактури или доказателства за значителни костни аномалии след 144 седмици лечение.
Костни аномалии (рядко водещи до фрактури) могат да бъдат свързани с проксимална бъбречна тубулопатия (вж. Точка 4.8).
Ако се подозират или открият костни аномалии, трябва да се потърси подходяща консултация.
Бъбречни и костни ефекти при педиатричната популация
Дългосрочните ефекти на костната и бъбречната токсичност не са известни със сигурност. Също така не е възможно да се установи напълно обратимостта на бъбречната токсичност. Затова се препоръчва мултидисциплинарен подход за адекватна оценка на съотношението полза / риск от лечението за всеки отделен случай, за вземане на решение за подходящо наблюдение по време на лечението (включително решението за прекратяване на лечението) и за отчитане на необходимостта от допълнения.
Ефекти върху бъбреците
Бъбречни нежелани реакции, съответстващи на проксимална бъбречна тубулопатия, са докладвани в клинично проучване GS-US-104-0352 при инфектирани с HIV-1 педиатрични пациенти на възраст от 2 до
Мониторинг на бъбречната функция
Бъбречната функция (креатининов клирънс и серумен фосфат) трябва да се определи преди лечението и да се следи по време на лечението, както при възрастни (вж. По -горе).
Управление на бъбречната функция
В случай на потвърдени серумни концентрации на фосфат в урината (вж. Точка 4.8, проксимална тубулопатия). Ако се подозират или открият бъбречни аномалии, трябва да се потърси нефрологична консултация за оценка на евентуалното прекратяване на лечението с тенофовир дизопроксил фумарат. Прекратяването на тенофовир дизопроксил фумарат също трябва да се обмисли в случай на прогресивно намаляване на бъбречната функция, ако не е установена друга причина.
Едновременното приложение и риск от бъбречна токсичност
Същите препоръки важат като за възрастни (виж по -горе).
Бъбречна недостатъчност
Употребата на тенофовир дизопроксил фумарат не се препоръчва при педиатрични пациенти с бъбречно увреждане (вж. Точка 4.2) .Тенофовир дизопроксил фумарат не трябва да се започва при педиатрични пациенти с бъбречно увреждане и трябва да се преустанови при педиатрични пациенти, които развият бъбречно увреждане по време на лечението с тенофовир дизопроксил фумарат.
Ефекти на костно ниво
Viread може да причини намалена КМП. Ефектите на свързаните с тенофовир дизопроксил фумарат промени в КМП върху дългосрочното състояние на костите и бъдещия риск от фрактури все още не са известни (вж. Точка 5.1).
Ако се открият или подозират костни аномалии при педиатрични пациенти, трябва да се потърси консултация с ендокринолог и / или нефролог.
Чернодробно заболяване
Данните за безопасност и ефикасност са ограничени при пациенти с чернодробна трансплантация.
Данните за безопасност и ефикасност на тенофовир дизопроксил фумарат са ограничени при инфектирани с HBV пациенти с декомпенсирано чернодробно заболяване и оценка по Child-Pugh-Turcotte (CPT)> 9. Тези пациенти може да са с повишен риск от чернодробни или бъбречни нежелани реакции. Следователно при тази популация пациенти хепатобилиарните и бъбречните параметри трябва да се следят внимателно.
Обостряния на хепатит
Пристъпи по време на лечението: Спонтанните обостряния на хроничен хепатит В са сравнително чести и се характеризират с преходно повишаване на серумния ALT. След започване на антивирусна терапия серумният ALT може да се увеличи при някои пациенти (вж. Точка 4.8).
При пациенти с компенсирано чернодробно заболяване тези повишения на серумния ALT обикновено не са придружени от повишени серумни билирубинови концентрации или чернодробна декомпенсация. Пациентите с цироза могат да бъдат изложени на по -висок риск от чернодробна декомпенсация след обостряне на хепатит и поради това трябва да бъдат внимателно наблюдавани по време на терапията.
Обостряне след преустановяване на лечението: Съобщавани са и остри екзацербации на хепатит при пациенти, които са преустановили терапията с хепатит В. Екзацербациите след лечение обикновено са свързани с повишаване на HBV ДНК и повечето изглежда са самоограничаващи се. Въпреки това са докладвани тежки обостряния, включително фатални случаи Чернодробната функция трябва да се проследява на многократни интервали с проследяване както клинично, така и лабораторно в продължение на най-малко 6 месеца след прекратяване на терапията за хепатит В. Ако е подходящо, възобновяването на терапията е оправдано. При пациенти с напреднало чернодробно заболяване или цироза, преустановяването на лечението не се препоръчва като „обостряне на хепатит след лечение може да доведе до чернодробна декомпенсация.
Чернодробните обостряния са особено тежки и понякога фатални при пациенти с декомпенсирано чернодробно заболяване.
Съпътстваща инфекция с хепатит С или D: Няма данни за ефикасността на тенофовир при пациенти, коинфектирани с хепатит С или D вирус.
ХИВ-1 и хепатит В коинфекция: При пациенти, коинфектирани с HIV / HBV, поради риска от развитие на HIV резистентност, тенофовир дизопроксил фумарат трябва да се използва само като част от подходящ комбиниран антиретровирусен режим.Пациенти с предшестваща чернодробна дисфункция, включително хроничен активен хепатит, по време на комбинирана антиретровирусна терапия терапия (комбинирана антиретровирусна терапия, CART) показват увеличаване на честотата на нарушения на чернодробната функция и трябва да се проследяват в съответствие с общата клинична практика. Ако при такива пациенти настъпи влошаване на чернодробното заболяване, трябва да се обмисли прекъсване или прекратяване на лечението, но трябва да се отбележи, че повишаването на ALT може да бъде част от клирънса на HBV по време на терапията с тенофовир. (Вижте по -горе Обостряния на хепатит).
Липодистрофия
CART се свързва с преразпределение на телесните мазнини (липодистрофия) при пациенти с ХИВ. Дългосрочните последици от тези събития в момента не са известни. Познаването на механизма е непълно. Предполага се връзка между висцерална липоматоза и протеазни инхибитори и липоатрофия и нуклеозидни инхибитори на обратната транскриптаза. Повишен риск от липодистрофия е свързан с наличието на отделни фактори, като по-напреднала възраст, и фактори, свързани с лекарството, като по-голяма продължителност на антиретровирусно лечение и свързани метаболитни нарушения. Клиничният преглед трябва да включва оценка на физическите признаци на преразпределение на мазнините Трябва да се обмислят серумните измервания на липидите и глюкозата на гладно.
Тъй като тенофовир е структурно свързан с нуклеозидни аналози, рискът от липодистрофия не може да бъде изключен. Клиничните данни от 144 седмици лечение при HIV-инфектирани възрастни пациенти, които не са били предварително лекувани с антиретровирусни средства, показват, че рискът от липодистрофия е по-нисък при тенофовир дизопроксил фумарат в сравнение със ставудин, когато се прилага с ламивудин и ефавиренц.
Митохондриална дисфункция
Доказано е и това in vivo че инвитро, че нуклеозидните и нуклеотидните аналози причиняват различни нива на митохондриални увреждания. Има съобщения за митохондриална дисфункция при заразени с ХИВ отрицателни бебета, вътреутробно и / или след раждането, до нуклеозидни аналози. Основните съобщени нежелани реакции са хематологични нарушения (анемия, неутропения), метаболитни нарушения (хиперлактатемия, хиперлипаземия). Тези събития често са преходни. Някои неврологични нарушения (хипертония, конвулсии, анормално поведение) са докладвани като късни епизоди. Понастоящем не е известно дали неврологичните разстройства са преходни или постоянни. За всяко изложено дете вътреутробно към нуклеозидни или нуклеотидни аналози, дори ако HIV е отрицателен, a проследяване клинично и лабораторно и в случай на съответни признаци или симптоми пълен преглед за откриване на възможни митохондриални дисфункции. Тези констатации не променят настоящите национални препоръки за използване на антиретровирусна терапия при бременни жени за предотвратяване на вертикално предаване на ХИВ.
Синдром на имунна реактивация
При HIV-инфектирани пациенти с тежък имунен дефицит по време на въвеждането на CART може да възникне възпалителна реакция към асимптоматични или остатъчни опортюнистични патогени и да причини сериозни клинични състояния или влошаване на симптомите. Обикновено такива реакции са наблюдавани в рамките на първите няколко седмици или месеци след започване на CART. Съответни примери за това са цитомегаловирусен ретинит, генерализирани и / или фокални микобактериални инфекции и Pneumocystis jirovecii. Всички възпалителни симптоми трябва да бъдат оценени и при необходимост да се започне лечение.
Съобщава се и за появата на автоимунни нарушения (като болестта на Грейвс) в контекста на имунната реактивация; записаното време до началото е по -променливо и тези събития могат да настъпят дори много месеци след започване на лечението.
Остеонекроза
Въпреки че етиологията се счита за многофакторна (включително употреба на кортикостероиди, консумация на алкохол, тежка имуносупресия, по-висок индекс на телесна маса), случаи на остеонекроза са докладвани главно при пациенти с напреднало заболяване на ХИВ. И / или дългосрочно излагане на КАРТ Пациентите трябва посъветвайте се да потърсите медицинска помощ в случай на дискомфорт в ставите, болка и скованост или затруднено движение.
По-стари хора
Тенофовир дизопроксил фумарат не е проучен при пациенти на възраст над 65 години. При пациенти в напреднала възраст намалената бъбречна функция е по -вероятна, поради което лечението с тенофовир дизопроксил фумарат при възрастни хора трябва да се предприема с повишено внимание.
Гранулите Viread съдържат манитол, който може да има леко слабително действие.
04.5 Взаимодействия с други лекарствени продукти и други форми на взаимодействие
Проучвания за взаимодействия са провеждани само при възрастни.
Въз основа на резултатите, получени с експерименти инвитро и известни данни за пътя на елиминиране на тенофовир, потенциалът за CYP450-медиирани взаимодействия между тенофовир и други лекарствени продукти е нисък.
Съпътстващите терапии не се препоръчват
Viread не трябва да се прилага едновременно с други лекарствени продукти, съдържащи тенофовир дизопроксил фумарат.
Viread не трябва да се прилага едновременно с адефовир дипивоксил.
Диданозин
Не се препоръчва едновременното приложение на тенофовир дизопроксил фумарат и диданозин (вж. Точка 4.4 и таблица 2).
Лекарствени продукти, отделяни от бъбреците
Тъй като тенофовир се елиминира предимно от бъбреците, едновременното приложение на тенофовир дизопроксил фумарат с лекарствени продукти, които намаляват бъбречната функция или се конкурират за активна тубулна секреция чрез транспортера на протеини hOAT 1, hOAT 3 или MRP 4 (например цидофовир) може да повиши серумните концентрации тенофовир и / или други едновременно прилагани лекарствени продукти.
Употребата на тенофовир дизопроксил фумарат трябва да се избягва при едновременна или скорошна употреба на нефротоксични лекарствени продукти. Някои примери включват, но не се ограничават до: аминогликозиди, амфотерицин В, фоскарнет, ганцикловир, пентамидин, ванкомицин, цидофовир или интерлевкин-2 (вж. Точка 4.4).
Тъй като такролимус може да повлияе на бъбречната функция, се препоръчва внимателно проследяване, когато се прилага с тенофовир дизопроксил фумарат.
Други взаимодействия
Взаимодействията между тенофовир дизопроксил фумарат и протеазните инхибитори и антиретровирусни препарати, различни от протеазните инхибитори, са показани в Таблица 2 по -долу ("увеличението е посочено като" ↑ ", намалено като"? ", Няма промяна като" ↔ ", два пъти дневно като" наддаване ") , веднъж на ден като "qd").
Таблица 2: Взаимодействия между тенофовир дизопроксил фумарат и други лекарствени продукти
Проучвания, проведени с други лекарства
Няма клинично значими фармакокинетични взаимодействия, когато тенофовир дизопроксил фумарат се прилага едновременно с емтрицитабин, ламивудин, индинавир, ефавиренц, нелфинавир, саквинавир (усилен с ритонавир), метадон, рибавирин, рифестампицин, етакролимус или хормонални контрацептиви.
Тенофовир дизопроксил фумарат трябва да се приема с храна, тъй като храната повишава бионаличността на тенофовир (вж. Точка 5.2).
04.6 Бременност и кърмене
Бременност
Умерено количество данни при бременни жени (между 300 и 1000 бременности при експозиция) показва, че няма малформации или фетална / неонатална токсичност, свързани с тенофовир дизопроксил фумарат. Проучванията при животни не показват репродуктивна токсичност (вж. Точка 5.3). При необходимост може да се обмисли употребата на тенофовир дизопроксил фумарат по време на бременност.
Време за хранене
Доказано е, че тенофовир се екскретира в кърмата. Няма достатъчно информация за ефектите на тенофовир върху новородени / кърмачета. Следователно Viread не трябва да се използва по време на кърмене.
Като общо правило се препоръчва жените, заразени с HIV и HBV, да не кърмят бебетата си, за да се избегне предаването на HIV и HBV на новороденото.
Плодовитост
Клиничните данни за ефекта на тенофовир дизопроксил фумарат върху фертилитета са ограничени. Проучванията при животни не показват вредни ефекти на тенофовир дизопроксил фумарат върху фертилитета.
04.7 Ефекти върху способността за шофиране и работа с машини
Не са провеждани проучвания за способността за шофиране и работа с машини.
04.8 Нежелани реакции
Обобщение на профила на безопасност
ХИВ-1 и хепатит В: При пациенти, приемащи тенофовир дизопроксил фумарат, са докладвани редки събития, бъбречно увреждане, бъбречна недостатъчност и проксимална бъбречна тубулопатия (включително синдром на Фанкони), които понякога водят до костни промени (и рядко фрактури). При пациенти, приемащи Viread, се препоръчва проследяване на бъбречната функция (вж. Точка 4.4).
ХИВ-1: Приблизително една трета от пациентите могат да получат нежелани реакции след лечение с тенофовир дизопроксил фумарат в комбинация с други антиретровирусни средства. Тези реакции обикновено се състоят от леки или умерени стомашно -чревни епизоди. Приблизително 1% от възрастните пациенти, лекувани с тенофовир дизопроксил фумарат, са прекратени поради стомашно -чревни ефекти.
Липодистрофията е свързана с тенофовир дизопроксил фумарат (вж. Точки 4.4 и 4.8 Описание на избрани нежелани реакции).
Едновременното приложение на Viread и диданозин не се препоръчва, тъй като може да доведе до повишен риск от нежелани реакции (вж. Точка 4.5) Рядко се съобщава за панкреатит и лактатна ацидоза, понякога фатални (вж. Точка 4.4).
Хепатит Б: Приблизително една четвърт от пациентите, приемащи тенофовир дизопроксил фумарат, могат да получат нежелани реакции, повечето от които са леки. В клинични проучвания с пациенти, инфектирани с HBV, най -честата нежелана реакция е гадене (5,4%).
Съобщавани са остри екзацербации на хепатит както при пациенти на лечение, така и при пациенти, които са преустановили лечението на хепатит В (вж. Точка 4.4).
Обобщена таблица на нежеланите реакции
Оценката на нежеланите реакции за тенофовир дизопроксил фумарат се основава на данни за безопасност от клинични проучвания и постмаркетингов опит. Всички нежелани реакции са показани в таблица 3.
Клинични проучвания при HIV-1: Оценката на нежеланите реакции от клинични изпитвания за HIV-1 се основава на опита от две проучвания, в които 653 възрастни пациенти с предишен опит в лечението са лекувани с тенофовир дизопроксил фумарат (n = 443) или плацебо (n = 210) в комбинация с други антиретровирусни лекарствени продукти за 24 седмици, както и двойно-сляпо контролирано сравнително проучване, при което 600 нелекувани възрастни пациенти са лекувани или с тенофовир дизопроксил 245 mg (като фумарат) (n = 299) или със ставудин (n = 301) в комбинация с ламивудин и ефавиренц в продължение на 144 седмици.
Клинични проучвания при хепатит В: Оценката на нежеланите реакции от данните от клиничните изпитвания се основава главно на опита от две двойно-слепи, контролирани сравнителни проучвания при 641 възрастни пациенти с хроничен хепатит В и компенсирано чернодробно заболяване, лекувани с тенофовир дизопроксил 245 mg (като фумарат) на ден (n = 426) или адефовир дипивоксил 10 mg дневно (n = 215) в продължение на 48 седмици. Нежеланите реакции, наблюдавани при продължително лечение от 384 седмици, са в съответствие с профила на безопасност на тенофовир дизопроксил фумарат. След първоначален спад от приблизително - 4,9 ml / min ( използвайки уравнението на Cockcroft -Gault) или -3.9 mL / min / 1.73 m2 (използвайки уравнението за промяна на диетата при бъбречно заболяване [промяна на диетата при бъбречно заболяване, MDRD]) след първите 4 седмици от лечението, процентът на годишен пост -изходен спад на бъбречната функция, докладван при пациенти, лекувани с тенофовир дизопроксил фумарат, е -1,41 ml / min годишно (използвайки уравнението на Cockcroft -Gault) и -0,74 mL / min / 1,73 m2 годишно (използвайки уравнението на MDRD).
Пациенти с декомпенсирано чернодробно заболяване: Профилът на безопасност на тенофовир дизопроксил фумарат при пациенти с декомпенсирано чернодробно заболяване е оценен в двойно-сляпо контролирано проучване (GS-US-174-0108), при което възрастни пациенти са лекувани в продължение на 48 седмици с тенофовир дизопроксил фумарат (n = 45) или емтрицитабин плюс тенофовир дизопроксил фумарат (n = 45) или ентекавир (n = 22).
В групата за лечение с тенофовир дизопроксил фумарат 7% от пациентите са прекратили лечението поради нежелано събитие; 9% от пациентите са имали потвърдено повишаване на серумния креатинин ≥ 0,5 mg / dL или потвърдена серумна фосфатна стойност ≥ 0,5 mg / dL или потвърдена серумна фосфатна стойност
На 168 седмица при тази популация от пациенти с декомпенсирано чернодробно заболяване смъртността е била 13% (6/45) в групата на тенофовир дизопроксил фумарат, 11% (5/45) в групата на емтрицитабин плюс тенофовир дизопроксил фумарат и 14% (3 /22) в групата на ентекавир. Честотата на хепатоцелуларен карцином е 18% (8/45) в групата на тенофовир дизопроксил фумарат, 7% (3/45) в групата на емтрицитабин плюс тенофовир дизопроксил фумарат и 9% (2/ 22) в групата на ентекавир.
Установено е, че субектите с висок изходен CPT резултат са с повишен риск от развитие на сериозни нежелани събития (вж. Точка 4.4).
Пациенти с хроничен резистентен към ламивудин хепатит В: В рандомизирано, двойно-сляпо проучване (GS-US-174-0121), при което 280 резистентни на ламивудин пациенти са лекувани с тенофовир дизопроксил фумарат (n = 141) или емтрицитабин / тенофовир дизопроксил фумарат (n = 139) до 96 седмици не са установени нови нежелани реакции при тенофовир дизопроксил фумарат.
Нежеланите реакции, които имат предполагаема (или поне възможна) корелация с лечението, са изброени по -долу, разделени по системо -органен клас и честота. В рамките на всеки честотен клас нежеланите реакции са изброени в низходящ ред. Честотите се определят като много чести (≥ 1/10), чести (≥ 1/100,
Таблица 3: Обобщена таблица на нежеланите реакции, свързани с тенофовир дизопроксил фумарат въз основа на клинични проучвания и постмаркетингов опит
1 Тази нежелана реакция може да възникне вследствие на проксимална бъбречна тубулопатия. При липса на това състояние не се счита, че е свързано с тенофовир дизопроксил фумарат.
2 Тази нежелана реакция е установена чрез постмаркетингово наблюдение, но не е наблюдавана при рандомизирани контролирани клинични проучвания или програми за разширен достъп с тенофовир дизопроксил фумарат. Честотата се оценява чрез статистическо изчисление въз основа на общия брой пациенти, изложени на тенофовир дизопроксил фумарат в рандомизирани контролирани проучвания и програми с разширен достъп (n = 7319).
Описание на избрани нежелани реакции
ХИВ-1 и хепатит В:
Бъбречна недостатъчност
Тъй като Viread може да причини бъбречно увреждане, се препоръчва проследяване на бъбречната функция (вж. Точки 4.4 и 4.8 Обобщение на профила на безопасност). Проксималната бъбречна тубулопатия обикновено отзвучава или се подобрява след прекратяване на тенофовир дизопроксил фумарат. При някои пациенти обаче намаленият креатининов клирънс не отшумява напълно въпреки преустановяването на тенофовир дизопроксил фумарат.При пациенти с риск от бъбречно увреждане (като пациенти с изходни бъбречни рискови фактори, ХИВ заболяване или пациенти, приемащи съпътстващи нефротоксични лекарствени продукти) възстановяване на бъбреците функцията е по -вероятно да бъде непълна, въпреки прекратяването на тенофовир дизопроксил фумарат (вж. точка 4.4).
ХИВ-1:
Взаимодействия с диданозин
Едновременното приложение на тенофовир дизопроксил фумарат и диданозин не се препоръчва, тъй като води до 40-60% увеличение на системната експозиция на диданозин и може да доведе до повишен риск от свързани с диданозин нежелани реакции (вж. Точка 4.5). Рядко се съобщава за панкреатит и лактатна ацидоза, понякога фатални.
Липиди, липодистрофия и метаболитни промени
CART се свързва с метаболитни аномалии като хипертриглицеридемия, хиперхолестеролемия, инсулинова резистентност, хипергликемия и хиперлактатемия (вж. Точка 4.4).
CARt се свързва с преразпределението на телесните мазнини (липодистрофия) при HIV-инфектирани пациенти, включително загуба на периферна и лицева подкожна мазнина, увеличена коремна и висцерална мазнина, „хипертрофия на гърдите и„ натрупване на дорзоцервикална мазнина (биволска гърбица) (вж. 4.4).
В 144-седмично контролирано проучване, проведено при възрастни пациенти, които не са били предварително лекувани с антиретровирусни лекарства, сравняващо тенофовир дизопроксил фумарат със ставудин в комбинация с ламивудин и ефавиренц, пациентите, лекувани с тенофовир дизопроксил фумарат, имат значително по-ниска честота на липодистрофия в сравнение с пациентите, които са били лекуван със ставудин Рамото с тенофовир дизопроксил фумарат също показа значително по -ниско средно увеличение на триглицеридите и общия холестерол на гладно в сравнение с рамото за сравнение.
Синдром на имунна реактивация
При HIV-инфектирани пациенти с тежък имунен дефицит по време на започване на CART може да възникне възпалителна реакция към асимптоматични или остатъчни опортюнистични инфекции. Съобщавани са и автоимунни нарушения (като болестта на Грейвс); той е по -променлив и тези събития могат да настъпят дори много месеци след започване на лечението (вж. точка 4.4).
Остеонекроза
Случаи на остеонекроза са докладвани главно при пациенти с общоизвестни рискови фактори, с напреднало ХИВ заболяване и / или дългосрочно излагане на CART. Честотата на такива случаи е неизвестна (вж. Точка 4.4).
Хепатит Б:
Обостряния на хепатит по време на лечението
В проучвания с пациенти, които не са били лекувани с нуклеозид, повишенията на ALT> 10 пъти ULN, ULN и> 2 пъти изходните стойности са настъпили по време на лечението при 2,6% от пациентите, лекувани с тенофовир дизопроксил фумарат. Повишаването на ALT продължава средно 8 седмици, отшумява с продължаване на терапията и в повечето случаи се свързва с намаление на вирусното натоварване с ≥ 2 log 10 копия / mL, което предшества или съвпада с увеличаването на ALT. По време на лечението се препоръчва периодично проследяване на чернодробната функция (вж. Точка 4.4).
Обостряния на хепатит след преустановяване на лечението
Клинични и лабораторни данни за обостряне на хепатит се появиха при пациенти с HBV инфекция след преустановяване на лечението с HBV (вж. Точка 4.4).
Педиатрична популация
ХИВ-1
Оценката на нежеланите реакции се основава на две рандомизирани проучвания (проучвания GS-US-104-0321 и GS-US-104-0352), проведени при 184 педиатрични пациенти (на 2 години и обобщена таблица на нежеланите реакции и 5.1).
Съобщава се за намаление на КМП при педиатрични пациенти. При инфектирани с HIV-1 юноши, BM-Z-резултатите, наблюдавани при лица, приемащи тенофовир дизопроксил фумарат, са по-ниски от тези, наблюдавани при лица, приемащи плацебо. При заразени с HIV-1 деца, BM-Z-резултатите, наблюдавани при лица, преминали на тенофовир дизопроксил фумарат, са по-ниски от тези, наблюдавани при лица, които са останали на терапия със ставудин или зидовудин (вж. Точки 4.4 и 5.1).
От 89 пациенти (на възраст от 2 до
Хроничен хепатит В
Оценката на нежеланите реакции се основава на рандомизирано проучване (проучване GS-US-174-0115), проведено при 106 подрастващи пациенти (на 12 години и обобщена таблица на нежеланите реакции и 5.1).
Намаляване на BMD се наблюдава при юноши, заразени с HBV. Z-резултатите от BMD Z, наблюдавани при лица, приемащи тенофовир дизопроксил фумарат, са по-ниски от тези, наблюдавани при лица, приемащи плацебо (вж. Точки 4.4 и 5.1).
Други специални популации
По-стари хора
Тенофовир дизопроксил фумарат не е проучен при пациенти на възраст над 65 години. По -възрастните пациенти са по -склонни да имат намалена бъбречна функция, поради което тенофовир дизопроксил фумарат трябва да се използва с повишено внимание при лечението на тези пациенти (вж. Точка 4.4).
Пациенти с бъбречно увреждане
Тъй като тенофовир дизопроксил фумарат може да причини бъбречна токсичност, се препоръчва внимателно проследяване на бъбречната функция при възрастни пациенти с бъбречно увреждане, лекувани с Viread (вж. Точки 4.2, 4.4 и 5.2). Употребата на тенофовир дизопроксил фумарат не се препоръчва при педиатрични пациенти с бъбречно увреждане (вж. Точки 4.2 и 4.4).
Докладване на предполагаеми нежелани реакции
Съобщаването на предполагаеми нежелани реакции, настъпили след разрешаване на лекарствения продукт, е важно, тъй като позволява непрекъснато проследяване на съотношението полза / риск на лекарствения продукт. От медицинските специалисти се изисква да съобщават всички предполагаеми нежелани реакции чрез националната система за докладване:
Италианска агенция по лекарствата
Уебсайт: http://www.agenziafarmaco.gov.it/it/responsabili
04.9 Предозиране
Симптоми
В случай на предозиране, пациентът трябва да бъде наблюдаван за признаци на токсичност (вж. Точки 4.8 и 5.3) и, ако е необходимо, да се прилага обичайната поддържаща грижа.
Управление
Тенофовир може да бъде отстранен чрез хемодиализа; средният клирънс за хемодиализа е 134 ml / min. Не е известно дали тенофовир може да се елиминира чрез перитонеална диализа.
05.0 ФАРМАКОЛОГИЧНИ СВОЙСТВА
05.1 Фармакодинамични свойства
Фармакотерапевтична група: Антивирусни средства за системна употреба; нуклеозиди и нуклеотиди, инхибиращи обратната транскриптаза, АТС код: J05AF07
Механизъм на действие и фармакодинамични ефекти
Тенофовир дизопроксил фумарат е фумаратната сол на пролекарството тенофовир дизопроксил. Тенофовир дизопроксил се абсорбира и превръща в активното вещество тенофовир, което е монофосфатен (нуклеотиден) нуклеозиден аналог.След това тенофовир се превръща в активния метаболит тенофовир дифосфат, задължителен терминатор на веригата, чрез конститутивно експресирани клетъчни ензими. Тенофовир дифосфатът има вътреклетъчен полуживот от 10 часа в активирани мононуклеарни клетки от периферна кръв (РВМС) и 50 часа в клетки в покой. Тенофовир дифосфатът инхибира HIV-1 обратната транскриптаза и вирусните HBV полимерази чрез свързване в пряка конкуренция с естествения субстрат дезоксирибонуклеотид и чрез крайната верига на ДНК след включване в самата ДНК. Тенофовир дифосфат слаб инхибитор ли е на клетъчните полимерази?,? И ?. Тенофовир не демонстрира никакъв ефект върху синтеза на митохондриална ДНК или производството на млечна киселина в тестовете инвитро, при концентрации до 300 mcmol / l.
Данни, свързани с ХИВ
In vitro активност на HIV антивирусни лекарства: Необходимата концентрация на тенофовир за 50% (EC50) инхибиране на див тип Лабораторният тест за HIV-1IIIB е 1-6 μmol / l в лимфоидни клетъчни линии и 1,1 μmol / l срещу първични HIV-1 подтип В изолати в PBMCs. Тенофовир е активен и срещу HIV-1 подтипове A, C, D, E, F, G и O и срещу HIVBaL в първични клетки от моноцити / макрофаги. Тенофовир е активен инвитро срещу HIV-2, с EC50 от 4,9 μmol / l в МТ-4 клетки.
Устойчивост: Те са избрани инвитро и при някои пациенти (вж. Клинична ефикасност и безопасност) щамове на HIV-1 с по-ниска чувствителност към тенофовир и мутация K65R в обратна транскриптаза. Тенофовир дизопроксил фумарат трябва да се избягва при антиретровирусни пациенти, лекувани преди това с мутация на K65R (вж. Точка 4.4). В допълнение, K70E заместване в обратна транскриптаза на HIV-1 е избрано с тенофовир, което води до леко намалена чувствителност към тенофовир.
Клиничните проучвания при пациенти, лекувани по-рано, оценяват анти-HIV активността на тенофовир дизопроксил 245 mg (като фумарат) срещу резистентни на нуклеозидни инхибитори щамове HIV-1. Резултатите показват, че пациенти с ХИВ, които са имали 3 или повече мутации, свързани с аналози на тимидин ( TAMs), които включват мутация на обратна транскриптаза на M41L или L210W, показват намалена чувствителност към терапия с 245 mg тенофовир дизопроксил (като фумарат).
Клинична ефикасност и безопасност
Демонстрацията на активност на тенофовир дизопроксил фумарат при пациенти, заразени с HIV-1 с предишен опит в лечението, и при нелекувани пациенти е демонстрирана в клинични изпитвания, съответно 48 седмици и 144 седмици.
В проучване GS-99-907, 550 възрастни пациенти с предишен опит в лечението са получавали 245 mg плацебо или тенофовир дизопроксил 245 mg (като фумарат) за 24 седмици. Средният изходен брой на CD4 е 427 клетки / mm3, средната изходна плазмена HIV-1 РНК е 3,4 log10 копия / ml (78% от пациентите имат вирусен товар от
На 24 -та седмица среднопретеглената промяна в сравнение с изходното ниво в плазмените нива на HIV -1 РНК на log10 (DAVG24) е -0.03 log10 копия / ml и -0.61 log10 копия / ml за пациенти, приемащи плацебо и тенофовир дизопроксил 245 mg (като фумарат ) (стр
144-седмичната, двойно-сляпа, контролирана фаза на проучване GS-99-903 оценява ефикасността и безопасността на тенофовир дизопроксил 245 mg (като фумарат) срещу ставудин, когато се използва в комбинация с ламивудин и ефавиренц при възрастни пациенти, заразени с HIV-1, които преди това не са лекувани с антиретровирусна терапия. Средният изходен брой CD4 клетки е 279 клетки / mm3, средната изходна плазмена HIV-1 РНК е 4,91 log10 копия / ml, 19% от пациентите са имали симптоматична HIV инфекция и 18% са имали СПИН. Пациентите са стратифицирани от HIV-1 РНК и изходен CD4 43% от пациентите са имали изходен вирусен товар> 100 000 копия / mL и 39% са имали брой CD4 клетки
От анализа на „намерението да се лекува“ (липсващи данни и промени в антиретровирусната терапия (ART) се считат за неуспешни), делът на пациентите с HIV-1 РНК под 400 копия / ml и 50 копия / ml на 48-седмично лечение, той е съответно 80% и 76% в групата с тенофовир дизопроксил 245 mg (като фумарат), в сравнение с 84% и 80% в рамото на ставудин.На 144-та седмица процентът на пациентите с HIV-1 РНК под 400 копия / mL и 50 копия / mL е 71% и 68% в групата с тенофовир дизопроксил 245 mg (като фумарат) спрямо 64% и 63% в рамото на ставудин, съответно.
Средната промяна от изходното ниво за броя на HIV-1 РНК и CD4 на седмица 48 от лечението е сходна и в двете групи (-3.09 и -3.09 log10 копия / ml; съответно +169 и 167 клетки / mm3. Група, лекувана с тенофовир дизопроксил 245 mg (като фумарат) и в групата, лекувана със ставудин). На 144 седмици от лечението средната промяна спрямо изходното ниво остава сходна и в двете групи (-3,07 и -3,03 log10 копия / ml; +263 и +283 клетки / mm3, съответно, в групите с тенофовир дизопроксил (като фумарат) и ставудин ). Наблюдава се последователен отговор на лечението с 245 mg тенофовир дизопроксил (като фумарат), независимо от изходния брой на HIV-1 РНК и CD4.
Мутацията на K65R се наблюдава при малко по -висок дял от пациентите в групата на тенофовир дизопроксил фумарат, отколкото в групата с активна контрола (2,7% срещу 0,7%). Във всички случаи резистентността към ефавиренц или ламивудин или предхожда, или съвпада с развитието на K65R. Осем пациенти с ХИВ с K65R в групата с тенофовир дизопроксил 245 mg (като фумарат); при 7 от тях това се е случило през първите 48 седмици от лечението и през последните на 96 седмици. Не е наблюдавано по -нататъшно развитие на K65R до 144 седмици. Един пациент в групата с тенофовир дизопроксил (като фумарат) е развил заместването. K70E в вирус Нито генотипният, нито фенотипният анализ разкриха доказателства за друга резистентност към тенофовир.
Данни, свързани с „HBV
Антивирусна HBV активност in vitro: Антивирусната активност инвитро на тенофовир спрямо HBV се оценява в клетъчната линия HepG2 2.2.15. Стойностите на EC50 за тенофовир са в диапазона от 0,14 до 1,5 μmol / l, със стойности на CC50 (50% цитотоксична концентрация)> 100 mcmol / l .
Устойчивост: Не са идентифицирани HBV мутации, свързани с резистентност към тенофовир дизопроксил фумарат (вж. Клинична ефикасност и безопасност). В клетъчните анализи, HBV щамове, експресиращи rtV173L, rtL180M и rtM & SUP2; 04I / V мутации, свързани с резистентност към ламивудин и телбивудин, показват чувствителност към тенофовир в диапазона от 0,7 до 3,4 пъти по-висок от този на вируса от див тип.
Клинична ефикасност и безопасност
HBV щамове, експресиращи rtL180M, rtT184G, rtS202G / I, rtM & SUP2; 04V и rtM & SUP2; 50V мутации, свързани с резистентност към ентекавир, показват чувствителност към тенофовир в диапазона от 0,6 до 6,9 пъти на вируса от див тип. Мутациите на rtA181V и rtN236T, свързани с резистентност към адефовир дипивоксил, показват чувствителност към тенофовир в диапазона от 2,9 до 10 пъти в сравнение с вируса от див тип. Вирусите, съдържащи мутацията rtA181T, остават чувствителни към тенофовир с EC стойности
Демонстрацията на ползите от тенофовир дизопроксил фумарат при компенсирано и декомпенсирано заболяване се основава на вирусологични, биохимични и серологични реакции при лечението на възрастни с HBeAg позитивен и HBeAg отрицателен хроничен хепатит В. Лекуваните пациенти са включвали нелекувани пациенти, пациенти с предишен опит с лечение с ламивудин, пациенти с предишен опит с лечение с адефовир дипивоксил и пациенти с мутации на резистентност към ламивудин и / или адефовир дипивоксил в началото. Ползите също са демонстрирани въз основа на хистологични отговори при компенсирани пациенти.
Опит при пациенти с компенсирано чернодробно заболяване на седмица 48 (проучвания GS-US-174-0102 и GS-US-174-0103)
48-седмичните резултати от две двойно-слепи рандомизирани проучвания фаза III, сравняващи тенофовир дизопроксил и адефовир дипивоксил при възрастни пациенти с компенсирано чернодробно заболяване, са представени в Таблица 4 по-долу. Проучване GS-US-174-0103 е проведено при 266 HBeAg позитивни пациенти (рандомизирани и лекувани), докато проучване GS-US-174-0102 е проведено при 375 пациенти (рандомизирани и лекувани), отрицателни за HBeAg и положителни за HBeAb.
И в двете проучвания беше установено, че тенофовир дизопроксил фумарат е значително по -добър от адефовир дипивоксил по отношение на първичната крайна точка за ефикасност на пълния отговор (дефиниран като нива на ДНК на HBV.
В проучване GS-US-174-0103 значително по-висок дял от пациентите на тенофовир дизопроксил фумарат в сравнение с групата на адефовир дипивоксил постига нормализиране на ALT и загуба на HBsAg на 48-та седмица (вж. Таблица 4 по-долу) .50 1,5 пъти по-голяма от тази на дивия тип вирус.
Таблица 4: Параметри на ефикасност след 48 седмици при HBeAg отрицателни и HBeAg позитивни пациенти с компенсация
* P-стойност срещу адефовир дипивоксил
пълен отговор, определен като нива на HBV ДНК
b Подобряване на некроинфламаторния индекс на Knodell с поне 2 точки без влошаване на фиброзата на Knodell.
c Средната промяна от изходното ниво в HBV DNA просто отразява разликата между "HBV DNA в началото и границата на идентификация" (Граница на откриване, LOD) от теста.
d Популацията, използвана за анализи за нормализиране на ALT, включва само пациенти с ALT над нормата (ULN) в началото.
n / a = не е приложимо.
Тенофовир дизопроксил фумарат е свързан със значително по -висок дял пациенти с неоткриваема HBV ДНК (
Когато се комбинират проучвания GS-US-174-0102 и GS-US-174-0103, отговорът на лечението с тенофовир дизопроксил фумарат е сравним при пациенти, лекувани с нуклеозид (n = 51), при пациенти, които не са лекувани с нуклеозид (n = 375) и при пациенти с нормална (n = 21) и ненормална (n = 405) ALT в началото. Четиридесет и девет от 51 пациенти, предварително лекувани с нуклеозиди, преди това са били лекувани с ламивудин. Седемдесет и три процента от пациентите, лекувани с нуклеозиди, и 69% от пациентите, които не са били лекувани предварително, постигат пълен отговор на лечението; 90% от пациентите, лекувани преди това с нуклеозид, и 88% от пациентите, които не са били лекувани предварително, са постигнали потискане на HBV ДНК
Опит над 48 седмици в проучвания GS-US-174-0102 и GS-US-174-0103
В проучвания GS-US-174-0102 и GS-US-174-0103, след получаване на двойно-сляпо лечение в продължение на 48 седмици (както тенофовир дизопроксил 245 mg (като фумарат), така и адефовир дипивоксил 10 mg), пациентите са сменени, без прекъсване на лечение, до открита терапия с тенофовир дизопроксил фумарат. 77% и 61% от пациентите, участващи съответно в проучвания GS-US-174-0102 и GS-US-174-0103, продължиха проучването в продължение на 384 седмици. На седмици 96, 144, 192, 240, 288 и 384, вирусологично потискане, биохимичните и серологичните отговори се поддържат при продължително лечение с тенофовир дизопроксил фумарат (вж. таблици 5 и 6 по -долу).
Таблица 5: Параметрите на ефикасност на 96, 144, 192, 240, 288 и 384 седмици на открито лечение при пациенти с отрицателна компенсация на HBeAg
Проучване 174-0102 (HBeAg отрицателно)
Въз основа на алгоритъма Дългосрочна оценка (LTE анализ) - Пациентите, които са прекратили терапията преди седмица 384 поради определена протоколна цел, както и тези, които са завършили терапията до седмица 384, са включени в знаменателя.
b 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 48 седмици отворен етикет.
c 48 седмици двойно-сляп адефовир дипивоксил, последван от 48 седмици открит тенофовир дизопроксил фумарат.
d Популацията, използвана за анализи за нормализиране на ALT, включва само пациенти с ALT над нормалните изходни нива.
и 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 96 седмици отворен етикет.
f 48 седмици двойно-сляп адефовир дипивоксил, последван от 96 седмици открит тенофовир дизопроксил фумарат.
g 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 144 седмици отворен етикет.
h 48 седмици двойно-сляп адефовир дипивоксил, последван от 144 седмици открит тенофовир дизопроксил фумарат.
48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 192 седмици отворен етикет.
48 седмици двойно-сляп адефовир дипивоксил, последван от 192 седмици открит тенофовир дизопроксил фумарат.
k Един пациент в тази група за пръв път е станал HBsAg отрицателен при посещението на седмица 240 и все още е участвал в проучването по време на прекъсване на данните. Загубата на HBsAg на субекта обаче бе окончателно потвърдена при следващото посещение.
l 48 седмици двойно-сляпо тенофовир дизопроксил фумарат, последвано от 240 седмици отворен етикет.
m 48 седмици двойно-сляп адефовир дипивоксил, последван от 240 седмици открит тенофовир дизопроксил фумарат.
n Показаните числа се отнасят до кумулативни проценти, базирани на анализа на Kaplan Meier, с изключение на данните, събрани след добавянето на емтрицитабин към отворения етикет тенофовир дизопроксил фумарат (KM-TDF).
или 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 336 седмици отворен етикет.
p 48 седмици двойно-сляп адефовир дипивоксил, последван от 336 седмици открит тенофовир дизопроксил фумарат.
n / a = не е приложимо.
Таблица 6: Параметри на ефикасност на 96, 144, 192, 240, 288 и 384 седмици от открито лечение при пациенти с HBeAg положителна компенсация
Проучване 174-0103 (HBeAg положително)
Въз основа на алгоритъма Дългосрочна оценка (LTE анализ) - Пациентите, които са прекратили терапията преди седмица 384 поради определена протоколна цел, както и тези, които са завършили терапията до седмица 384, са включени в знаменателя.
b 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 48 седмици отворен етикет.
c 48 седмици двойно-сляп адефовир дипивоксил, последван от 48 седмици открит тенофовир дизопроксил фумарат.
d Популацията, използвана за анализи за нормализиране на ALT, включва само пациенти с ALT над нормалните изходни нива.
и 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 96 седмици отворен етикет.
f 48 седмици двойно-сляп адефовир дипивоксил, последван от 96 седмици открит тенофовир дизопроксил фумарат.
g Показаните числа се отнасят до кумулативни проценти, базирани на анализа на Kaplan Meier, включително данни, събрани след добавянето на емтрицитабин към отворен етикет тенофовир дизопроксил фумарат (KM-ITT).
h 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 144 седмици отворен етикет.
48 седмици двойно-сляп адефовир дипивоксил, последван от 144 седмици открит тенофовир дизопроксил фумарат.
48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 192 седмици отворен етикет.
k 48 седмици двойно-сляп адефовир дипивоксил, последван от 192 седмици открит тенофовир дизопроксил фумарат.
Показаните числа се отнасят до кумулативни проценти, базирани на анализа на Kaplan Meier, с изключение на данните, събрани след добавянето на емтрицитабин към отворения етикет тенофовир дизопроксил фумарат (KM-TDF).
m 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 240 седмици отворен етикет.
n 48 седмици двойно-сляп адефовир дипивоксил, последван от 240 седмици открит тенофовир дизопроксил фумарат.
или 48 седмици двойно-сляп тенофовир дизопроксил фумарат, последван от 336 седмици отворен етикет.
p 48 седмици двойно-сляп адефовир дипивоксил, последван от 336 седмици открит тенофовир дизопроксил фумарат.
Бяха налични сдвоени изходни данни и данни за чернодробна биопсия за 240 седмици за 331/489 пациенти, които са продължили проучванията GS-US-174-0102 и GS-US-174-0103 на 240 седмици (вж. Таблица 7 по-долу). Деветдесет и пет процента (225/237) от пациентите без цироза в началото и 99% (93/94) от пациентите с цироза в началото не са имали промяна или подобрение на фиброзата (оценка на фиброзата на Ишак). От 94 пациенти с цироза на изходно ниво (фиброза на Ishak: 5-6), 26% нямат промяна в резултата на фиброзата на Ishak, а 72% имат регресия на цироза до 240 седмица с намаляване на фиброзата на Ishak с най-малко 2 точки.
Таблица 7: Хистологичен отговор (%) на седмица 240 от изходното ниво при HBeAg отрицателни и HBeAg положително компенсирани пациенти
a Популацията, използвана за хистологичен анализ, включва само пациенти, за които има данни за чернодробна биопсия (липсващи = изключени) на 240 -та седмица. Реакцията след добавяне на емтрицитабин е изключена (общо 17 пациенти в двете проучвания).
b Подобряване на некроинфламаторния индекс на Knodell с поне 2 пункта без влошаване на индекса на фиброзата на Knodell.
c 48 седмици двойно-сляпо тенофовир дизопроксил фумарат, последвано от до 192 седмици отворен етикет.
d 48 седмици двойно-сляп адефовир дипивоксил, последван от до 192 седмици открит тенофовир дизопроксил фумарат.
Опит при пациенти, коинфектирани с HIV, и предишно лечение с ламивудин
В 48-седмично рандомизирано, двойно-сляпо контролирано проучване на 245 mg тенофовир дизопроксил (като фумарат) при възрастни пациенти, коинфектирани с HIV-1 и хроничен хепатит В с предишно лечение с ламивудин (ACTG проучване 5127), средните плазмени нива на изходното ниво на HBV ДНК при пациенти, рандомизирани в рамото на тенофовир, е 9.45 log копия / mL (n = 27). Лечението с 245 mg тенофовир дизопроксил (като фумарат) е свързано със средна промяна от изходното ниво на серумната HBV ДНК от -5,74 log 10 копия / ml (n = 18). Освен това е установено, че 61% от пациентите имат нормални нива на ALT на 48 -та седмица.
Опит при пациенти с персистираща вирусна репликация (проучване GS-US-174-0106)
Ефикасността и безопасността на тенофовир дизопроксил 245 mg (като фумарат) или тенофовир дизопроксил 245 mg (като фумарат) плюс 200 mg емтрицитабин е оценена в рандомизирано, двойно-сляпо проучване (проучване GS-US-174-0106). В HBeAg положителни и HBeAg отрицателни възрастни пациенти с персистираща виремия (HBV ДНК ≥ 1000 копия / ml) по време на лечение с 10 mg адефовир дипивоксил за повече от 24 седмици.В изходното ниво 57% от пациентите са рандомизирани на тенофовир дизопроксил в групата фумарат срещу 60% от пациентите рандомизирани в групата с емтрицитабин плюс тенофовир дизопроксил фумарат, преди това са били лекувани с ламивудин.Като цяло на 24 седмици, лечението с тенофовир дизопроксил фумарат води до 66% (35/53) от пациентите с HBV ДНК
Опит при пациенти с декомпенсирано чернодробно заболяване след 48 седмици (проучване GS-US-174-0108)
Изследване GS-US-174-0108 е рандомизирано, двойно-сляпо, контролирано проучване за оценка на безопасността и ефикасността на тенофовир дизопроксил фумарат (n = 45), емтрицитабин плюс тенофовир дизопроксил фумарат (n = 45) и ентекавир (n = 22), при пациенти с декомпенсирано чернодробно заболяване.В рамото на лечение с тенофовир дизопроксил фумарат пациентите са имали среден CPT резултат от 7,2, средни нива на HBV ДНК от 5,8 log копия / ml и средни плазмени нива ALT от 61 U / I в началото Четиридесет и два процента (19/45) от пациентите са имали поне шест месеца предишно лечение с ламивудин, 20% (9/45) преди това са били лекувани с адефовир дипивоксил, а 9 процента 45 пациенти (20%) са имали резистентни мутации свързани с ламивудин и / или адефовир дипивоксил в началото. Съпътстващите цели за безопасност бяха прекратяване поради нежелано събитие и потвърдено повишаване на плазмения креатинин ≥ 0,5 mg / dl или потвърдената стойност на серумния фосфат
При пациенти с CPT резултат ≤ 9, 74% (29/39) от групата на тенофовир дизопроксил фумарат и 94% (33/35) от групата на емтрицитабин плюс тенофовир дизопроксил фумарат постигат нива на HBV ДНК
Като цяло данните от това проучване са твърде ограничени, за да се направят категорични заключения за сравнението между емтрицитабин + тенофовир дизопроксил фумарат. срещу тенофовир дизопроксил фумарат (вж. Таблица 8 по -долу).
Таблица 8: Параметри на безопасност и ефикасност при декомпенсирани пациенти на 48 седмица
в стойност стр сравнение на комбинираните рамена, съдържащи тенофовир срещу рамото на ентекавир = 0,622,
b стойност стр сравнение на комбинираните рамена, съдържащи тенофовир срещу рамото на ентекавир = 1000.
Опит над 48 седмици в проучване GS-US-174-0108
В „анализ, базиран на уравнения“, субекти, които не са завършили лечението/които са променили лечението = неуспех ”, 50% (21/42) от субектите, които са получавали тенофовир дизопроксил фумарат, 76% (28/37) от пациентите, получавали емтрицитабин плюс тенофовир дизопроксил фумарат и 52% (11/21) от пациентите, получавали ентекавир, са постигнали стойности на HBV ДНК
Опит на 96 седмици при пациенти с резистентен към ламивудин HBV (проучване GS-US-174-0121)
Ефикасността и безопасността на 245 mg тенофовир дизопроксил (като фумарат) бяха оценени в рандомизирано, двойно-сляпо проучване (GS-US-174-0121) при HBeAg положителни и HBeAg отрицателни (n = 280) пациенти с чернодробно заболяване. Компенсирано, виремия (HBV ДНК ≥ 1000 IU / mL) и генотипни доказателства за резистентност към ламивудин (rtM & SUP2; 04I / V +/- rtL180M). Само пет са имали свързани с адефовир резистентност мутации в началото. Сто четиридесет и една и 139 възрастни субекти бяха рандомизирани съответно на групите на лечение с тенофовир дизопроксил фумарат и емтрицитабин плюс тенофовир дизопроксил фумарат. Изходните демографски данни бяха сходни между двете групи на лечение: в началото 52,5% от пациентите бяха HBeAg отрицателни, 47,5% бяха HBeAg положителни, средната стойност Нивото на HBV ДНК е съответно 6,5 log копия / mL, а средната ALT е 79 U / L.
След 96 седмици лечение 126 от 141 (89%) субекта, рандомизирани на тенофовир дизопроксил фумарат, са имали HBV ДНК
Клинична резистентност
Четиристотин двадесет и шест HBeAg отрицателни (GS-US-174-0102, n = 250) и HBeAg положителни (GS-US-174-0103, n = 176) пациенти, първоначално рандомизирани на двойно-сляпо лечение с тенофовир дизопроксил фумарат и впоследствие прехвърлени на лечение с открит тенофовир дизопроксил фумарат, бяха оценени за генотипни промени в HBV полимераза от изходното ниво.Генотипни оценки, извършени при всички пациенти с HBV ДНК> 400 копия / mL при 48 (n = 39), 96 (n = 24 ), 144 (n = 6), 192 (n = 5), 240 (n = 4), 288 (n = 6) и 384 (n = 2) седмици на монотерапия с тенофовир дизопроксил фумарат показват, че те не развиват свързани мутации с резистентност към тенофовир дизопроксил фумарат.
Двеста и петнадесет HBeAg отрицателни (GS-US-174-0102, n = 125) и HBeAg положителни (GS-US-174-0103, n = 90) пациенти, първоначално рандомизирани на двойно-сляпо лечение с адефовир дипивоксил и впоследствие прехвърлени на лечение с отворен етикет тенофовир дизопроксил фумарат бяха оценени за генотипни промени в HBV полимераза от изходното ниво.Генотипни оценки, извършени при всички пациенти с HBV ДНК> 400 копия / mL при 48 (n = 16), 96 (n = 5), 144 (n = 1), 192 (n = 2), 240 (n = 1), 288 (n = 1) и 384 (n = 2) седмици на монотерапия с тенофовир дизопроксил фумарат показват, че не се развиват мутации, свързани с резистентност към тенофовир дизопроксил фумарат.
В проучване GS-US-174-0108, 45 пациенти (включително 9 пациенти с резистентни на ламивудин и / или адефовир дипивоксил мутации в началото) са получавали тенофовир дизопроксил фумарат за период до 168 седмици. Генотипни данни от изходните и лекуваните изолати на HBV двойки бяха налични за 6/8 пациенти с HBV ДНК> 400 копия / ml на седмица 48. В тези изолати не бяха идентифицирани аминокиселинни замествания, свързани с резистентност към тенофовир. Дизопроксил фумарат. проведено за 5 пациенти в рамото на тенофовир дизопроксил фумарат след 48 -та седмица. Не са открити аминокиселинни замествания, свързани с резистентност към тенофовир дизопроксил фумарат.
В проучване GS-US-174-0121, 141 пациенти с замествания, свързани с резистентност към ламивудин, в началото са приемали тенофовир дизопроксил фумарат до 96 седмици. Генотипни данни от изходните и лекуваните изолати на HBV двойки са налични за 6 от 9 пациенти с HBV ДНК> 400 копия / mL през последния период на тенофовир дизопроксил фумарат. В тези изолати не са идентифицирани аминокиселинни замествания, свързани с резистентност към тенофовир дизопроксил фумарат.
В едно педиатрично проучване (GS-US-174-0115) 52 пациенти (включително 6 пациенти с мутации на резистентност към ламивудин в началото) са получавали тенофовир дизопроксил фумарат за период до 72 седмици. Генотипни оценки бяха извършени при всички пациенти с HBV ДНК> 400 копия / mL на 48 седмици (n = 6) и 72 седмици (n = 5). В тези изолати не са идентифицирани аминокиселинни замествания, свързани с резистентност към тенофовир дизопроксил фумарат.
Педиатрична популация
ХИВ-1: В проучване GS-US-104-0321, 87 пациенти, заразени с HIV-1, с предишен опит на лечение, на възраст 12 и оптимизиран фонов режим (OBR) за 48 седмици. Поради ограниченията на проучването не е доказана полза от тенофовир дизопроксил фумарат спрямо плацебо въз основа на плазмените нива на HIV-1 РНК на седмица 24. Въпреки това се очаква полза за популацията на юноши въз основа на „екстраполация на данни за възрастни и сравнителна фармакокинетика данни (вж. точка 5.2).
При пациенти, лекувани с тенофовир дизопроксил фумарат или плацебо, средната Z -оценка на BMD на лумбалния гръбначен стълб е съответно -1.004 и -0.809, а средната обща Z -оценка на BMD е съответно -0.866 и -0.584. Средните промени на 48 -та седмица (в края на двойно -сляпата фаза) са -0,215 и -0,165 за ZM резултат на лумбалния гръбначен стълб и -0,254 и -0,179 за общия ZM резултат на BMD в групите с тенофовир. Дизопроксил фумарат и плацебо , съответно. Средната скорост на повишаване на BMD е по -ниска в групата на тенофовир дизопроксил фумарат в сравнение с групата на плацебо. На 48 -та седмица шест юноши в групата на тенофовир дизопроксил фумарат и един юноша в групата на плацебо са имали значително намаляване на КМП на лумбалния гръбначен стълб (определено като> 4% намаление). При 28 пациенти, лекувани в продължение на 96 седмици с тенофовир дизопроксил фумарат, BM -Z -резултатите намаляват с -0,341 за лумбалния гръбначен стълб и -0,458 за цялото тяло.
В проучване GS-US-104-0352, 97 предварително лекувани пациенти на възраст 2 до зидовудин са рандомизирани да заменят ставудин или зидовудин с тенофовир дизопроксил фумарат (n = 48) или да продължат първоначалния режим (n = 49) в продължение на 48 седмици. На 48-та седмица 83% от пациентите в групата на лечение с тенофовир дизопроксил фумарат и 92% от пациентите в групата на лечение със ставудин или зидовудин са имали концентрации на HIV-1 РНК.
Съобщава се за намаление на КМП при педиатрични пациенти. При пациенти, лекувани с тенофовир дизопроксил фумарат или със ставудин или зидовудин, средната Z -оценка на BMD на лумбалния гръбначен стълб е съответно -1.034 и -0.498, а средният общ Z -резултат на BMD е -0.471 и -0.386 в началото. Средните промени на 48 -та седмица (в края на рандомизираната фаза) са 0,032 и 0,087 за Z -скора на BMD на лумбалния гръбнак и -0,184 и -0,027 за общата Z -оценка на BMD в групите съответно с тенофовир дизопроксил фумарат. И ставудин или зидовудин. . Средната честота на нарастване на костите в лумбалния гръбначен стълб на 48 -та седмица е сходна в групата на тенофовир дизопроксил фумарат и в групата на ставудин или зидовудин. Увеличаването на общата костна тъкан е по -малко в групата на тенофовир дизопроксил фумарат в сравнение със групата на ставудин или зидовудин. лумбален гръбначен стълб на 48 -та седмица. При 64 пациенти, лекувани в продължение на 96 седмици с тенофовир дизопроксил фумарат, BM -Z -резултатите намаляват с -0,012 за лумбалния гръбначен стълб и с -0,338 за цялото тяло, те са коригирани спрямо теглото и ръста.
В проучване GS-US-104-0352 4 от 89 педиатрични пациенти, изложени на тенофовир дизопроксил фумарат, са прекратили лечението поради нежелани реакции, съответстващи на проксималната бъбречна тубулопатия (средна експозиция на тенофовир дизопроксил фумарат: 104 седмици).
Хроничен хепатит В: В проучване GS-US-174-0115, 106 HBeAg отрицателни и HBeAg позитивни пациенти на възраст 12 и интерферон (> 6 месеца преди скрининга) или всяка друга анти-HBV перорална нуклеозидна / нуклеотидна терапия, която не съдържа тенофовир дизопроксил фумарат (> 16 седмици преди скрининга). На 72-та седмица общо 88% (46/52) от пациентите в групата на тенофовир дизопроксил фумарат и 0% (0/54) от пациентите в групата на плацебо са имали 1,5 пъти стойности на HBV ДНК в сравнение с „ULN) на групата на тенофовир дизопроксил фумарат и 0% (0/32) от пациентите в групата на плацебо са имали стойности на HBV ДНК
Нито един пациент не е постигнал основната крайна точка за безопасност от 6% намаление на КМП в лумбалния гръбначен стълб. При пациенти, лекувани с тенофовир дизопроксил фумарат или плацебо, средната (SD) лумбална ZM оценка на лумбалния гръбначен стълб е съответно -0,43 и -0,28 и средната общата Z -оценка на BMD е била -0.20 и -0.26, съответно, в изходно състояние.от изходното ниво до 72 -та седмица е -0.05 при пациенти, лекувани с тенофовир дизопроксил фумарат и 0.07 при пациенти, които са получавали плацебо. Средната промяна в общата Z -оценка на BMD е -0,15 при лекувани пациенти с тенофовир дизопроксил фумарат и 0,06 при пациенти, които са получавали плацебо. Средното процентно увеличение на общата КМП и лумбалния гръбначен стълб от изходното ниво до 72 -ма седмица е съответно 2,84% и 4,95% при пациенти, лекувани с тенофовир дизопроксил фумарат. съответно в сравнение с пациентите, получавали плацебо.Три пациенти в групата на тенофовир дизопроксил фумарат и 2 пациенти в групата на плацебо са имали> 4% намаление на МПК на гръбначния стълб.
Европейската агенция по лекарствата отложи задължението да представи резултатите от проучванията с Viread в една или повече подгрупи от педиатричната популация при ХИВ и хроничен хепатит В (вж. Точка 4.2 за информация относно педиатричната употреба).
05.2 Фармакокинетични свойства
Тенофовир дизопроксил фумарат е водоразтворимо естерно пролекарство, което се превръща бързо in vivo в тенофовир и формалдехид.
В клетката тенофовир се превръща в тенофовир монофосфат и активният компонент тенофовир дифосфат.
Абсорбция
След перорално приложение на тенофовир дизопроксил фумарат при пациенти, заразени с HIV, това съединение се абсорбира бързо и се превръща в тенофовир. Многократното приложение на тенофовир дизопроксил фумарат по време на хранене на HIV-инфектирани пациенти води до средни (% CV) стойности на Cmax, AUC и Cmin на тенофовир от 326 (36.6%) ng / ml, съответно 3 324 (41), 2 %) ng • h / ml и 64.4 (39.4%) ng / ml. Максимални концентрации на тенофовир се наблюдават в серума в рамките на 1 час след гладуване и в рамките на 2 часа след приемане с храна.Оралната бионаличност на тенофовир от тенофовир дизопроксил фумарат при гладни пациенти е приблизително 25%. бионаличност, което води до повишаване на AUC на тенофовир от приблизително 40% и Cmax от приблизително 14%. След първото приложение на тенофовир дизопроксил фумарат на пациенти след хранене, средната серумна Cmax варира от 213 до 375 ng / ml.
Разпределение
След интравенозно приложение, равновесният обем на тенофовир се оценява на приблизително 800 ml / kg. След перорално приложение на тенофовир дизопроксил фумарат, тенофовир се разпределя в повечето тъкани, с повишени концентрации в бъбреците, черния дроб и чревното съдържание (предклинични проучвания). В диапазона на концентрация на тенофовир от 0,01 до 25 mcg / ml, инвитро на плазмата на тенофовир или серумния протеин е съответно по -малко от 0,7 и 7,2%.
Биотрансформация
Проучвания инвитро установено, че нито тенофовир дизопроксил фумарат, нито тенофовир са субстрати за ензимите CYP450. Освен това, при концентрации, значително по -високи (около 300 пъти) от наблюдаваните in vivo, тенофовир не инхибира инвитро лекарствен метаболизъм, медииран от една от основните човешки CYP450 изоформи, участващи в биотрансформацията на лекарството (CYP3A4, CYP2D6, CYP2C9, CYP2E1 или CYP1A1 / 2). При концентрации от 100 μmol / l тенофовир дизопроксил фумарат не оказва влияние върху изоформите на CYP450, с изключение на CYP1A1 / 2, където е отбелязано леко (6%), но статистически значимо намаляване на метаболизма на CYP1A1 / субстрата. Въз основа на тези данни са малко вероятни клинично значими взаимодействия между тенофовир дизопроксил фумарат и лекарствени продукти, метаболизирани чрез CYP450.
Елиминиране
Тенофовир се елиминира главно чрез бъбреците както чрез филтрация, така и чрез активна тръбна транспортна система, като приблизително 70-80% от дозата се екскретира непроменена в урината след интравенозно приложение. Общият клирънс се оценява на около 230 ml. / Час / kg (около 300 бъбречен клирънс е оценен около 160 ml / час / кг (около 210 ml / min), стойност по -висока от скоростта на гломерулната филтрация. че активната тубулна секреция е важен елемент при елиминирането на тенофовир. След перорално приложение терминалният полуживот на тенофовир е приблизително 12-18 часа.
Проучванията идентифицират пътя на активната тубулна секреция на тенофовир, който навлиза в проксималните тубуларни клетки чрез транспортьори на органични аниони на човека 1 и 3 и се влива в урината чрез мултирезистентни протеини 4 (MRP 4).
Линейност / Нелинейност
В диапазона на дозите от 75 до 600 mg, фармакокинетичните свойства на тенофовир не зависят от дозата тенофовир дизопроксил фумарат и всякакви повторни дози не ги повлияват.
Възраст
Фармакокинетични проучвания при възрастни хора (над 65 години) все още не са провеждани.
Секс
Ограничените налични данни за фармакокинетиката на тенофовир при жени не показват важен ефект по отношение на пола.
Етническа принадлежност
Фармакокинетиката при различни етнически групи не е проучена специално.
Педиатрична популация
ХИВ-1: Стационарната фармакокинетика на тенофовир е анализирана при 8 юноши (на възраст от 12 до
Таблица 9: Средни (± SD) фармакокинетични параметри на тенофовир във връзка с възрастовата група при педиатрични пациенти
Хроничен хепатит В: Стационарна експозиция на тенофовир, постигната при юноши (на възраст от 12 до
Фармакокинетични проучвания все още не са провеждани при деца на възраст под 2 години.
Бъбречна недостатъчност
Фармакокинетичните параметри на тенофовир са определени след прилагане на единична доза тенофовир дизопроксил 245 mg на 40 възрастни пациенти, неинфектирани с HIV и HBV, с различна степен на бъбречно увреждане, определено от креатининовия клирънс (CrCl) при възрастни (нормална бъбречна функция, когато CrCl> 80 ml / min; средно с CrCl = 50-79 mL / min; умерено с CrCl = 30-49 mL / min и тежко с CrCl = 10-29 mL / min). В сравнение с пациенти с нормална бъбречна функция, средната концентрация (%CV) се е увеличила от 2185 (12%) ng • h / ml при лица с CrCl> 80 ml / min до 3064 (30%) ng • h / ml, 6,009 ( 42%) ng • h / ml и 15,985 (45%) ng • h / ml съответно при пациенти с леко, умерено и тежко бъбречно увреждане.
Фармакокинетични модели, разработени от фармакокинетични данни за еднократна доза при възрастни пациенти, неинфектирани с HIV и HBV, с различни нива на бъбречно увреждане, бяха използвани за да се направят препоръки за дозата и диапазоните на дозиране за възрастни пациенти с различни нива на бъбречно увреждане (вж. Точка 4.2).
За възрастни пациенти с изчислен креатининов клирънс (CrCl) 30-49 ml / min, 20-29 ml / min или 10-19 ml / min се препоръчват дози съответно 132 mg, 65 mg и 33. mg tenofovir гранули дизопроксил (като фумарат) веднъж дневно. Въпреки че не се очаква тези дози да отразяват точно фармакокинетичния профил на тенофовир при пациенти с нормална бъбречна функция, лекувани с тенофовир дизопроксил (като фумарат) 245 mg филмирани таблетки, се приема, че те представляват най-доброто съотношение полза / риск за пациенти с увреждане бъбречна.
При пациенти с краен стадий на бъбречна недостатъчност (краен стадий на бъбречно заболяване, ESRD) (CrCl
Фармакокинетиката на тенофовир при нехемодиализни пациенти с креатининов клирънс перитонеална диализа или други форми на диализа не е проучена.
Фармакокинетиката на тенофовир при педиатрични пациенти с бъбречно увреждане не е проучена. Няма налични данни за препоръчване на дозата (вж. Точки 4.2 и 4.4).
Еднократна доза от 245 mg тенофовир дизопроксил се прилага на възрастни пациенти, неинфектирани с HIV и HBV, с различна степен на чернодробно увреждане, както е определено от класификацията на Child-Pugh-Turcotte (CPT). Фармакокинетиката на тенофовир не се променя съществено при лица с чернодробно увреждане, което предполага, че не се налага коригиране на дозата при тези лица. Средното (% CV) на Cmax и AUC0-? на тенофовир е 223 (34.8%) ng / mL и 2050 (50.8%) ng • h / mL при съответните нормални индивиди, съответно 289 (46.0%) ng / mL и 2310 (43, 5%) ng • h / ml mL при лица с умерено чернодробно увреждане и 305 (24.8%) ng / mL и 2740 (44.0%) ng • h / mL при лица с тежко чернодробно увреждане.
При хората, в непролифериращи мононуклеарни клетки от периферна кръв (PBMCs), е установено, че полуживотът на тенофовир дифосфат е около 50 часа, докато полуживотът на фитохемаглутинин-стимулирани РВМС е около 10 часа.
05.3 Предклинични данни за безопасност
Неклинични проучвания на фармакология за безопасност не разкриват особен риск за хората. Костната токсичност е диагностицирана като остеомалация (при маймуни) и намалена костна минерална плътност (BMD) (при плъхове и кучета). При плъхове и млади възрастни кучета костна токсичност се проявява при експозиции ≥ 5 пъти по -високи от експозицията на педиатрични или възрастни пациенти; при заразени млади маймуни, костна токсичност се проявява при много високи експозиции след подкожно приложение (≥ 40 пъти l "експозиция на пациент). Резултатите от проучвания при плъхове и маймуни предполагат свързано с веществото намаляване на чревната абсорбция на фосфати, с потенциално вторично намаляване на КМП.
Изследванията на генотоксичността дават положителни резултати от теста инвитро върху миши лимфом двусмислени резултати в един от щамовете, използвани в теста на Ames и слабо положителни резултати в USD тест в първични хепатоцити на плъхове. Въпреки това, той е отрицателен при индуцирането на мутации в тест за микроядра на костен мозък на мишка. in vivo.
Чернодробно увреждане
Вътреклетъчна фармакокинетика
Оралните проучвания за канцерогенност при плъхове и мишки показват ниска честота на дуоденални тумори при изключително висока доза при мишки. Малко вероятно е тези тумори да са от значение за хората.
Проучванията за репродуктивна токсичност, проведени при плъхове и зайци, не показват ефект върху чифтосването, плодовитостта, бременността или параметрите на плода. Въпреки това, в проучвания за пери и постнатална токсичност тенофовир дизопроксил фумарат намалява жизнеспособността и теглото на малките при токсични дози за майката.
Активното вещество тенофовир дизопроксил фумарат и неговите основни продукти на трансформация продължават да съществуват в околната среда.
06.0 ФАРМАЦЕВТИЧНА ИНФОРМАЦИЯ
06.1 Помощни вещества
Етилцелулоза (E462)
Хидроксипропилцелулоза (E463)
Манитол (E421)
Силициев диоксид (E551)
06.2 Несъвместимост
Не е от значение.
06.3 Срок на валидност
3 години.
06.4 Специални условия на съхранение
Да не се съхранява над 25 ° C.
06.5 Естество на непосредствената опаковка и съдържанието на опаковката
Бутилка от полиетилен с висока плътност (HDPE) с полипропиленово затваряне, защитено от деца, съдържащо 60 g гранули и мерителна чашка.
06.6 Инструкции за употреба и боравене
Неизползваното лекарство и отпадъците, получени от това лекарство, трябва да се изхвърлят в съответствие с местните разпоредби.
07.0 Притежател на разрешението за търговия
Gilead Sciences International Limited
Кеймбридж
CB21 6GT
Великобритания
08.0 НОМЕР НА РАЗРЕШЕНИЕТО ЗА УПОТРЕБА
EU/1/01/200/003
035565035
09.0 ДАТА НА ПЪРВО РАЗРЕШЕНИЕ ИЛИ ПОДНОВЯВАНЕ НА РАЗРЕШЕНИЕТО
Дата на първо разрешаване: 5 февруари 2002 г.
Дата на последното подновяване: 14 декември 2011 г.
10.0 ДАТА НА ПРЕГЛЕД НА ТЕКСТА
05/2015
11.0 ЗА РАДИОЛЕКАТИ, ПЪЛНИ ДАННИ ЗА ВЪТРЕШНАТА ДОЗИМЕТРИЯ НА РАДИАЦИЯТА
12.0 ЗА РАДИОЛЕКАТИ, ДОПЪЛНИТЕЛНИ ПОДРОБНИ ИНСТРУКЦИИ ЗА ПЪРВИЧНА ПОДГОТОВКА И КОНТРОЛ НА КАЧЕСТВОТО