Активни съставки: Менингококова конюгирана ваксина от групи A, C, W135 и Y
Прах и разтвор за инжекционен разтвор (прах и инжекционен разтвор).
Защо Menveo се използва? За какво е?
Menveo е ваксина, използвана за активна имунизация на деца (на възраст от 2 години), юноши (на възраст от 11 години) и възрастни, изложени на риск от излагане на серогрупи A, C, W135 и Y на бактерия, наречена Neisseria meningitidis за да се предотврати появата на инвазивни заболявания. Ваксината действа, като задейства защита (антитела) срещу тези бактерии в организма.
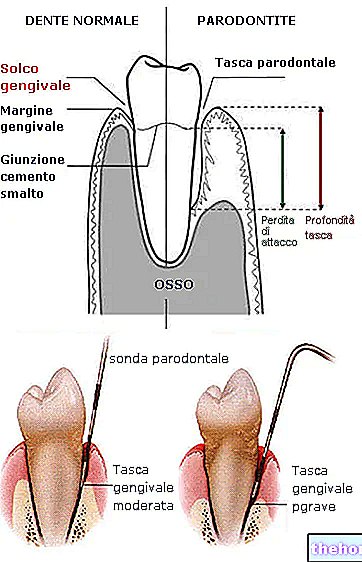
Бактериите Neisseria meningitidis от групи A, C, W135 и Y могат да причинят сериозни и понякога животозастрашаващи инфекции като менингит и сепсис (кръвно отравяне).
Menveo не може да причини бактериален менингит. Ваксината съдържа протеин (наречен CRM197) от бактерията, причиняваща дифтерия. Menveo не предпазва от дифтерия. Това означава, че вие (или вашето дете) ще трябва да направите други ваксинации, за да се предпазите от дифтерия, когато това е необходимо или препоръчано от Вашия лекар.
Противопоказания Когато Menveo не трябва да се използва
Не използвайте Menveo, ако лицето трябва да бъде ваксинирано
- сте имали алергична реакция към активните вещества или който и да е компонент на тази ваксина (изброени в раздел 6)
- сте имали алергична реакция към дифтериен токсоид (вещество, използвано в няколко други ваксини)
- има заболяване с висока температура. Леко фебрилно събитие и / или „инфекция на горните дихателни пътища (например настинка)“ сами по себе си не са достатъчна причина за отлагане на ваксинацията.
Предпазни мерки при употреба Какво трябва да знаете, преди да приемете Menveo
Уведомете Вашия лекар или медицинска сестра, преди да получите Menveo, ако лицето, което ще бъде ваксинирано, има
- отслабена имунна система. Има малко данни за ефективността на Menveo, дадени на хора, чиято имунна система е отслабена поради употребата на имуносупресивни лекарства, HIV инфекция и други възможни причини.Ефективността на Menveo може да бъде намалена при тези хора.
- хемофилия или друг проблем, който може да спре правилното съсирване на кръвта, например при пациенти, приемащи антикоагуланти.
В отговор на всяка инжекция с игла може да възникне припадък, чувство на слабост или други реакции, свързани със стреса. Говорете с Вашия лекар или медицинска сестра, ако преди сте имали такъв тип реакция.
Тази ваксина може да предпази само от бактерии от менингококова група А, С, W135 и Y. Тя не може да предпази от други видове менингококови бактерии, различни от групи А, С, W135 и Y или други фактори, които причиняват менингит и сепсис (кръвно отравяне).
Както при другите ваксини, Menveo може да не защити 100% от тези, които получават ваксината.
Възможно е да се разгледа хипотезата за прилагане на бустер доза за поддържане на защита, ако ваксинираното лице е получило доза Menveo за повече от година и все още е изложено на особен риск от излагане на менингококова бактерия от група А. Лекарят ще Ви посъветва дали и кога да получите бустер доза.
Взаимодействия Кои лекарства или храни могат да променят ефекта на Menveo
Уведомете Вашия лекар или медицинска сестра, ако приемате, наскоро сте приемали или е възможно да приемете други лекарства.
Menveo може да се прилага едновременно с други ваксинации, но за предпочитане е всякакви други ваксини да се инжектират в ръка, различна от мястото на инжектиране на Menveo.
Те включват: ваксина срещу дифто-тетанус-ацелуларен коклюш (Tdap), ваксина срещу човешки папиломен вирус (HPV), ваксина срещу жълта треска, ваксина срещу коремен тиф (полизахарид Vi), ваксина срещу японски енцефалит, ваксина срещу бяс и ваксина срещу хепатит А и В.
Действието на Menveo може да бъде намалено, ако се дава на хора, приемащи лекарства за инхибиране на имунната система.
Ако се инжектират няколко ваксини едновременно, трябва да се използват отделни места за инжектиране.
Предупреждения Важно е да знаете, че:
Бременност, кърмене и фертилитет
Уведомете Вашия лекар, преди да приемете това лекарство, ако сте бременна, кърмите, подозирате бременност или планирате да забременеете. Вашият лекар или медицинска сестра обаче могат да препоръчат Menveo, ако рискът от инфекция с менингококови бактерии от групи А, С, W-135 и Y е висок.
Шофиране и работа с машини
Не са провеждани проучвания за способността за шофиране и работа с машини. Много редки са съобщени случаи на замаяност след ваксинацията. Способността за шофиране и работа с машини може временно да бъде нарушена.
Menveo съдържа
Това лекарство съдържа по-малко от 1 mmol натрий (23 mg) на доза и поради това е по същество „без натрий“.
Това лекарство съдържа по-малко от 1 mmol калий (39 mg) на доза и поради това е по същество „без калий“.
Дозировка и начин на употреба Как да използвате Menveo: Дозировка
Menveo ще бъде даден на Вас или Вашето дете от лекар или медицинска сестра.
Обикновено ваксината се инжектира в мускула на горната част на ръката (делтоид) при деца (от 2 -годишна възраст), юноши и възрастни. Вашият лекар или медицинска сестра ще внимават да не инжектират ваксината в кръвоносен съд и ще проверят дали тя е инжектирана в мускула, а не в кожата.
За деца (от 2 -годишна възраст), юноши и възрастни: ще се приложи еднократна инжекция (0,5 ml).
Безопасността и ефикасността на Menveo при деца на възраст под 2 години все още не са установени.
Уведомете Вашия лекар, ако преди това сте получили "инжекция с Menveo или друга менингококова ваксина. Вашият лекар ще Ви каже дали имате нужда от друга" инжекция с Menveo.
За информация относно разтварянето на ваксината вижте раздела за Вашия лекар или медицински специалист в края на тази листовка.
Ако имате допълнителни въпроси относно употребата на това лекарство, попитайте Вашия лекар или медицинска сестра.
Странични ефекти Какви са страничните ефекти на Menveo
Както всички лекарства, това лекарство може да предизвика нежелани реакции, въпреки че не всеки ги получава.
Най -честите нежелани реакции, съобщени по време на клиничните изпитвания, обикновено са продължили само от един ден до два дни и като цяло не са сериозни.
При деца (на възраст 2-10 години) нежеланите реакции, съобщени по време на клиничните изпитвания, са изброени по-долу.
Много чести (могат да засегнат повече от 1 на 10 души): сънливост, главоболие, раздразнителност, общо неразположение, болка на мястото на инжектиране, зачервяване на мястото на инжектиране (≤50 mm), инжектиране на мястото на инжектиране (≤50 mm)
Чести (могат да засегнат до 1 на 10 души): промяна в хранителните навици, гадене, повръщане, диария, обрив, мускулни болки, болки в ставите, втрисане, треска ≥38 ° C, зачервяване на мястото на инжектиране (> 50 mm) и втвърдяване на мястото на инжектиране (> 50 mm)
Нечести (могат да засегнат до 1 на 100 души): сърбеж на мястото на инжектиране
При юноши (на възраст над 11 години) и възрастни най -честите нежелани реакции, съобщени по време на клиничните изпитвания, са изброени по -долу.
Много чести: главоболие, гадене, болка на мястото на инжектиране, зачервяване на мястото на инжектиране (≤50 mm), индукция на мястото на инжектиране (≤50 mm), мускулна болка, общо неразположение
Чести: обрив, зачервяване на мястото на инжектиране (> 50 mm), индукция на мястото на инжектиране (> 50 mm), болки в ставите, треска ≥38 ° C, втрисане
Нечести: замаяност, сърбеж на мястото на инжектиране
Странични ефекти, които са докладвани, откакто Menveo е на пазара: Алергични реакции, които могат да включват тежко подуване на устните, устата, гърлото (което може да причини затруднено преглъщане), затруднено дишане с хрипове или кашлица, обрив и подуване на ръцете , стъпала и глезени, загуба на съзнание, много ниско кръвно налягане; припадъци (припадъци), включително пристъпи, свързани с треска; нарушения на равновесието; припадък; инфекция на кожата на мястото на инжектиране; подуване на мястото на инжектиране, включително обширно подуване на инжектирания крайник.
Ако получите тежка алергична реакция, незабавно се свържете с Вашия лекар или отидете / заведете детето си в спешното отделение, тъй като може да се нуждае от „спешна медицинска помощ“.
Докладване на странични ефекти
Ако получите някакви нежелани реакции, говорете с Вашия лекар, фармацевт или медицинска сестра. предоставете повече информация за безопасността на това лекарство.
Срок на годност и задържане
Съхранявайте това лекарство на място, недостъпно за деца.
Не използвайте това лекарство след срока на годност, отбелязан върху картонената опаковка и флакона след указанието Годен до: Срокът на годност се отнася до последния ден от месеца.
Съхранявайте в хладилник (2 ° C - 8 ° C). Не замразявайте. Съхранявайте флаконите във външната опаковка, за да предпазите лекарството от светлина.
Продуктът трябва да се използва веднага след разтваряне. Въпреки това, физико-химичната стабилност е доказана в продължение на 8 часа след разтваряне при температура под 25 ° С.
Лекарствата не трябва да се изхвърлят чрез отпадъчни води или битови отпадъци. Вашият лекар или медицинска сестра ще организира изхвърлянето на лекарството. Това ще помогне за опазването на околната среда.
Краен срок "> Друга информация
Какво съдържа Menveo
Една доза (0,5 ml разтворена ваксина) съдържа:
Активните съставки са:
- първоначално се съдържа в праха
- менингококова група А олигозахарид 10 микрограма, конюгирани с протеина Corynebacterium diphtheriae CRM197 16,7 до 33,3 микрограма
- първоначално се съдържа в разтвора
- Менингококов олигозахарид от група C 5 микрограма, конюгиран с Corynebacterium diphtheriae CRM197 протеин 7,1 до 12,5 микрограма
- менингококова група W135 олигозахарид 5 микрограма, конюгирани с протеина Corynebacterium diphtheriae CRM197 от 3,3 до 8,3 микрограма
- Менингококов олигозахарид от група Y 5 микрограма, конюгиран с протеин Corynebacterium diphtheriae CRM197 5,6 до 10,0 микрограма
Другите съставки (помощни вещества) са:
В праха: едноосновен калиев фосфат и захароза.
В разтвора: натриев хлорид, натриев дихидроген фосфат монохидрат, натриев хидроген фосфат дихидрат и вода за инжекции (вж. Също края на раздел 2).
Описание на това как изглежда Menveo и съдържанието на опаковката
Menveo е прах и инжекционен разтвор.
Всяка доза Menveo се предоставя като:
- 1 флакон, съдържащ лиофилизиран конюгиран компонент MenA като бял до почти бял прах;
- 1 флакон, съдържащ течния конюгиран компонент MenCWY като бистър разтвор;
- Размер на опаковката от една доза (2 флакона) или пет дози (10 флакона).
Не всички видове опаковки могат да бъдат пуснати на пазара.
Съдържанието на двата компонента (флакон и флакон) трябва да се смеси преди ваксинацията, за да се получи 1 доза от 0,5 ml.
Източник на листовката: AIFA (Италианска агенция по лекарствата). Съдържание, публикувано през януари 2016 г. Наличната информация може да не е актуална.
За да имате достъп до най-актуалната версия, препоръчително е да получите достъп до уебсайта на AIFA (Италианска агенция по лекарствата). Отказ от отговорност и полезна информация.
01.0 ИМЕ НА ЛЕКАРСТВЕНИЯ ПРОДУКТ -
ПО -малко прах и разтвор за разтвор за инжектиране
СЪЕДИНЕНА МЕНИНГОКОККАЛНА ВАКСИНА ОТ ГРУПА A, C, W135 И Y
02.0 КАЧЕСТВЕН И КОЛИЧЕСТВЕН СЪСТАВ -
Една доза (0,5 ml разтворена ваксина) съдържа:
(първоначално се съдържа в праха)
• 10 mcg менингококов олигозахарид от група А, конюгиран с протеина Corynebacterium diphtheriae CRM197 от 16,7 до 33,3 мкг (първоначално се съдържа в разтвора)
• олигозахарид на менингококова група С 5 mcg, конюгиран с протеина Corynebacterium diphtheriae CRM197 от 7,1 до 12,5 мкг
• олигозахарид от менингококовата група W135 5 mcg, конюгиран с протеина Corynebacterium diphtheriae CRM197 от 3.3 до 8.3 mcg
• 5 mcg менингококова олигозахарид от група Y, конюгиран с протеина Corynebacterium diphtheriae CRM197 от 5,6 до 10,0 мкг
За пълния списък на помощните вещества вижте точка 6.1.
03.0 ЛЕКАРСТВЕНА ФОРМА -
Прах и разтвор за инжекционен разтвор (прах и инжекционен разтвор).
Прахът е бял до почти бял агломерат.
Разтворът е бистър и безцветен.
04.0 КЛИНИЧНА ИНФОРМАЦИЯ -
04.1 Терапевтични показания -
Menveo е показан за активна имунизация на деца (на 2 години и по -големи), юноши и възрастни с риск от експозиция на групи А, С, W135 и Y от Neisseria meningitidis за да се предотврати появата на инвазивни заболявания.
Употребата на тази ваксина трябва да е в съответствие с официалните препоръки.
04.2 Дозировка и начин на приложение -
Дозировка
Деца (на 2 години и повече), тийнейджъри и възрастни
Menveo трябва да се прилага като единична доза (0,5 ml).
За да се осигурят оптимални нива на антитела срещу всички серогрупи ваксини, графикът на първичната ваксинация с Menveo трябва да бъде завършен един месец преди риска от излагане на Neisseria meningitidis групи A, C, W135 и Y; бактерицидни антитела (hSBA≥1: 8) са наблюдавани при поне 64% от пациентите 1 седмица след ваксинацията (вж. точка 5.1 за данни за имуногенността за отделни серогрупи).
Възрастни граждани
Данните за субекти на възраст 56-65 години са ограничени, а данни за лица на възраст> 65 години не са налични.
Бустер ваксинация
Налични са данни за дългосрочна персистираност на антителата след ваксинация с Menveo до 5 години (вж. Точки 4.4 и 5.1).
Menveo може да се прилага като бустер доза при лица, които преди това са получили първична ваксинация с Menveo, друга менингококова конюгирана ваксина или менингококова полизахаридна неконюгирана ваксина. Необходимостта и времето за повишаване на дозата при лица, предварително ваксинирани с Menveo, трябва да се определят съгласно националните препоръки.
Педиатрична популация (на възраст под 2 години)
Безопасността и ефикасността на Menveo при деца на възраст под 2 години все още не са установени. Понастоящем наличните данни са описани в точка 5.1, но не могат да се направят препоръки относно дозировката.
Начин на приложение
Menveo се прилага чрез инжектиране в мускул, за предпочитане в делтоиден мускул.
Не трябва да се прилага интраваскуларно, подкожно или интрадермално.
Трябва да се използват отделни места за инжектиране за прилагане на повече от една ваксина едновременно.
За инструкции за приготвяне и разтваряне на лекарствения продукт преди приложение вижте точка 6.6.
04.3 Противопоказания -
Свръхчувствителност към активното вещество или към някое от помощните вещества, изброени в точка 6.1, или към дифтериен токсоид (CRM197), или животозастрашаваща реакция след предишно приложение на ваксина, съдържаща подобни компоненти (вж. Точка 4.4).
Както при другите ваксини, приложението на Menveo трябва да се отложи при лица, страдащи от остро тежко фебрилно събитие. Наличието на лека инфекция не е противопоказание.
04.4 Специални предупреждения и подходящи предпазни мерки при употреба -
Преди да инжектира каквато и да е ваксина, лицето, отговорно за прилагането, трябва да вземе всички известни предпазни мерки, за да предотврати алергични или други реакции, включително събиране на информация за медицинската история на пациента и текущото здравословно състояние. Както при всички ваксини. Инжекциите, подходящо медицинско лечение и надзор винаги трябва да бъдат лесно достъпни в редки случаи на анафилактични реакции след прилагане на ваксината.
Реакции, свързани с тревожност, включително вазовагални реакции (синкоп), хипервентилация или реакции, свързани със стреса, като психогенен отговор при прилагане на иглата може да възникне във връзка с ваксинацията (вж. Точка 4.8 Нежелани реакции). Ето защо е важно да се прилагат процедури за избягвайте припадъци.
Menveo при никакви обстоятелства не трябва да се прилага интраваскуларно.
Menveo не предпазва от инфекции, причинени от друга серогрупа N. meningitidis не присъства във ваксината.
Както при всички ваксини, защитен имунен отговор може да не се получи при всички ваксини (вж. Точка 5.1).
Проучванията с Menveo показват намаляване на серумните титри на бактерицидни антитела спрямо серогрупа А при използване на човешки комплемент в теста (hSBA) (вж. Точка 5.1).
Клиничното значение на намаляването на титрите на антитела към hSBA на серогрупа А е неизвестно.
Необходимостта от бустер доза трябва да се има предвид, ако се смята, че дадено лице е изложено на особен риск от излагане на MenA и е получавало предишна доза Menveo за повече от година.
Няма данни за приложимостта на ваксината за пост-експозиционна профилактика.
При имунокомпрометирани индивиди ваксинацията може да не доведе до адекватен защитен отговор на антитела. Инфекцията с вируса на човешкия имунодефицит (HIV) не е противопоказание, но Menveo не е специално оценяван при хора с имунен дефицит. Лица с дефицит на комплемент и лица с анатомична или функционална аспления може да не развият имунен отговор към менингококови конюгирани ваксини от група А, С, W135 и Y.
Menveo не е оценяван при хора с тромбоцитопения, нарушения на хемостазата или на антикоагулантно лечение поради риска от хематом. Здравните специалисти трябва да оценят съотношението полза-риск за хората, изложени на риск от образуване на хематом, след интрамускулна инжекция.
04.5 Взаимодействия с други лекарствени продукти и други форми на взаимодействие -
Menveo може да се прилага едновременно с някоя от следните ваксини: едновалентна и комбинирана ваксина срещу хепатит А и В, ваксина срещу жълта треска, ваксина срещу коремен тиф (полизахарид Vi), ваксина срещу японски енцефалит и ваксина срещу бяс.
При юноши (на възраст 11-18 години) Menveo е оценяван в две проучвания за едновременно приложение само с адсорбирана ваксина срещу дифто-тетанус-ацелуларен коклюш (Tdap) или
Tdap и четиривалентна рекомбинантна ваксина срещу папилома вирус (типове 6, 11, 16 и 18) (HPV); и двете проучвания подкрепят съвместното приложение на ваксини.
Няма данни от проучванията за увеличаване на степента на реактогенност или за промяна в профила на безопасност на ваксините. .
Приложението на Menveo един месец след Tdap води до статистически значимо намалени серореакции на серогрупа W135. Тъй като не е регистрирано пряко въздействие върху степента на серопротекция, клиничните последици в момента са неизвестни. Има данни за известно потискане на отговора на антителата към два от трите коклюшни антигена. Клиничното значение на това наблюдение е неизвестно.
След ваксинацията над 97% от пациентите са имали откриваеми коклюшни титри и към трите коклюшни антигена.
При деца на възраст от 2 до 10 години няма налични данни за оценка на безопасността и имуногенността на други детски ваксини, прилагани едновременно с Menveo.
Едновременното приложение на Menveo и други ваксини, различни от изброените по-горе, не е проучено. Съпътстващите ваксини винаги трябва да се прилагат на отделни места за инжектиране, за предпочитане в контралатералните крайници.Трябва да се проучи дали нежеланите реакции могат да бъдат засилени при едновременно приложение.
Ако ваксинираният получава имуносупресивна терапия, имунологичният отговор може да бъде намален.
04.6 Бременност и кърмене -
Няма достатъчно клинични данни за експозиция по време на бременност.
Неклиничните проучвания показват, че Menveo няма преки или косвени вредни ефекти по отношение на бременността, ембрионалното / феталното развитие, раждането или постнаталното развитие. Като се има предвид тежестта на инвазивното менингококово заболяване, причинено от серогрупи A, C, W135 и Y на Neisseria meningitidis, бременността не е пречка за ваксинацията, когато рискът от експозиция е ясно определен.
Въпреки че клиничните данни за употребата на Menveo по време на кърмене не са пълни, малко вероятно е антителата, секретирани в млякото, да представляват опасност, когато се асимилират от кърмаче. Следователно, Menveo може да се използва по време на кърмене.
04.7 Ефекти върху способността за шофиране и работа с машини -
Не са провеждани проучвания за способността за шофиране и работа с машини. Много редки са съобщени случаи на замаяност след ваксинацията. Способността за шофиране и работа с машини може временно да бъде нарушена.
04.8 Нежелани реакции -
В рамките на всеки честотен клас нежеланите реакции се съобщават в низходящ ред по тежест.
Честотата се определя, както следва:
Много чести: (≥ 1/10)
Чести: (≥1 / 100 до
Нечести: (≥ 1/1 000 до
Редки: (≥ 1/10 000 до
Много рядко: (
С неизвестна честота (честотата не може да бъде оценена от наличните данни)
Нежелани реакции, наблюдавани при клинични проучвания
Деца на възраст между 2 и 10 години
Общо 3464 лица на възраст между 2 и 10 години са били изложени на ваксинация с Menveo в завършени клинични изпитвания. Охарактеризирането на профила на безопасност на Menveo при деца на възраст от 2 до 10 години се основава на данни от четири клинични проучвания, в които 3 181 пациенти са получавали Menveo.
Най -честите нежелани реакции по време на клиничните изпитвания обикновено продължават един или два дни и не са сериозни. Нежеланите реакции бяха:
Нарушения на метаболизма и храненето:
Чести: хранителни разстройства
Нарушения на нервната система:
Много чести: сънливост, главоболие
Стомашно -чревни нарушения:
Чести: гадене, повръщане, диария
Нарушения на кожата и подкожната тъкан:
Чести: обрив
Нарушения на мускулно -скелетната система и съединителната тъкан:
Чести: миалгия, артралгия
Общи нарушения и състояния на мястото на приложение:
Много чести: раздразнителност, неразположение, болка на мястото на инжектиране, еритем на мястото на инжектиране (≤ 50 mm), индукция на мястото на инжектиране (≤ 50 mm)
Чести: еритем на мястото на инжектиране (> 50 mm), индукция на мястото на инжектиране (> 50 mm), втрисане, треска ≥38 ° C
Нечести: сърбеж на мястото на инжектиране
Субекти на възраст между 11 и 65 години
Характеристиката на профила на безопасност на Menveo при юноши и възрастни се основава на данни от пет рандомизирани контролирани проучвания с включването на 6401 участници (на възраст от 11 до 65 години), които са получили Menveo.
Menveo принадлежат съответно, в проценти от 58.9%, 16.4%, 21.3%и 3.4%, към следните възрастови групи 11-18 години, 19-34 години, 35-55 години и 56-65 години. Двете основни проучвания за безопасност са рандомизирани и активно контролирани проучвания, в които участват участници съответно на възраст от 11 до 55 (N = 2663) и 19 и 55 години (N = 1606).
Честотата и тежестта на всички локални, системни и други реакции обикновено се припокриват в групите на всички проучвания, лекувани с Menveo и във възрастовите групи на юноши и възрастни. които са получили Menveo (N = 216) са подобни на тези, наблюдавани при пациенти, получавали Menveo на възраст от 11 до 55 години.
Най -честите системни и локални нежелани реакции, наблюдавани в клиничните изпитвания, са: болка на мястото на инжектиране и главоболие.
Представеният по -долу списък представя нежеланите реакции, докладвани в трите основни клинични проучвания и двете поддържащи проучвания, разбити по системо -органни класове. несериозно.
Нарушения на нервната система:
Много чести: главоболие
Нечести: замаяност
Стомашно -чревни нарушения:
Много чести: гадене
Нарушения на кожата и подкожната тъкан:
Чести: обрив
Нарушения на мускулно -скелетната система и съединителната тъкан:
Много чести: миалгия
Чести: артралгия
Общи нарушения и състояния на мястото на приложение:
Много чести: болка на мястото на инжектиране, еритем на мястото на инжектиране (≤50 mm), индукция на мястото на инжектиране (≤50 mm), неразположение
Чести: еритем на мястото на инжектиране (> 50 mm), индурация на мястото на инжектиране (> 50 mm), треска ≥38 ° C, втрисане
Нечести: сърбеж на мястото на инжектиране
В юношеската група безопасността и поносимостта на ваксината са благоприятни по отношение на Tdap и не се променят съществено при едновременно приложение или последващи други ваксини.
Постмаркетингов опит (всички възрастови групи)
Нарушения на имунната система
С неизвестна честота: свръхчувствителност, включително анафилаксия
Нарушения на нервната система
С неизвестна честота: тонични гърчове, фебрилни гърчове, синкоп
Нарушения на ухото и лабиринта
С неизвестна честота: световъртеж
Общи нарушения и състояния на мястото на приложение
С неизвестна честота: целулит на мястото на инжектиране, подуване на мястото на инжектиране, включително обширно подуване на инжектирания крайник
Докладване на предполагаеми нежелани реакции
Съобщаването на предполагаеми нежелани реакции, настъпили след разрешаване на лекарствения продукт, е важно, тъй като позволява непрекъснато проследяване на съотношението полза / риск на лекарствения продукт. От медицинските специалисти се изисква да съобщават всякакви предполагаеми нежелани реакции чрез националната система за докладване. В „Приложение V
04.9 Предозиране -
Не са докладвани случаи на предозиране.
05.0 ФАРМАКОЛОГИЧНИ СВОЙСТВА -
05.1 "Фармакодинамични свойства -
Фармакотерапевтична група: менингококови ваксини.
ATC код: J07AH08.
Имуногенност
Ефикасността на Menveo се извежда чрез измерване на производството на специфични за серогрупата анти-капсулни антитела с бактерицидна активност.Серумната бактерицидна активност (SBA) се измерва, като се използва човешки серум като източник на екзогенен комплемент (hSBA). HSBA е първоначалният корелат на защитата срещу менингококова болест.
Имуногенността се оценява в рандомизирани, многоцентрови, активно контролирани клинични изпитвания, които включват деца (2-10 години), юноши (11-18 години), възрастни (19-55 години) и по-възрастни (56-65 години).
Имуногенност при деца на възраст от 2 до 10 години
В основното проучване V59P20 имуногенността на Menveo е сравнена с тази на ACWY-D; 1170 деца са ваксинирани с Menveo и 1161 са получили сравнителната ваксина в популациите от протокол. В две поддържащи проучвания V59P8 и V59P10 имуногенността на Menveo е сравнена с тази на ACWY-PS.
В основното, рандомизирано, заслепено от наблюдатели проучване V59P20, в което участниците са стратифицирани по възраст (2 до 5 години и 6 до 10 години), имуногенността на единична доза Menveo, един месец по-късно ваксинацията е сравнена с тази на единична доза ACWY-D. Резултатите от имуногенността един месец след ваксинацията с Menveo при лица на възраст от 2 до 5 и от 6 до 10 са обобщени в Таблица 1
Таблица 1: Отговори на серумни бактерицидни антитела след приложение на Menveo един месец след ваксинацията при лица на възраст от 2 до 5 до 6 до 10 години
В друго рандомизирано проучване, заслепено от наблюдатели (V59P8), децата в САЩ са имунизирани с еднократна доза Menveo (N = 284) или ACWY-PS (N = 285). При деца на възраст 2 и 10 години, както и във всяко възрастова стратификация (2-5 и 6-10 години), имунните отговори, измерени като процент от субекти със серореакция, hSBA≥1: 8 и GMT, не само не са по-ниски от сравнителната ваксина ACWY -PS, но те също са всички статистически по-голям от сравнителния за всички серогрупи и всички имунни измервания един месец след ваксинацията.Една година след ваксинацията Menveo остава статистически по-добър от ACWY-PS за серогрупи A, W-135 и Y, измерен като процент от субекти с hSBA≥1 : 8 и GMT.
Menveo не е по-нисък за тези крайни точки за серогрупа С (Таблица 2). Клиничното значение на по-високите пост-ваксинални имунни отговори е неизвестно.
Таблица 2: Имуногенност на доза Menveo или ACWY-PS при лица на възраст от 2 до 10 години, измерена един месец и дванадесет месеца след ваксинацията
В рандомизирано проучване, заслепено от наблюдатели (V59P10), проведено в Аржентина, децата са имунизирани с единична доза Menveo (N = 949) или ACWY-PS (N = 551).
Имуногенността се оценява в подгрупа от 150 пациенти във всяка ваксинална група.
Имунният отговор, наблюдаван при деца на възраст от 2 до 10 години, е много подобен на този, наблюдаван в изследването V59P8, показано по -горе: имунният отговор към Menveo един месец след ваксинацията, измерен като процент от субекти със серореакция, hSBA ≥1: 8 и GMT, не беше по-малко от ACWY-PS.
Проведено е рандомизирано, заслепено от наблюдатели проучване при деца на възраст от 12 до 59 месеца във Финландия и Полша (V59P7) .Общо 199 пациенти на възраст от 2 до 5 години са били в популацията за протокол. За имуногенността на Menveo и 81 пациенти на възраст между 3 и 5 години съставлява групата ACWY-PS.
Един месец след първата ваксинация делът на субектите с hSBA ≥ 1: 8 е значително по -висок в групата Menveo за всичките четири серогрупи (63% срещу 39%, 46% срещу 39%, 78% срещу 59% и 65% % срещу 57 % за Menveo в сравнение с ACWY-PS съответно за серогрупи A, C, W135 и Y).
В рандомизирано проучване, заслепено от наблюдатели (V59_57), проведено в Съединените щати, е сравнена имуногенността на двудозов и еднодозов режим на Menveo при деца на възраст от 2 до 5 до 6 до 10 години (N = 715) .
В началото процентът на субектите с hSBA ≥ 1: 8 в двете възрастови стратификации е 1% -5% за серогрупа А, 13% -28% за серогрупа С, 42% -64% за серогрупа W135 и 6% -19 % за серогрупа Y. Един месец след последната ваксинация процентите на субектите с hSBA ≥ 1: 8 в групата с 2 дози и в групата с еднократна доза в двете възрастови групи са: 90% -95% срещу 76% -80% за серогрупа А, 98% -99% срещу 76% -87% за серогрупа С, 99% срещу 93% -96% за серогрупа W135 и 96% срещу 65% -69% за серогрупа Y. Един месец след ваксинацията , GMTs са били по-високи в групата с 2 дози, отколкото в групата с единична доза и в двете възрастови стратификации; тази разлика обаче е по-слабо изразена в стратификацията на по-възрастната възраст.
Една година след последната ваксинация процентът на субектите с hSBA ≥ 1: 8 след лечение с двудозов и еднодозов режим е по-нисък от този, записан 1 месец след ваксинацията (30% след схемата при 2 дози, 11 % -20% след режим на единична доза за серогрупа А; 61% -81% и 41% -55% за серогрупа С; 92% -94% и 90% -91% за серогрупа W135; 67% -75% и 57 % -65% за серогрупа Y) .Една година след ваксинацията разликите между hSBA GMTs в групите с 2 дози и еднократни дози са по-малки от установените.1 месец след ваксинацията.
Клиничната полза от режим на 2 дози при деца на възраст от 2 до 10 години е неизвестна.
Устойчивост на имунния отговор и отговор на бустер доза при възрастни деца между 2 и 10 години
Устойчивостта на антителата 5 години след първичната ваксинация беше оценена в проучване V59P20E1, разширение на изследването V59P20. Наблюдава се устойчивост на антитела срещу серогрупи C, W135 и Y. Процентите на субектите с hSBA ≥1: 8 са равни на 32% и 56% срещу серогрупа C съответно при лица на възраст между 2 и 5 години и между 6 и 10 години, 74% и 80% срещу серогрупа W135 и 48% и 53% срещу серогрупа Y, с GMTs съответно 6.5 и 12 за серогрупа C, 19 и 26 за серогрупа W135 и 8.13 и 10 за серогрупа Y. За серогрупа А съответно 14% и 22% от субектите на възраст от 2 до 5 и от 6 до 10 години съобщават за hSBA ≥1: 8 (GMT 2.95 и 3.73).
Пет години след първичната ваксинация с единична доза, на децата също беше дадена бустер доза Menveo. Всички субекти и в двете възрастови групи съобщават за hSBA ≥1: 8 за всички серогрупи, като титрите на антителата са няколко пъти по -високи от тези, наблюдавани след първичната ваксинация (Таблица 3).
Таблица 3: Продължителност на имунния отговор 5 години след първичната ваксинация с Menveo и имунен отговор 1 месец след бустер доза при лица на възраст от 2 до 5 години и от 6 до 10 години по време на първата ваксинация
Имуногенност при лица на възраст над 11 години
В основното проучване (V59P13) юноши или възрастни са получили една доза Menveo (N = 2649) или сравнителна ваксина ACWY-D (N = 875). Серумите се събират преди ваксинацията и един месец след ваксинацията.
В друго проучване (V59P6), проведено при 524 юноши, имуногенността на Menveo е сравнена с тази на ACWY-PS.
Имуногенност при подрастващите
В популацията от 11-18 години от основното проучване V59P13 имуногенността на единична доза Menveo един месец след ваксинацията се сравнява с тази на ACWY-D.
Резултатите от имуногенността един месец след приложението на Menveo са обобщени по -долу в Таблица 4.
Таблица 4: Отговори на серумни бактерицидни антитела след приложение на Menveo един месец след ваксинацията при лица на възраст от 11 до 18 години
В подгрупата субекти на възраст от 11 до 18 години, които са били серонегативни в началото (hSBA
В проучването за непълноценност V59P6, имуногенността е оценена при юноши на възраст 11-17 години, които са рандомизирани да получават Menveo или ACWY-PS. Показано е, че Menveo не е по-нисък от ваксината ACWY-PS за всички. И четири серогрупи (A, C, W135 и Y) въз основа на сероотговор, като процентите достигат hSBA ≥1: 8 и GMT.
Таблица 5: Имуногенност на доза Menveo или ACWY-PS при юноши, измерена един месец след ваксинацията
Една година след ваксинацията при същите субекти, в сравнение с ACWY-PS, по-висок процент субекти, ваксинирани с Menveo, имат hSBA ≥1: 8 за серогрупи C, W135 и Y, със сравними нива за серогрупа А. Подобни резултати са наблюдавани при сравнението на hSBA GMT.
Устойчивост на имунния отговор и отговор на бустер доза при юноши
В проучване V59P13E1 е оценена устойчивостта на имунния отговор срещу серогрупи A, C, W135 и Y на 21 месец, 3 години и 5 години след първичната ваксинация при лица на възраст от 11 до 18 години по време на ваксинацията. Процентите на субектите с hSBA ≥1: 8 остават постоянни за антителата срещу серогрупи C, W135 и Y от 21 месеца до 5 години след ваксинацията в групата Menveo, докато този за антителата срещу серогрупа А леко намалява с течение на времето (Таблица 6) . 5 години след първичната ваксинация са наблюдавани значително по-високи проценти от субекти с hSBA ≥1: 8 в групата Menveo в сравнение с контролни субекти, които не са били ваксинирани и за четирите серогрупи.
Таблица 6: Продължителност на имунния отговор приблизително 21 месеца, 3 и 5 години след ваксинацията с Menveo (лица на възраст от 11 до 18 години по време на ваксинацията)
Бустер доза Menveo е приложена 3 години след първичната ваксинация с Menveo или ACWY-D. И двете групи показаха стабилен отговор на бустерната доза Menveo един месец след ваксинацията (100% от пациентите са имали hSBA ≥1: 8 за всички серогрупи) и този отговор продължава до голяма степен през 2 години след бустерната доза за серогрупи C, W135 и Y (87% -100% от пациентите са имали hSBA ≥1: 8 за серогрупи).
Наблюдава се леко намаляване на процентите на субектите с hSBA ≥1: 8 за серогрупа А, въпреки че процентите все още са високи (77% -79%). GMT намаляват с течение на времето, както се очаква, но остават 2 до 8 пъти по-високи от стойностите преди бустер (Таблица 8).
В проучване V59P6E1 една година след ваксинацията процентът на субектите, които са получавали Menveo с hSBA ≥1: 8, остава значително по-висок от тези, които са получавали ACWY-PS за серогрупи C, W135 и Y и по подобен начин между двете проучвани групи за серогрупа A. hSBA GMT за серогрупи W135 и Y са по -високи сред субектите, които са получавали Menveo. 5 години след ваксинацията процентът на субектите, които са получавали Menveo с hSBA ≥1: 8, остава значително по-висок от тези, които са получавали ACWY-PS за серогрупи C и Y. По-високи hSBA GMTs се наблюдават за серогрупи W135 и Y (Таблица 7).
Таблица 7: Продължителност на имунния отговор приблизително 12 месеца и 5 години след ваксинацията с Menveo и ACWY-PS (лица на възраст от 11 до 18 години по време на ваксинацията)
Бустер доза Menveo е дадена 5 години след първичната ваксинация с Menveo или ACWY-PS. 7 дни след бустерната доза 98% -100% от пациентите, които преди това са получавали Menveo и 73% -84% от пациентите, които преди това са получавали ACWY -PS, развиват hSBA ≥1: 8 спрямо серогрупи A, C, W135 и Y. Един месец след ваксинацията процентите на субектите с hSBA≥1: 8 са съответно 98% -100% и 84% -96% .7 и 28 дни след бустерната доза е имало значително увеличение на hSBA GMTs спрямо всичките четири серогрупи (Таблица 8) .
Таблица 8: Отговори на бустер дозата: Реакции на бактерицидни антитела към бустер дозата на Menveo, дадена 3 и 5 години след първичната ваксинация с Menveo и ACWY-PS при пациенти на възраст от 11 до 17 години
Имуногенност при възрастни
В основното проучване за имуногенност V59P13 имунният отговор към Menveo е оценен при възрастни на възраст от 19 до 55 години. Резултатите са представени в таблица 9. При подгрупата от субекти на възраст от 19 до 55 години, които са били серонегативни в началото, процентът на субектите, постигнали hSBA ≥ 1: 8 след доза Menveo беше както следва: серогрупа А 67% (582/875); серогрупа С 71% (401/563); серогрупа W135 82% (131/160); серогрупа Y 66% (173/263 ).
Таблица 9: Отговори на серумни бактерицидни антитела след приложение на Menveo един месец след ваксинацията при лица на възраст от 19 до 55 години
В проучване V59P6E1 е оценена появата на имунен отговор след първична ваксинация с Menveo при здрави индивиди на възраст 18-22 години. 7 дни след ваксинацията 64% от пациентите са развили hSBA ≥1: 8 срещу серогрупа А и между 88% и 90% от пациентите са имали бактерицидни антитела срещу серогрупи С, W135 и Y. Един месец след ваксинацията 92% -98% от пациентите са имали hSBA ≥1: 8 срещу серогрупи A, C, W135 и Y. Също така се наблюдава стабилен имунен отговор, измерен като hSBA GMT срещу всички серогрупи на 7 дни (GMT 34 до 70) и на 28 дни (GMT 79 до 127) след единична доза ваксинация.
Имуногенност при възрастни хора
Сравнителната имуногенност на Menveo спрямо ACWY-PS е оценена при пациенти на възраст от 56 до 65 години в проучване V59P17. Процентът на субектите с hSBA ≥ 1: 8 не е по-малък от ACWY-PS за всичките четири серогрупи и статистически по-добър за серогрупи А и Y (Таблица 10).
Таблица 10: Имуногенност на доза Menveo или ACWY-PS при възрастни на възраст от 56 до 65 години, измерена един месец след ваксинацията
Налични данни за деца на възраст 2-23 месеца
Имуногенността на Menveo при деца на възраст 2-23 месеца е оценена в няколко проучвания. Въпреки че hSBA титър по-голям от 1: 8 е постигнат при висок процент пациенти, имунизирани с Menveo с дози от 4 дози, с по-ниски нива постигнато в проучвания с двудозови режими на еднократна доза, Menveo е сравнен с друга менингококова ваксина само в едно основно проучване, при което не е демонстриран отговор, поне еквивалентен на този на едновалентна серогрупова конюгирана ваксина С (след еднократна доза при 12 -месечна възраст). Наличните понастоящем данни са недостатъчни, за да се установи ефикасността на Menveo при деца на възраст под 2 години.За информация относно педиатричната употреба вижте точка 4.2.
05.2 "Фармакокинетични свойства -
Не е от значение.
05.3 Предклинични данни за безопасност -
Неклиничните данни не разкриват особен риск за хората въз основа на конвенционални проучвания за токсичност при многократни дози и токсичност за репродукцията и развитието.
При лабораторни животни не са открити нежелани реакции при ваксинирани бременни зайци или тяхното потомство до 29 -ия ден след раждането.
Не са наблюдавани ефекти върху фертилитета при женски зайци, които са приемали Menveo преди чифтосване и по време на бременност.
06.0 ФАРМАЦЕВТИЧНА ИНФОРМАЦИЯ -
06.1 Помощни вещества -
Прах
Захароза
Моноосновен калиев фосфат
Решение
Моноосновен натриев фосфат монохидрат
Динатриев фосфат дихидрат
Натриев хлорид
Вода за инжекции
06.2 Несъвместимост "-
Този лекарствен продукт не трябва да се смесва с други лекарствени продукти, с изключение на споменатите в точка 6.6.
06.3 Срок на валидност "-
3 години.
Лекарственият продукт трябва да се използва веднага след разтваряне. Въпреки това, физико-химичната стабилност е доказана в продължение на 8 часа след разтваряне при температура под 25 ° С.
06.4 Специални условия на съхранение -
Съхранявайте в хладилник (2 ° C - 8 ° C). Не замразявайте.
Съхранявайте флаконите в картонената кутия, за да предпазите лекарството от светлина.
За условията на съхранение на лекарствения продукт след разтваряне, вижте точка 6.3.
06.5 Естество на непосредствената опаковка и съдържанието на опаковката -
Прах във флакон (стъкло тип I) със запушалка (халобутилова гума) и разтвор във флакон (стъкло тип I) със запушалка (бутилова гума).
Размер на опаковката от една доза (2 флакона) или пет дози (10 флакона).
Не всички видове опаковки могат да бъдат пуснати на пазара.
06.6 Инструкции за употреба и боравене -
Menveo трябва да бъде подготвен за приложение чрез разтваряне на праха (във флакона) с разтвора (във флакона).
Съдържанието на двата различни флакона (прах MenA и разтвор на MenCWY) трябва да се смеси преди ваксинацията, за да се получи 1 доза от 0,5 ml.
Компонентите на ваксината трябва да бъдат визуално проверени преди и след разтваряне.
Със спринцовка и подходяща игла (21G, дължина 40 mm или 21G, дължина 1 ½ ") извадете цялото съдържание на флакона с разтвора и го инжектирайте във флакона с прах, за да разтворите компонента на конюгата MenA.
Обърнете и разклатете флакона енергично, след което изтеглете 0,5 ml от приготвения продукт. Обърнете внимание, че е нормално малко количество течност да остане във флакона след изтегляне на дозата.
След разтваряне ваксината е бистър, безцветен до бледожълт разтвор, без видими чужди частици. Ако се наблюдават чужди частици и / или промяна във външния вид, ваксината трябва да се изхвърли.
Преди инжектиране сменете иглата с подходяща за прилагане на ваксината. Проверете дали в спринцовката няма въздушни мехурчета, преди да инжектирате ваксината.
Неизползваното лекарство и отпадъците, получени от това лекарство, трябва да се изхвърлят в съответствие с местните разпоредби.
07.0 ПРИТЕЖАТЕЛ НА „РАЗРЕШЕНИЕТО ЗА ТЪРГОВЕ“
GSK Vaccines S.r.l.
Виа Фиорентина 1
53100 Сиена, Италия
08.0 НОМЕР НА РАЗРЕШЕНИЕ ЗА ТЪРГОВЕ -
EU/1/10/614/002
039766023
EU/1/10/614/003
039766035
09.0 ДАТА НА ПЪРВО РАЗРЕШЕНИЕ ИЛИ ПОДНОВЯВАНЕ НА РАЗРЕШЕНИЕТО -
Дата на първо разрешаване: 15 март 2010 г.
Дата на последното подновяване: 4 декември 2014 г.




















-cos-cause-sintomi-e-cura.jpg)