Активни съставки: Бортезомиб
VELCADE 3,5 mg прах за инжекционен разтвор.
Показания Защо се използва Velcade? За какво е?
VELCADE съдържа активното вещество бортезомиб, така наречения „протеазомен инхибитор“. Протеазомите играят важна роля в контролирането на клетъчната функция и растежа. Като пречи на тяхната функция, бортезомиб може да убие раковите клетки.
VELCADE се използва за лечение на множествен миелом (вид злокачествено заболяване на костния мозък) при пациенти на възраст над 18 години:
- самостоятелно или заедно с лекарствата пегилиран липозомален доксорубицин или дексаметазон, за пациенти с влошаващо се (прогресиращо) заболяване след получаване на поне едно предишно лечение или при които трансплантацията на кръвни стволови клетки е неуспешна или не е осъществима
- в комбинация с лекарствата мелфалан и преднизон за пациенти с нелекувано преди това заболяване, които не могат да получат химиотерапия с високи дози с трансплантация на кръвни стволови клетки.
- в комбинация с дексаметазон или дексаметазон заедно с талидомид, за пациенти с преди това нелекувано заболяване и преди получаване на високи дози химиотерапия с трансплантация на кръвни стволови клетки (индукционно лечение)
VELCADE се използва за лечение на мантийно -клетъчен лимфом (вид злокачествено заболяване, което засяга лимфните възли) при пациенти на 18 или повече години. В този случай VELCADE се използва в комбинация с лекарствата ритуксимаб, циклофосфамид, доксорубицин и преднизон, за пациенти с преди това нелекувано заболяване и за които трансплантацията на кръвни стволови клетки не е осъществима.
Противопоказания Когато Velcade не трябва да се използва
Не използвайте VELCADE
- ако сте алергични към бортезомиб, бор или към някоя от останалите съставки на това лекарство (изброени в точка 6)
- ако имате тежки белодробни или сърдечни проблеми.
Предпазни мерки при употреба Какво трябва да знаете, преди да приемете Velcade
Кажете на Вашия лекар, ако имате:
- нисък брой червени кръвни клетки или бели кръвни клетки
- проблеми с кървенето и / или нисък брой на тромбоцитите в кръвта
- диария, запек, гадене или повръщане
- предишни преживявания на припадък, замаяност или замаяност
- бъбречни проблеми
- умерени до тежки чернодробни проблеми
- предишни оплаквания като изтръпване, изтръпване или болка в ръцете или краката (невропатия)
- нарушение на сърцето или кръвното налягане
- задух или кашлица
- конвулсии
- херпес зостер (също разположен около очите или се разпространява в останалата част на тялото)
- симптоми на синдром на туморен лизис, като например мускулни крампи, мускулна слабост, объркване, нарушено зрение или загуба на зрение и задух
- загуба на памет, затруднено мислене, затруднено ходене или загуба на зрение. Това могат да бъдат признаци на сериозна мозъчна инфекция и Вашият лекар може да посочи допълнителни тестове и проверки.
Ще трябва да правите редовно кръвни изследвания преди и по време на терапията с VELCADE, за да проверявате постоянно стойностите на кръвните си клетки.
Ако имате мантийно -клетъчен лимфом и Ви се прилага ритуксимаб заедно с VELCADE, трябва да кажете на Вашия лекар:
- ако мислите, че имате хепатит или сте го имали в миналото. В някои случаи пациентите, които са имали хепатит В, могат да получат нова атака на хепатит, която може да бъде фатална. Ако в миналото сте имали инфекция с хепатит В, Вашият лекар ще трябва да Ви наблюдава отблизо за признаци и симптоми на активен хепатит Б.
Прочетете листовката на всички лекарства, които приемате в комбинация с VELCADE за информация относно тези лекарства, преди да започнете лечение с VELCADE.
Когато VELCADE се прилага заедно с лекарствения продукт талидомид, обърнете специално внимание на съветите за тестване на бременността и програмата за превенция на бременността (вижте "Бременност и кърмене" в този раздел).
Деца и юноши
VELCADE не трябва да се използва при деца и юноши, тъй като не е известно как действа лекарството при тези хора.
Взаимодействия Кои лекарства или храни могат да променят ефекта на Velcade
Уведомете Вашия лекар или фармацевт, ако приемате или наскоро сте приемали или е възможно да приемете други лекарства.
По -специално, кажете на Вашия лекар, ако използвате лекарства, съдържащи някое от следните активни вещества:
- кетоконазол, използван за лечение на гъбични инфекции
- ритонавир, използван за лечение на HIV инфекция - рифампицин, антибиотик, използван за лечение на бактериални инфекции
- карбамазепин, фенитоин или фенобарбитал, използвани за лечение на епилепсия
- Жълт кантарион (Hypericum perforatum), използван за лечение на депресия или други състояния
- перорални антидиабетни средства.
Предупреждения Важно е да знаете, че:
Бременност и кърмене
Не трябва да използвате VELCADE, ако сте бременна, освен ако не е наложително.
Мъжете и жените на терапия с VELCADE трябва да използват ефективни методи за контрацепция по време и до 3 месеца след лечението. Ако въпреки тези предпазни мерки забременеете, незабавно уведомете Вашия лекар.
Не трябва да кърмите, докато приемате VELCADE. Обсъдете с Вашия лекар най -доброто време да започнете да кърмите отново след края на терапията.
Лекарството талидомид причинява вродени дефекти и смърт на плода. Когато VELCADE се прилага едновременно с талидомид, трябва да следвате програмата за предотвратяване на бременност с талидомид (вижте листовката с талидомид).
Шофиране и работа с машини
VELCADE може да причини умора, замаяност, припадък или замъглено зрение. Не шофирайте и не работете с машини, ако почувствате някой от тези симптоми. Обърнете специално внимание, ако тези ефекти не настъпят.
Доза, метод и време на приложение Как да използвате Velcade: Дозировка
Вашият лекар ще изчисли дозата на VELCADE пропорционално на Вашия ръст и тегло. Стандартната начална доза на VELCADE е 1,3 mg / m2 телесна повърхност два пъти седмично. Вашият лекар може да промени дозата и общия брой курсове на лечение в зависимост от Вашия отговор на лечението, появата на някои странични ефекти и общите Ви здравословни състояния (напр. Чернодробни проблеми).
Множествен миелом в прогресия
Когато VELCADE се прилага самостоятелно, ще получите 4 дози VELCADE интравенозно или подкожно на 1, 4, 8 и 11. ден. Това е последвано от 10-дневен период на почивка без лечение.
Този 21-дневен (3-седмичен) период съответства на един курс на лечение.
Можете да получите до 8 цикъла (24 седмици). Може да приемате VELCADE заедно с пегилирани липозомни доксорубицин или дексаметазонови лекарства.
Когато VELCADE се прилага заедно с пегилиран липозомален доксорубицин, ще получите 21-дневен курс на интравенозен или подкожен VELCADE и 30 mg / m2 пегилиран липозомален доксорубицин ще бъде приложен на 4 ден от 21-дневния цикъл на лечение с VELCADE като инфузия интравенозно след инжектиране на VELCADE.
Можете да получите до 8 цикъла (24 седмици лечение).
Когато VELCADE се прилага едновременно с дексаметазон, ще получите 21-дневен курс на лечение с интравенозен или подкожен VELCADE и перорален дексаметазон в доза от 20 mg на 1, 2, 4, 5, 8, 9, 11 и 12 дни, от 21-дневния курс на лечение с VELCADE.
Можете да получите до 8 цикъла (24 седмици лечение).
Нелекуван преди това множествен миелом
Ако никога досега не сте се лекували от множествен миелом и не сте кандидат за трансплантация на кръвни стволови клетки, ще получите VELCADE заедно с две други лекарства: мелфалан и преднизон.
В този случай продължителността на курса на лечение е 42 дни (6 седмици). Той ще получи 9 цикъла (54 седмици).
- В цикли 1-4 VELCADE се прилага два пъти седмично в дни 1, 4, 8, 11, 22, 25, 29 и 32.
- В цикли 5-9 VELCADE се прилага веднъж седмично в дни 1, 8, 22 и 29.
Мелфалан (9 mg / m2) и преднизон (60 mg / m2) се прилагат през устата на 1, 2, 3 и 4 ден от първата седмица на всеки цикъл.
Ако никога преди не сте се лекували от множествен миелом и сте кандидат за трансплантация на кръвни стволови клетки, ще получите VELCADE интравенозно или подкожно заедно с лекарствата: дексаметазон или дексаметазон и талидомид, като индукционно лечение.
Когато VELCADE се прилага едновременно с дексаметазон, ще получите 21-дневен курс на лечение с интравенозен или подкожен VELCADE и перорален дексаметазон 40 mg на 1, 2, 3, 4, 8, 9, 10 и 11 ден от цикъла. -дневно лечение с VELCADE.
Ще получите 4 цикъла (12 седмици лечение).
Когато VELCADE се прилага заедно с талидомид и дексаметазон, продължителността на курса на лечение е 28 дни (4 седмици).
Дексаметазон 40 mg се прилага перорално на 1, 2, 3, 4, 8, 9, 10 и 11 ден от 28-дневния цикъл на лечение с VELCADE, а талидомид се прилага перорално в доза от 50 mg дневно до 14-ия ден от първия цикъл и, ако се понася, дозата на талидомид се увеличава до 100 mg на 15-28 дни и впоследствие може да се увеличи до 200 mg на ден от втория цикъл нататък. Можете да получите до 6 цикъла (24 седмици лечение).
Нелекуван преди това мантийно -клетъчен лимфом
Ако никога досега не сте получавали специфично лечение за мантийно -клетъчен лимфом, ще получите VELCADE интравенозно или подкожно заедно с лекарствата ритуксимаб, циклофосфамид, доксорубицин и преднизон.
VELCADE се прилага интравенозно или подкожно на 1, 4, 8 и 11 ден, последван от период на "почивка" без лечение. Продължителността на курса на лечение е 21 дни (3 седмици).
Можете да получите до 8 курса на лечение (24 седмици).
Следните лекарства се прилагат на 1 ден от всеки 21-дневен цикъл на лечение с VELCADE като интравенозна инфузия: ритуксимаб при 375 mg / m2, циклофосфамид при 750 mg / m2 и доксорубицин при 50 mg / m2.
Преднизон се прилага перорално в доза от 100 mg / m2 на 1, 2, 3, 4 и 5 ден от цикъла на лечение с VELCADE.
Как се прилага VELCADE
Това лекарство е за интравенозно или подкожно приложение. VELCADE ще се прилага от медицински специалист с опит в употребата на цитотоксични лекарства. Прахът от VELCADE трябва да се разтвори преди приложение. Това ще бъде направено от медицински специалист. Полученият разтвор след това бързо се инжектира във вена или подкожно. L "инжектирането във вена е бързо, за период от 3 до 5 секунди. Подкожната инжекция може да се направи или в бедрото, или в корема.
Предозиране Какво да направите, ако сте приели твърде много Velcade
Тъй като това лекарство е дадено от Вашия лекар или медицинска сестра, е малко вероятно да приемете повече, отколкото трябва.В малко вероятния случай на предозиране, Вашият лекар ще наблюдава за странични ефекти.
Странични ефекти Какви са страничните ефекти на Velcade
Както всички лекарства, това лекарство може да предизвика нежелани реакции, въпреки че не всеки ги получава. Някои от тези ефекти могат да бъдат сериозни.
Ако сте получили VELCADE за множествен миелом или мантийно -клетъчен лимфом, незабавно уведомете Вашия лекар, ако забележите някой от следните симптоми:
- мускулни крампи, мускулна слабост
- объркване, нарушена или загуба на зрение, слепота, гърчове, главоболие
- задух, подуване на краката или промени в сърдечната честота, високо кръвно налягане, умора, припадък
- кашлица и затруднено дишане или стягане в гърдите.
Лечението с VELCADE може много често да причини намаляване на броя на червените и белите кръвни клетки и тромбоцитите в кръвта. Поради това ще трябва редовно да правите кръвни изследвания преди и по време на лечението с VELCADE, за да проверявате редовно броя на кръвните си клетки. Може да получите намаляване на броя на:
- тромбоцити, които биха могли да ви направят по -податливи на натъртвания или кървене без забележими наранявания (например кървене в червата, стомаха, устата и венците или кръвоизлив в мозъка или черния дроб)
- червени кръвни клетки, които могат да причинят анемия, със симптоми като умора и бледност
- бели кръвни клетки, което може да ви направи по-податливи на инфекции или грипоподобни симптоми.
Ако сте получили VELCADE за лечение на множествена миелома, страничните ефекти, които могат да възникнат, са изброени по -долу.
Много чести нежелани реакции (могат да засегнат повече от 1 на 10 души)
- Сенсибилизация, изтръпване, изтръпване или парене на кожата или болка в ръцете или краката, поради увреждане на нервите.
- Намаляване на броя на червените и / или белите кръвни клетки (виж по -горе).
- Треска.
- Усещане за гадене или повръщане, загуба на апетит.
- Запек със или без излишни газове (може да бъде тежък).
- Диария: ако това се случи, важно е да пиете много повече вода от обикновено. Вашият лекар може да Ви предпише лекарства за контрол на диарията.
- Умора (умора), чувство на слабост.
- Болки в мускулите, болки в костите.
Чести нежелани реакции (могат да засегнат до 1 на 10 души)
- Ниско кръвно налягане, внезапен спад на кръвното налягане при изправяне, което може да доведе до припадък.
- Повишено кръвно налягане.
- Намалена функция на бъбреците.
- Главоболие.
- Общо неразположение, болка, замаяност, замаяност, чувство на слабост или загуба на съзнание.
- Втрисане.
- Инфекции, включително пневмония, респираторни инфекции, бронхит, гъбична инфекция, кашлица с храчки, грипоподобни заболявания.
- Инфекция с херпес зостер (локализирана, включително около очите, или разпространена по тялото).
- Болка в гърдите или затруднено дишане по време на физическа активност.
- Различни видове кожен обрив (обрив).
- Сърбеж по кожата, бучки по кожата или суха кожа.
- Зачервяване на лицето или малки счупвания в капилярите.
- Зачервяване на кожата.
- Дехидратация.
- Киселини, подуване на корема, оригване, газове, болки в стомаха, чревно или стомашно кървене.
- Промяна в чернодробната функция.
- Дразнене на устата или устните, сухота в устата, язви в устата или възпалено гърло.
- Загуба на тегло, загуба на вкус.
- Мускулни крампи, мускулни спазми, мускулна слабост, болка в ръцете и краката.
- Замъглено зрение.
- Инфекция на най -външния слой на очите и вътрешната повърхност на клепачите (конюнктивит).
- Назален кръвоизлив (кървене).
- Нарушения или проблеми със съня, изпотяване, тревожност, промени в настроението, потиснато настроение, безпокойство или възбуда, промени в психичното състояние, дезориентация.
- Подуване на тялото, включително подуване около очите и други части на тялото.
Нечести нежелани реакции (могат да засегнат до 1 на 100 души)
- Сърдечна недостатъчност, инфаркт, гръдна болка, дискомфорт в гърдите, повишена или намалена сърдечна честота.
- Бъбречна недостатъчност.
- Възпаление на вена, кръвни съсиреци във вените и белите дробове.
- Проблеми с кръвосъсирването.
- Нарушение на кръвообращението.
- Възпаление на мембраната около сърцето или наличие на течност около сърцето.
- Инфекции, включително инфекции на пикочните пътища, грип, херпесни вирусни инфекции, ушни инфекции и целулит.
- Кръв в изпражненията или кървене от лигавиците, например уста, вагина.
- Цереброваскуларни нарушения.
- Парализа, конвулсии, падане, нарушения на движението, анормална, променена или намалена чувствителност (усещане, слух, вкус, мирис), нарушение на вниманието, тремор, спазми.
- Артрит, включително възпаление на ставите на пръстите, пръстите на краката и челюстта.
- Нарушения, които засягат белите дробове, пречат на тялото ви да получава достатъчно кислород. Някои от тях включват затруднено дишане, задух, хрипове дори без физическа активност, затруднено повърхностно дишане или необходимост от спиране, хрипове.
- Хълцане, нарушения на говора.
- Повишено или намалено производство на урина (увреждане на бъбреците), болезнено уриниране или кръв / протеин в урината, задържане на течности.
- Променени нива на съзнание, объркване, увреждане или загуба на паметта.
- Свръхчувствителност.
- Загуба на слуха, глухота или звънене в ушите, дискомфорт в ухото.
- Хормонални промени, които могат да повлияят на реабсорбцията на соли и вода.
- Хиперактивност на щитовидната жлеза.
- Невъзможност за производство на достатъчно инсулин или резистентност към нормални нива на инсулин.
- Болки или възпаление на очите, прекомерно влажни очи, болка в очите, сухота в очите, очни инфекции, изпускане от очите, нарушения на зрението, кръвотечение от очите.
- Увеличени лимфни възли.
- Скованост на ставите или мускулите, усещане за тежест, болка в слабините.
- Косопад или необичайна текстура на косата.
- Алергични реакции.
- Зачервяване или болка на мястото на инжектиране.
- Болка в устата.
- Инфекция или възпаление на устата, язви в устата, хранопровода, стомаха и червата, понякога свързани с болка или кървене, нарушена подвижност на червата (включително чревна запушване), дискомфорт в корема или хранопровода, затруднено преглъщане, повръщане на кръв.
- Кожни инфекции.
- Бактериални и вирусни инфекции.
- Инфекция на зъбите.
- Възпаление на панкреаса, запушване на жлъчните пътища.
- Болка в гениталиите, проблеми с ерекцията.
- Качване на тегло.
- Усещане за жажда.
- Хепатит.
- Нарушения на мястото на инжектиране или на мястото на катетъра.
- Кожни реакции или нарушения (които могат да бъдат сериозни и животозастрашаващи), кожни язви.
- Синини, падания и наранявания.
- Възпаление или кървене на кръвоносните съдове, които могат да се проявят като малки червени или лилави точки (обикновено по краката), които могат да станат подобни на големи натъртвания по кожата или тъканите.
- Доброкачествени кисти.
- Сериозно и обратимо състояние на мозъка, което включва гърчове, високо кръвно налягане, главоболие, умора, объркване, слепота или други проблеми със зрението.
Редки нежелани реакции (могат да засегнат до 1 на 1 000 души)
- Сърдечни проблеми, включително инфаркт, стенокардия.
- Зачервявания.
- Обезцветяване на вените.
- Възпаление на гръбначния нерв.
- Ушни проблеми, кървене от ухото.
- Намалена активност на щитовидната жлеза.
- Синдром на Budd-Chiari (клиничните признаци са причинени от запушване на вените на черния дроб).
- Промяна или анормална функция на червата.
- Мозъчен кръвоизлив (кървене).
- Жълто обезцветяване на очите и кожата (жълтеница).
- Признаците на тежка алергична реакция (анафилактичен шок) включват затруднено дишане, болка в гърдите или стягане в гърдите и / или чувство на замаяност / слабост, силен сърбеж по кожата или бучки по кожата, подуване на лицето, устните, езика и / или гърлото, което може да причини затруднено преглъщане, колапс.
- Нарушения на гърдите.
- Вагинално течение.
- Подуване на гениталиите.
- Неспособност да се толерира консумацията на алкохол.
- Разхищение или загуба на телесна маса.
- Повишен апетит.
- Фистули.
- Съвместен излив.
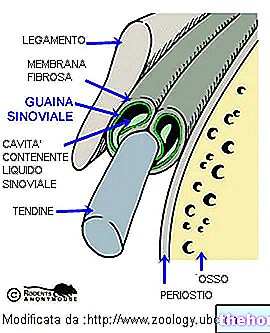
- Киста на мембраната, която покрива ставите (синовиални кисти).
- Фрактури.
- Разграждането на мускулните влакна води до други усложнения.
- Увеличен черен дроб, чернодробни кръвоизливи.
- Рак на бъбреците.
- Кожно състояние, подобно на псориазис.
- Рак на кожата.
- Бледност на кожата.
- Увеличаване на тромбоцитите или плазмените клетки (вид бели кръвни клетки) в кръвта.
- Анормална реакция към кръвопреливане.
- Частична или пълна загуба на зрение.
- Намалено либидо.
- Загуба на слюнка.
- Изпъкналост на очите.
- Фотофобия (прекомерна чувствителност на окото към светлина).
- Бързо дишане.
- Болка в ректума.
- Жлъчни камъни.
- Херния.
- Наранявания.
- Чупливи или слаби нокти.
- Ненормално отлагане на протеини в жизненоважни органи.
- Кома.
- Чревни язви.
- Увреждане на множество органи.
- Смърт.
Ако Ви е даден VELCADE заедно с други лекарства за лечение на мантийно -клетъчен лимфом, страничните ефекти, които могат да възникнат, са изброени по -долу.
Много чести нежелани реакции (могат да засегнат повече от 1 на 10 души)
- Пневмония.
- Загуба на апетит.
- Сенсибилизация, изтръпване, изтръпване или парене на кожата или болка в ръцете или краката, поради увреждане на нервите.
- Гадене и повръщане.
- Диария.
- Язви в устата.
- Чревен запек.
- Болки в мускулите, болки в костите.
- Косопад или необичайна текстура на косата.
- Умора, чувство на слабост.
- Треска.
Чести нежелани реакции (могат да засегнат до 1 на 10 души)
- Инфекция с херпес зостер (локализирана, включително около очите или разпространена по тялото).
- Херпесна вирусна инфекция.
- Бактериални и вирусни инфекции.
- Респираторни инфекции, бронхит, кашлица с храчки, грипоподобно заболяване.
- Гъбични инфекции.
- Свръхчувствителност (алергична реакция).
- Невъзможност за производство на достатъчно инсулин или резистентност към нормални нива на инсулин.
- Задържане на вода.
- Трудности или проблеми със съня.
- Загуба на съзнание.
- Променени нива на съзнание, объркване.
- Чувствам се замаян.
- Повишена сърдечна честота, високо кръвно налягане, изпотяване.
- Зрителни смущения, замъглено зрение.
- Сърдечна недостатъчност, инфаркт, гръдна болка, дискомфорт в гърдите, повишена или намалена сърдечна честота.
- Високо или ниско кръвно налягане.
- Внезапно спадане на кръвното налягане при изправяне, което може да доведе до припадък.
- Недостиг на въздух при физическа активност.
- Кашлица.
- Хълцане.
- Звънене в ушите, дискомфорт в ухото.
- Чревно или стомашно кървене.
- Стомашни болки.
- Болка в стомаха, подуване на корема.
- Затруднено преглъщане.
- Инфекция или възпаление на стомаха и червата.
- Стомашни болки.
- Дразнене на устата или устните, възпалено гърло.
- Промяна в чернодробната функция.
- Сърбяща кожа.
- Зачервяване на кожата.
- Обрив.
- Мускулни спазми.
- Инфекция на пикочните пътища.
- Болка в крайниците.
- Подуване на тялото, включително подуване около очите и други части на тялото.
- Втрисане.
- Зачервяване и болка на мястото на инжектиране.
- Усещане за общо неразположение.
- Загуба на телесно тегло.
- Повишаване на телесното тегло.
Нечести нежелани реакции (могат да засегнат до 1 на 100 души)
- Хепатит.
- Тежка алергична реакция (анафилактична реакция), чиито признаци могат да включват затруднено дишане, болка в гърдите или стягане в гърдите и / или чувство на замаяност / слабост, силно сърбеж по кожата или бучки по кожата, подуване на лицето, устните, езика и / или гърлото, което може да причини затруднено преглъщане, колапс.
- Нарушения на движението, парализа, контракции.
- Замайване.
- Загуба на слуха, глухота.
- Нарушения, които засягат белите дробове, пречат на тялото ви да получава достатъчно кислород. Някои от тях включват затруднено дишане, задух, хрипове дори и без физическа активност, дишане, което става плитко, затруднено или спира, хрипове.
- Кръвни съсиреци в белите дробове.
- Жълто обезцветяване на очите и кожата (жълтеница).
Докладване на странични ефекти
Ако получите някакви нежелани реакции, говорете с Вашия лекар или фармацевт.Това включва всички възможни нежелани реакции, които не са изброени в тази листовка. Можете също да съобщите нежелани реакции директно чрез националната система за докладване, изброена в допълнение V. Чрез съобщаване на странични ефекти можете да помогнете за предоставяне на повече информация за безопасността на това лекарство.
Срок на годност и задържане
Съхранявайте това лекарство на място, недостъпно за деца.
Не използвайте това лекарство след срока на годност, отбелязан върху флакона и картонената опаковка след „Годен до:“.
Съхранявайте при температура не по -висока от 30 ° C. Съхранявайте флакона във външната опаковка, за да предпазите лекарството от светлина.
Готовият разтвор трябва да се използва веднага след приготвянето. Ако приготвеният разтвор не се използва незабавно, условията и времето за употреба са отговорност на готвача. Приготвеният разтвор обаче е стабилен в продължение на 8 часа при 25 ° C преди приложение, когато се съхранява в оригиналния флакон и / или в спринцовка, като максималното време за съхранение на приготвения лекарствен продукт не надвишава 8 часа.
VELCADE е само за еднократна употреба. Неизползваният продукт и отпадъците трябва да се изхвърлят в съответствие с действащите местни разпоредби.
Краен срок "> Друга информация
Какво съдържа VELCADE
- Активната съставка е бортезомиб. Всеки флакон съдържа 3,5 mg бортезомиб (като боронен естер на манитол). След разтваряне 1 ml инжекционен разтвор съдържа 1 mg бортезомиб.
- Другите съставки са манитол (Е421) и азот.
Разтваряне за интравенозно приложение: След разтваряне 1 ml разтвор за интравенозно инжектиране съдържа 1 mg бортезомиб.
Разтваряне за подкожна употреба: След разтваряне 1 ml разтвор за подкожно инжектиране съдържа 2,5 mg бортезомиб.
Описание на това как изглежда VELCADE и съдържанието на опаковката
VELCADE прах за инжекционен разтвор е бял до кремаво бял.
Всяка опаковка VELCADE 3,5 mg съдържа 1 стъклен флакон от 10 ml със синя капачка, съдържащ се в прозрачен блистер.
Краен срок "> Информация за здравни специалисти
Следната информация е предназначена само за здравни специалисти
ВЪЗСТАНОВЯВАНЕ ЗА ИНТРАВЕННО ИНЖЕКТИРАНЕ
Забележка: VELCADE е цитотоксичен агент. Следователно, по време на манипулацията и подготовката трябва да се внимава особено. Препоръчително е да носите ръкавици и друго защитно облекло, за да предотвратите контакт с кожата.
Поради отсъствието на какъвто и да е вид консерванти, АСЕПТИЧНИТЕХНИЧНИ СТАНДАРТИ ТРЯБВА ДА СЕ СЛЕДВАТ ПО ВРЕМЕ НА РАБОТА С VELCADE.
- Приготвяне на флакона от 3,5 mg: Добавете 3,5 ml стерилен разтвор на натриев хлорид 9 mg / ml (0,9%) за инжектиране към флакона, съдържащ прах VELCADE. Лиофилизираният прах се разтваря напълно за по -малко от 2 минути.
Концентрацията на получения разтвор е равна на 1 mg / ml. Разтворът ще бъде бистър и безцветен с крайно рН между 4 и 7. Не е необходимо да се проверява рН на разтвора.
- Разтворът трябва да бъде визуално инспектиран преди прилагане, за да се провери за наличие на частици или промяна в цвета.В присъствието на прахови частици или промяна в цвета, разтворът не трябва да се използва и трябва да се изхвърли.
Потвърдете концентрацията върху флакона, за да сте сигурни, че правилната доза се прилага интравенозно (1 mg / ml).
- Разтвореният разтвор не съдържа консерванти и трябва да се използва веднага след приготвянето му, докато е химически и физически стабилен в продължение на 8 часа при 25 ° C в оригиналния флакон и / или в спринцовка с максимум 8 часа в спринцовката. Общото време за съхранение на приготвения лекарствен продукт не може да надвишава 8 часа преди приложението. Ако приготвеният разтвор не се използва веднага след приготвянето, потребителят носи отговорност да спазва условията и времето за съхранение на продукта преди употреба.
Не е необходимо да се предпазва разтвореният лекарствен продукт от светлина.
АДМИНИСТРИРАНЕ
- След като се разтвори, изтеглете подходящото количество от приготвения разтвор в съответствие с дозата, изчислена въз основа на телесната повърхност на пациента.
- Потвърдете дозата и концентрацията в спринцовката преди употреба (проверете дали спринцовката е маркирана за интравенозно приложение).
- Инжектирайте разтвора интравенозно под формата на 3-5 секунден болус, през периферен или централен интравенозен катетър.
- Промийте интравенозния катетър със стерилен инжекционен разтвор на натриев хлорид 9 mg / ml (0,9%).
VELCADE 3,5 mg прах за инжекционен разтвор е за подкожна или интравенозна употреба. Не прилагайте по други начини. Интратекалната администрация доведе до смърт.
ИЗХВЪРЛЯНЕ
Флаконът е само за еднократна употреба и останалият разтвор трябва да се изхвърли.
Неизползваното лекарство и отпадъците от това лекарство трябва да се изхвърлят в съответствие с местните разпоредби.
Следната информация е предназначена само за здравни специалисти:
Само флакон от 3,5 mg може да се прилага подкожно, както е описано по -долу.
ВЪЗСТАНОВЯВАНЕ ЗА ПОДКУТАННО ИНЖЕКТИРАНЕ
Забележка: VELCADE е цитотоксичен агент. Следователно, по време на работа и подготовка трябва да се внимава особено. Препоръчително е да носите ръкавици и друго защитно облекло, за да предотвратите контакт с кожата.
Поради отсъствието на какъвто и да е вид консерванти, АСЕПТИЧНИТЕХНИЧНИ СТАНДАРТИ ТРЯБВА ДА СЕ СЛЕДВАТ ПО ВРЕМЕ НА РАБОТА С VELCADE.
- Подготовка на флакона от 3,5 mg: Добавете 1,4 ml стерилен натриев хлорид 9 mg / ml (0,9%) инжекционен разтвор към флакона, съдържащ праха VELCADE. Лиофилизираният прах се разтваря напълно за по -малко от 2 минути.
Концентрацията на получения разтвор е равна на 2,5 mg / ml. Разтворът ще бъде бистър и безцветен с крайно рН между 4 и 7. Не е необходимо да се проверява рН на разтвора.
- Разтворът трябва да бъде визуално инспектиран преди прилагане, за да се провери за наличие на частици или промяна в цвета.В присъствието на прахови частици или промяна в цвета, разтворът не трябва да се използва и трябва да се изхвърли.
Потвърдете концентрацията върху флакона, за да сте сигурни, че правилната доза се прилага подкожно (2,5 mg / ml).
- Разтвореният разтвор не съдържа консерванти и трябва да се използва веднага след приготвянето му, докато е химически и физически стабилен в продължение на 8 часа при 25 ° C в оригиналния флакон и / или в спринцовка с максимум 8 часа в спринцовката. Общото време за съхранение на приготвения лекарствен продукт не може да надвишава 8 часа преди приложението. Ако приготвеният разтвор не се използва веднага след приготвянето, потребителят носи отговорност да спазва условията и времето за съхранение на продукта преди употреба.
Не е необходимо да се предпазва разтвореният лекарствен продукт от светлина.
АДМИНИСТРИРАНЕ
- След като се разтвори, изтеглете подходящото количество от приготвения разтвор в съответствие с дозата, изчислена въз основа на телесната повърхност на пациента.
- Потвърдете дозата и концентрацията в спринцовката преди употреба (проверете дали спринцовката е маркирана за подкожно приложение).
- Инжектирайте разтвора подкожно, под ъгъл 45-90 °
- Разтвореният разтвор се прилага подкожно в бедрата (дясно или ляво) или корема (дясно или ляво)
- При следващите приложения е необходимо да се смени мястото на инжектиране при ротация.
- Ако се появят локални реакции на мястото на инжектиране след подкожно инжектиране на VELCADE, може да се приложи по -ниска концентрация на 3,5 mg разтвор на VELCADE (1 mg / ml вместо 2,5 mg / ml) или се препоръчва да се премине към „интравенозна инжекция.
VELCADE 3,5 mg прах за инжекционен разтвор е за подкожна или интравенозна употреба. Не прилагайте по други начини. Интратекалната администрация доведе до смърт.
ИЗХВЪРЛЯНЕ
Флаконът е само за еднократна употреба и останалият разтвор трябва да се изхвърли.
Неизползваното лекарство и отпадъците от това лекарство трябва да се изхвърлят в съответствие с местните разпоредби.
Източник на листовката: AIFA (Италианска агенция по лекарствата). Съдържание, публикувано през януари 2016 г. Наличната информация може да не е актуална.
За да имате достъп до най-актуалната версия, препоръчително е да получите достъп до уебсайта на AIFA (Италианска агенция по лекарствата). Отказ от отговорност и полезна информация.
01.0 ИМЕ НА ЛЕКАРСТВЕНИЯ ПРОДУКТ -
VELCADE 3,5 MG прах за разтвор за инжектиране
02.0 КАЧЕСТВЕН И КОЛИЧЕСТВЕН СЪСТАВ -
Всеки флакон съдържа 3,5 mg бортезомиб (като боронен естер на манитол).
След разтваряне 1 ml инжекционен разтвор за подкожна употреба съдържа 2,5 mg бортезомиб.
След разтваряне 1 ml инжекционен разтвор за интравенозно приложение съдържа 1 mg бортезомиб.
За пълния списък на помощните вещества вижте точка 6.1.
03.0 ЛЕКАРСТВЕНА ФОРМА -
Прах за инжекционен разтвор.
Бял до кремаво -бял прах (дори уплътнен).
04.0 КЛИНИЧНА ИНФОРМАЦИЯ -
04.1 Терапевтични показания -
VELCADE като монотерапия или в комбинация с пегилиран липозомален доксорубицин или дексаметазон е показан за лечение на възрастни пациенти с прогресиращ множествен миелом, които вече са получили поне една предишна линия на лечение и които вече са преминали или не отговарят на изискванията за трансплантация на стволови клетки. .
VELCADE в комбинация с мелфалан и преднизон е показан за лечение на възрастни пациенти с преди това нелекуван множествен миелом, които не отговарят на условията за химиотерапия с високи дози с трансплантация на хемопоетични стволови клетки.
VELCADE в комбинация с дексаметазон или с дексаметазон и талидомид е показан за индукционно лечение на възрастни пациенти с преди това нелекуван множествен миелом, които отговарят на условията за химиотерапия с високи дози с трансплантация на хемопоетични стволови клетки.
VELCADE в комбинация с ритуксимаб, циклофосфамид, доксорубицин и преднизон е показан за лечение на възрастни пациенти с преди това нелекуван мантийно -клетъчен лимфом, които не отговарят на условията за трансплантация на хемопоетични стволови клетки.
04.2 Дозировка и начин на приложение -
Лечението трябва да започне и да се провежда под наблюдението на лекар, обучен и с опит в употребата на химиотерапевтични средства.VELCADE трябва да се разтвори от медицински специалист.
Дозировка за лечение на прогресиращ множествен миелом (пациенти, които са получили поне една предишна линия на лечение)
Монотерапия
VELCADE 3,5 mg прах за инжекционен разтвор се прилага интравенозно или подкожно в препоръчителната доза от 1,3 mg / m² телесна повърхност два пъти седмично в продължение на две седмици в ден 1, 4, 8 и 11 в един 21 -дневен цикъл на лечение Този 3 -седмичен период се счита за цикъл на лечение.
Препоръчва се пациентите да получат 2 курса на VELCADE след потвърждение, че е постигнат пълен отговор.
На пациентите, които се повлияват от лечението, но не постигат пълна ремисия, се препоръчва да приложат общо 8 курса на VELCADE.
Между прилагането на две последователни дози VELCADE трябва да изминат поне 72 часа.
Коригиране на дозата по време на лечението и възобновяването му като монотерапия
Терапията с VELCADE трябва да се преустанови в началото на всяка нехематологична токсичност от степен 3 или всякаква хематологична токсичност от степен 4, с изключение на невропатията, както е посочено по-долу (вж. Също точка 4.4). 1,3 mg / m² намален до 1,0 mg / m²; 1,0 mg / m² намален до 0,7 mg / m²). Когато симптомите на токсичност не са отзвучали или ако се повтарят при намалена доза, трябва да се обмисли прекратяване на VELCADE, освен ако ползите терапията очевидно надвишава рисковете.
Невропатична болка и / или периферна невропатия
Пациентите, които изпитват свързана с бортезомиб невропатична болка и / или периферна невропатия, трябва да бъдат лекувани съгласно Таблица 1 (вж. Точка 4.4).
Пациентите с предшестваща тежка невропатия могат да бъдат лекувани с VELCADE само след „внимателна оценка на риска / ползата“.
Таблица 1: Препоръчителни модификации на дозата * в случай на невропатия, свързана с приложението на бортезомиб
Комбинирана терапия с пегилиран липозомен доксорубицин
VELCADE 3,5 mg прах за инжекционен разтвор се прилага интравенозно или подкожно в препоръчителната доза от 1,3 mg / m² телесна повърхност два пъти седмично в продължение на две седмици в ден 1, 4, 8 и 11 в един 21 -дневен цикъл на лечение Този 3 -седмичен период се счита за цикъл на лечение Между приемането на две последователни дози VELCADE трябва да изминат най -малко 72 часа.
Пегилиран липозомален доксорубицин се прилага в доза 30 mg / m² на 4 -ия ден от цикъла на лечение с VELCADE като интравенозна инфузия с продължителност 1 час след инжектирането на VELCADE.
До 8 цикъла от тази комбинирана терапия могат да се прилагат, докато пациентите покажат прогресия и понасят лечението. Пациентите, които постигнат пълен отговор, могат да продължат лечението поне 2 цикъла след първите доказателства за пълен отговор, дори ако това изисква лечение за повече от 8 цикъла. Пациентите, чиито нива на парапротеини продължават да намаляват след 8 цикъла, могат да продължат терапията, докато лечението се понася и продължават да показват отговор.
За допълнителна информация относно пегилиран липозомен доксорубицин, моля, вижте съответното резюме на характеристиките на продукта.
Комбинация с дексаметазон
VELCADE 3,5 mg прах за инжекционен разтвор се прилага интравенозно или подкожно в препоръчителната доза от 1,3 mg / m² телесна повърхност два пъти седмично в продължение на две седмици в ден 1, 4, 8 и 11 в един 21 -дневен цикъл на лечение Този 3 -седмичен период се счита за цикъл на лечение Между приемането на две последователни дози VELCADE трябва да изминат най -малко 72 часа.
Дексаметазон се прилага перорално в доза от 20 mg на 1, 2, 4, 5, 8, 9, 11 и 12 ден от цикъла на лечение с VELCADE.
Пациентите, които постигнат отговор на заболяването или стабилизиране след 4 цикъла от тази комбинирана терапия, могат да продължат да получават същата комбинация за до 4 допълнителни цикъла.
За допълнителна информация относно дексаметазон, моля, вижте съответното резюме на характеристиките на продукта.
Корекция на дозата за комбинирана терапия при пациенти с прогресиращ множествен миелом
За корекции на дозата на VELCADE при комбинирана терапия следвайте препоръките за модифициране на дозата, описани в раздела за монотерапия по -горе.
Дозировка за лечение на преди това нелекуван множествен миелом при пациенти, които не отговарят на условията за химиотерапия с високи дози с трансплантация на хемопоетични стволови клетки.
Комбинирана терапия с мелфалан и преднизон
VELCADE 3,5 mg прах за инжекционен разтвор се прилага интравенозно или подкожно в комбинация с перорален мелфалан и перорален преднизон, както е посочено в таблица 2. 6-седмичен период се счита за курс на лечение. В цикли 1-4 VELCADE се прилага два пъти седмично в дни 1, 4, 8, 11, 22, 25, 29 и 32. В цикли 5-9 VELCADE се дава веднъж седмично в дни 1, 8, 22 и 29. Между прилагането на две последователни дози VELCADE трябва да изминат поне 72 часа.
Мелфалан и преднизон трябва да се прилагат перорално на 1, 2, 3 и 4 ден от първата седмица от всеки цикъл на лечение с VELCADE. Прилагат се 9 цикъла на лечение на тази комбинирана терапия.
Таблица 2: График на препоръчителната дозировка на VELCADE в комбинация с мелфалан и преднизон
Корекции на дозата по време на лечението и възобновяването му в комбинация с мелфалан и преднизон
Преди да започнете нов курс на терапия:
• броят на тромбоцитите трябва да бъде ≥ 70 x 109 / L, а абсолютният брой на неутрофилите (ANC) ≥ 1,0 x 109 / L
• Нехематологичните токсичности трябва да са намалели до степен 1 или изходно ниво
Таблица 3: Промени в дозировката по време на последващи курсове на терапия с VELCADE в комбинация с мелфалан и преднизон
За повече информация относно мелфалан и преднизон, вижте съответните им резюмета на характеристиките на продукта.
Дозировка за лечение на предварително нелекуван множествен миелом при пациенти, отговарящи на условията за трансплантация на хемопоетични стволови клетки (индукционна терапия).
Комбинирана терапия с дексаметазон
VELCADE 3,5 mg прах за инжекционен разтвор се прилага интравенозно или подкожно в препоръчителната доза от 1,3 mg / m² телесна повърхност два пъти седмично в продължение на две седмици в ден 1, 4, 8 и 11 в един 21 -дневен цикъл на лечение Този 3 -седмичен период се счита за цикъл на лечение Между приемането на две последователни дози VELCADE трябва да изминат най -малко 72 часа.
Дексаметазон се прилага перорално в доза от 40 mg на 1, 2, 3, 4, 8, 9, 10 и 11 ден от цикъла на лечение с VELCADE.
Прилагат се четири лечебни цикъла от тази комбинирана терапия.
Комбинирана терапия с талидомид и дексаметазон
VELCADE 3,5 mg прах за инжекционен разтвор се прилага интравенозно или подкожно в препоръчителната доза от 1,3 mg / m² телесна повърхност два пъти седмично в продължение на две седмици в ден 1, 4, 8 и 11 в един 28 -дневен цикъл на лечение Този 4 -седмичен период се счита за цикъл на лечение.
Между прилагането на две последователни дози VELCADE трябва да изминат поне 72 часа.
Дексаметазон се прилага перорално в доза от 40 mg на 1, 2, 3, 4, 8, 9, 10 и 11 ден от цикъла на лечение с VELCADE.
Талидомид се прилага перорално в дневна доза от 50 mg на 1-14 дни; ако се понася, дозата се увеличава до 100 mg на 15-28 дни и впоследствие може допълнително да се увеличи до 200 mg на ден от цикъл 2 (вж. Таблица 4).
Прилагат се четири лечебни цикъла от тази комбинирана терапия.
За пациенти, които постигат поне частичен отговор, се препоръчват допълнителни 2 курса на лечение.
Таблица 4: Дозировка на комбинирана терапия с VELCADE за лечение на нелекуван преди това множествен миелом при пациенти, отговарящи на условията за трансплантация на хематопоетични стволови клетки.
Корекция на дозата за кандидати за трансплантация
За корекция на дозата на VELCADE за невропатия, вижте Таблица 1.
Освен това, когато VELCADE се прилага в комбинация с други химиотерапевтични средства, трябва да се обмисли подходящо намаляване на дозата на тези лекарствени продукти в случай на токсичност съгласно препоръките в съответното резюме на характеристиките на продукта.
Дозировка за пациенти с преди това нелекуван мантийно -клетъчен лимфом (MCL)
Комбинирана терапия с ритуксимаб, циклофосфамид, доксорубицин и преднизон (VcR-CAP)
VELCADE 3,5 mg прах за инжекционен разтвор се прилага интравенозно или подкожно в препоръчителната доза от 1,3 mg / m² телесна повърхност два пъти седмично в продължение на две седмици на 1, 4, 8 и 11 ден, последвано от 10 -дневен период на почивка в дните 12 до 21. Този 3 -седмичен период се счита за курс на лечение Най -малко 72 часа трябва да изминат между прилагането на две последователни дози VELCADE.
Препоръчват се 6 цикъла на лечение с тази комбинирана терапия. Пациентите с документиран първи отговор на цикъл 6 могат да получат 2 допълнителни курса на лечение.
Следните лекарствени продукти се прилагат като интравенозна инфузия в ден 1 на всеки 3-седмичен цикъл на лечение с VELCADE: ритуксимаб в доза 375 mg / m², циклофосфамид в доза 750 mg / m² и доксорубицин в доза 50 mg / m².
Преднизон се прилага перорално в доза от 100 mg / m² на 1, 2, 3, 4 и 5 ден от всеки цикъл на лечение с VELCADE.
Корекция на дозата по време на лечението на пациенти с преди това нелекуван MCL
Преди да започнете нов курс на терапия:
• Броят на тромбоцитите трябва да бъде ≥ 100 000 клетки / mcL, а абсолютният брой на неутрофилите (ANC) трябва да бъде ≥ 1500 клетки / mcL
• Броят на тромбоцитите трябва да бъде ≥ 75 000 клетки / mcL при пациенти с инфилтрация на костен мозък или секвестрация на далака
• Хемоглобинът трябва да бъде ≥ 8 g / dL
• Нехематологичната токсичност трябва да бъде намалена до степен 1 или изходно ниво.
Лечението с VELCADE трябва да се преустанови в началото на всяка степен ≥ 3, свързана с VELCADE, нехематологична токсичност (с изключение на невропатия) или степен ≥ 3 хематологична токсичност (вижте също точка 4.4). За корекция на дозата вижте таблица 5 по-долу.
В случай на хематологична токсичност, гранулоцитни растежни фактори могат да се прилагат съгласно местната стандартна практика. Трябва да се обмисли превантивна употреба на растежни гранулоцитни фактори в случай на многократни забавяния при провеждане на курсове на терапия.Когато е клинично подходящо, трябва да се обмисли преливане на тромбоцити за лечение на тромбоцитопения.
Таблица 5: Корекция на дозата по време на лечение на пациенти с преди това нелекуван MCL
Освен това, когато VELCADE се прилага в комбинация с други химиотерапевтични средства, „трябва да се обмисли подходящо намаляване на дозата на тези лекарствени продукти в случай на токсичност, съгласно препоръките, съдържащи се в съответното резюме на характеристиките на продукта“.
Специални популации
Пациенти в напреднала възраст
Няма клинични доказателства, които да предполагат необходимост от коригиране на дозата при пациенти на възраст над 65 години с множествен миелом или мантийно -клетъчен лимфом.
Няма проучвания за употребата на VELCADE при пациенти в старческа възраст с нелекуван преди това множествен миелом, които са кандидати за химиотерапия с високи дози с трансплантация на хематопоетични стволови клетки.
Следователно не могат да се правят препоръки за дозиране при тази популация.
В проучване при пациенти, които преди това не са били лекувани с мантийно-клетъчен лимфом, 42,9% и 10,4% от пациентите, изложени на VELCADE, са били съответно в границите на 65-74 години и ≥ 75 години. При пациенти на възраст ≥ 75 години и двата режима, VELCADE в комбинация с ритуксимаб, циклофосфамид, доксорубицин и преднизон (VcR-CAP) и ритуксимаб, циклофосфамид, доксорубицин, винкристин и преднизон (R-CHOP), се понасят по-малко (вж. Параграф 8) ).
Чернодробна дисфункция
Пациентите с леко чернодробно увреждане не изискват корекция на дозата и трябва да бъдат лекувани с препоръчителната доза.Пациенти с умерено или тежко чернодробно увреждане трябва да започнат лечение с VELCADE в намалена доза от 0,7 mg / m² на инжекция по време на първия цикъл на лечение, а последващо повишаване на дозата до 1,0 mg / m² или допълнително намаляване на дозата до 0,5 mg / m² може трябва да се вземат предвид въз основа на толерантността на пациента (вж. Таблица 6 и раздели 4.4 и 5.2).
Таблица 6: Препоръчителни първоначални промени на дозата на VELCADE за пациенти с чернодробно увреждане
Бъбречна дисфункция
Фармакокинетиката на бортезомиб не се повлиява при пациенти с леко до умерено бъбречно увреждане (креатининов клирънс [CrCL]> 20 ml / min / 1,73 m²); следователно не се налага корекция на дозата при тези пациенти. Не е известно дали фармакокинетиката на бортезомиб е променена при пациенти с тежко бъбречно увреждане, които не са на диализа (CrCL
Педиатрична популация
Безопасността и ефикасността на VELCADE при пациенти на възраст под 18 години не са установени (вж. Точки 5.1 и 5.2) .Няма данни.
Начин на приложение
VELCADE 3,5 mg прах за инжекционен разтвор е за интравенозно или подкожно приложение.
VELCADE 1 mg прах за инжекционен разтвор е само за интравенозно приложение.
VELCADE не трябва да се прилага по други пътища. Интратекалната администрация причини смърт.
Интравенозно инжектиране
Разтвореният разтвор на VELCADE 3,5 mg се прилага интравенозно под формата на 3-5 секунден болус, чрез периферен или централен интравенозен катетър, последван от промиване с натриев хлорид 9 mg / ml (0,9%). Между две последователни дози VELCADE трябва да има поне 72 часа.
Подкожно инжектиране
Разтвореният разтвор на VELCADE 3,5 mg се прилага подкожно в бедрата (дясно или ляво) или корема (дясно или ляво) .Разтворът трябва да се инжектира подкожно под ъгъл 45-90 °.
Местата на инжектиране трябва да се променят при завъртане за последващи инжекции.
Ако след подкожно приложение на VELCADE се появят реакции на мястото на инжектиране, може да се приложи подкожно по -малко концентриран разтвор на VELCADE (VELCADE 3,5 mg, разтворен при 1 mg / ml вместо 2,5 mg / ml) или се препоръчва преминаване към интравенозно приложение.
Когато VELCADE се прилага в комбинация с други лекарствени продукти, вижте Резюмето на характеристиките на продукта на тези лекарствени продукти за инструкции за приложение.
04.3 Противопоказания -
Свръхчувствителност към активното вещество, бор или към някое от помощните вещества, изброени в точка 6.1.
Остра дифузна инфилтративна белодробна болест и перикардиопатия.
Когато VELCADE се прилага в комбинация с други лекарствени продукти, вижте съответната Кратка характеристика на продукта за допълнителни противопоказания.
04.4 Специални предупреждения и подходящи предпазни мерки при употреба -
Когато VELCADE се прилага в комбинация с други лекарствени продукти, преди започване на лечението с VELCADE трябва да се консултира със съответната Кратка характеристика на продукта.При прилагане на талидомид трябва да се обърне специално внимание на тестването на бременността и правилата за предотвратяване на бременността. Вижте точка 4.6).
Интратекално приложение
Има случаи на смърт след неволно интратекално приложение на VELCADE. VELCADE 1 mg прах за инжекционен разтвор е предназначен само за интравенозно приложение, докато VELCADE 3,5 mg прах за инжекционен разтвор е предназначен за интравенозно или подкожно приложение. VELCADE не трябва да се прилага интратекално.
Стомашно -чревна токсичност
Стомашно -чревните токсични ефекти, включително гадене, диария, повръщане и запек, са много чести по време на лечението с VELCADE. Нечесто са докладвани случаи на паралитичен илеус (вж. Точка 4.8). Следователно, пациентите, страдащи от запек, трябва да бъдат наблюдавани внимателно.
Хематологична токсичност
Лечението с VELCADE много често се свързва с хематологични токсични ефекти (тромбоцитопения, неутропения и анемия). В проучвания, проведени при пациенти с рецидивиращ множествен миелом, лекувани с VELCADE, и при пациенти с нелекуван преди това MCL, лекуван с VELCADE в комбинация с ритуксимаб, циклофосфамид, доксорубицин и преднизон (VcR-CAP), една от най-честите хематологични токсичности е преходна тромбоцитопения. Тромбоцитите са били на най -ниското си ниво на Ден 11 от всеки цикъл на лечение с VELCADE и се връщат към изходните нива обикновено през следващия цикъл. Няма данни за кумулативна тромбоцитопения. Средният надир на тромбоцитната стойност е приблизително 40% от изходната стойност в проучванията за множествен миелом с VELCADE, използван като монотерапия, и 50% в проучването MCL. При пациенти с напреднал миелом тежестта на тромбоцитопенията е свързана с стойностите на тромбоцитите преди лечението: за стойностите на тромбоцитите при изходните 75 000 / mcl само 14% от 309 пациенти са имали брой тромбоцити ≤ 25 000 / mcl по време на проучването.
При пациенти с MCL (проучване LYM-3002) се наблюдава по-висока честота (56,7% срещу 5,8%) Тромбоцитопения степен ≥ 3 в групата на лечение с VELCADE (VcR-CAP) спрямо групата, различна от VELCADE (ритуксимаб, циклофосфамид, доксорубицин, винкристин и преднизон [R-CHOP]). Двете лечебни групи бяха сходни както в общата честота на кръвоизливи от всички степени (6,3% в групата на VcR-CAP и 5,0% в групата на R-CHOP), така и в степен 3 и голямо кървене (VcR-CAP: 4 пациенти [ 1,7%]; R-CHOP: 3 пациенти [1,2%]) .В групата с VcR-CAP 22,5% от пациентите са получили трансфузия на тромбоцити в сравнение с 2,9% от пациентите в групата с R-CHOP.
Съобщава се за стомашно -чревен и вътремозъчен кръвоизлив във връзка с лечението с VELCADE. Следователно нивата на тромбоцитите трябва да се проследяват преди прилагането на всяка доза VELCADE. Терапията с VELCADE трябва да се преустанови, когато броят на тромбоцитите достигне стойности
По време на лечението с VELCADE трябва често да се следи пълната кръвна картина с различен брой, включително тромбоцитите.Когато е клинично подходящо, трябва да се обмисли трансфузия на тромбоцити (вж. Точка 4.2).
При пациенти с MCL без данни за кумулативна неутропения се наблюдава преходна обратима неутропения между курсовете на лечение. Неутрофилите са били на най -ниското си ниво на Ден 11 от всеки цикъл на лечение с VELCADE и обикновено се връщат към изходното ниво в следващия цикъл. В проучване LYM-3002, подкрепата на растежния фактор е използвана при 78% от пациентите в рамото на VcR-CAP и 61% от пациентите в рамото на R-CHOP. Тъй като пациентите с неутропения са с повишен риск от инфекции, те трябва да бъдат наблюдавани за признаци и симптоми на инфекция и да се лекуват своевременно. Гранулоцитни растежни фактори могат да се прилагат за лечение на хематологична токсичност съгласно местната стандартна практика. В случай на многократни забавяния в прилагането на курсове на терапия, трябва да се обмисли превантивното използване на растежни фактори на гранулоцити (вж. Точка 4.2).
Реактивиране на вируса на херпес зостер
Прилагането на антивирусна профилактика се препоръчва при пациенти, получаващи VELCADE. Във фаза III проучване, проведено при пациенти с предварително нелекуван множествен миелом, общата честота на реактивиране на херпес зостер е по -честа при пациенти, лекувани с VELCADE + Мелфалан + Преднизон, отколкото при пациенти, лекувани с Мелфалан + Преднизон (съответно 14 % срещу 4 %).
При пациенти с MCL (проучване LYM-3002) честотата на инфекция с херпес зостер е 6,7% в рамото на VcR-CAP и 1,2% в рамото на R-CHOP (вж. Точка 4.8).
Реактивиране и инфекция с вируса на хепатит В (HBV)
Когато ритуксимаб се използва в комбинация с VELCADE, винаги трябва да се извършва скрининг за HBV преди започване на лечението при пациенти с риск от HBV инфекция. Носителите на хепатит В и пациентите с анамнеза за хепатит В трябва да бъдат внимателно наблюдавани за клинични и лабораторни признаци на активна HBV инфекция по време и след лечение с ритуксимаб в комбинация с VELCADE. Трябва да се обмисли антивирусна профилактика. За повече информация вижте Кратката характеристика на продукта за ритуксимаб.
Прогресивна мултифокална левкоенцефалопатия (PML)
Съобщавани са много редки случаи на инфекция с вируса на Джон Къннингъм (JC), водеща до PML и смърт при пациенти, лекувани с VELCADE, с неизвестна причинно -следствена връзка. Пациентите, диагностицирани с PML, преди това са приемали имуносупресивна терапия или са я приемали едновременно. Повечето случаи на PML са диагностицирани в рамките на 12 месеца след приема на първата доза VELCADE. Пациентите трябва да бъдат наблюдавани на редовни интервали за нови или влошаващи се неврологични симптоми или признаци, които могат да показват ПМЛ сред диференциалните диагнози на проблеми с централната нервна система. Ако се подозира диагноза PML, пациентите трябва да бъдат насочени към лекар, който е специализиран в лечението на PML и да се прилагат подходящи диагностични мерки за PML. В случай на потвърдена диагноза PML, лечението с VELCADE трябва да се преустанови.
Периферна невропатия
Лечението с VELCADE най -често се свързва с появата на периферна, предимно сензорна невропатия, но са докладвани случаи на тежка моторна невропатия с или без периферна сензорна невропатия.
Честотата на периферна невропатия се увеличава в началото на лечението и достига пик в цикъл 5.
Пациентите трябва да бъдат внимателно наблюдавани за симптоми на невропатия, като усещане за парене, хиперестезия, хипестезия, парестезия, неразположение, невропатична болка или слабост.
В клиничното проучване фаза III, сравняващо VELCADE, прилаган интравенозно с подкожния път, честотата на събитията с периферна невропатия от степен 2 е 24% в групата с подкожно приложение и 41% в групата с интравенозно инжектиране (р = 0,0124). невропатия се е появила при 6% от пациентите в групата на подкожно лечение в сравнение с 16% в групата на интравенозно лечение (р = 0,0264) .Всички степени на периферна невропатия с интравенозно прилаган VELCADE са били по -ниски в предишни проучвания, при които VELCADE се е прилагал интравенозно, отколкото в проучване MMY -3021.
Препоръчва се неврологична оценка при пациенти с поява или влошаване на периферната невропатия, за които може да се наложи промяна в дозата или режима или промяна в начина на приложение към подкожния път (вж. Точка 4.2). Невропатията се лекува с поддържащи или други терапии.
Трябва да се обмисли ранен и редовен мониторинг за симптоми на свързана с лечението невропатия с неврологична оценка при пациенти, получаващи VELCADE в комбинация с лекарствени продукти, за които е известно, че са свързани с невропатия (напр. Талидомид) и трябва да се обмисли подходящо намаляване на дозата или преустановяване на лечението .
В допълнение към периферната невропатия, автономната невропатия може да допринесе за появата на някои нежелани реакции, като постурална хипотония и тежък илеус запек. Все още има ограничена информация за автономната невропатия и нейния принос за тези странични ефекти.
Конвулсии
Нечесто се съобщава за припадъци при пациенти без анамнеза за гърчове или епилепсия. Необходимо е специално внимание при лечение на пациенти с риск от припадъци.
Хипотония
Лечението с VELCADE обикновено се свързва с ортостатична / постурална хипотония. Повечето нежелани реакции са леки до умерени по тежест и са наблюдавани по време на лечението. Пациентите, които са имали ортостатична хипотония с VELCADE (инжектиран интравенозно), не са имали предишни епизоди на ортостатична хипотония преди лечението. При повечето пациенти е била необходима терапия за лечение на ортостатична хипотония.Малшинство от пациентите с ортостатична хипотония са имали епизоди на синкоп.
Механизмът на това събитие е неизвестен, въпреки че компонент може да бъде определен чрез автономна невропатия. Автономната невропатия може да бъде свързана с бортезомиб или е възможно лекарството да влоши вече съществуващо състояние, като диабетна или амилоидозна невропатия. Трябва да се използва изключително внимание при лечението на пациенти с анамнеза за синкоп, лекувани с лекарства, за които е известно, че са свързани с хипотония, или пациенти, които проявяват дехидратация в резултат на повтаряща се диария или повръщане. антихипертензивни лекарства, рехидратация или приложение на минералокортикостероиди и / или симпатикомиметични лекарства.Пациентите трябва да бъдат посъветвани да се консултират с лекаря си при замайване, замаяност или кратки епизоди на припадък.
Синдром на обратна обратима енцефалопатия (PRES)
Има съобщения за PRES при пациенти, получаващи VELCADE. PRES е рядка неврологична форма, характеризираща се с бърза, често обратима еволюция, която може да се прояви с гърчове, хипертония, главоболие, летаргия, объркване, слепота и други визуални и неврологични промени. Диагнозата се потвърждава от радиологични изображения на мозъчните структури, за предпочитане получени с ядрено -магнитен резонанс (ЯМР). При пациенти, развиващи PRES, лечението с VELCADE трябва да се преустанови.
Сърдечна недостатъчност
По време на лечението с бортезомиб се наблюдава остро начало или влошаване на застойна сърдечна недостатъчност и / или развитие на намалена фракция на изтласкване на лявата камера. Задържането на течности може да бъде предразполагащ фактор за признаци и симптоми на сърдечна недостатъчност. Пациенти със сърдечна недостатъчност или с рискови фактори за сърдечна недостатъчност трябва да се следи внимателно.
Електрокардиографски изследвания
В клинични проучвания са наблюдавани единични случаи на удължаване на QT интервала, чиято причинно -следствена връзка не е установена.
Белодробни изменения
Редки случаи на остра дифузна инфилтративна белодробна болест с неизвестна етиология, като пневмония, интерстициална пневмония, белодробна инфилтрация и остър респираторен дистрес синдром (ARDS), са съобщени при пациенти, получаващи VELCADE (вж. Точка 4.8). Някои от тези епизоди са фатални. Рентгенография на гръдния кош преди лечението се препоръчва като изходна база за потенциални белодробни промени след лечението.
В случай на поява или влошаване на белодробните симптоми (например кашлица, диспнея), трябва да се извърши бърза диагностична оценка на пациента и последващо подходящо лечение. Съотношението полза / риск трябва да се вземе предвид преди да продължите терапията с VELCADE.
По време на клинично проучване двама от двама пациенти, получаващи високи дози цитарабин (2 g / m² на ден) като 24-часова непрекъсната инфузия в комбинация с даунорубицин и VELCADE за лечение на рецидивираща остра миелоидна левкемия, умират поради ARDS. началната фаза на терапията, проучването е спряно. Следователно този специфичен режим на комбинирана терапия с висока доза цитарабин (2 g / m² на ден) в непрекъсната 24 -часова инфузия не се препоръчва.
Нарушена бъбречна функция
Бъбречните усложнения са чести при пациенти с множествен миелом. Пациентите с бъбречна недостатъчност трябва да бъдат внимателно наблюдавани (вж. Точки 4.2 и 5.2).
Нарушена чернодробна функция
Бортезомиб се метаболизира от чернодробните ензими. При пациенти с умерено или тежко чернодробно увреждане експозицията на бортезомиб се увеличава; такива пациенти трябва да бъдат лекувани с намалена доза VELCADE и трябва да бъдат внимателно проследявани за всяка проява на токсичност (вж. Точки 4.2 и 5.2.).
Чернодробни реакции
Съобщавани са редки случаи на чернодробна недостатъчност при пациенти, получаващи VELCADE и съпътстващи лекарствени терапии, и с тежко основно заболяване.Съобщавани са и други чернодробни реакции като повишени чернодробни ензими, хипербилирубинемия и хепатит. Тези промени могат да бъдат обратими след преустановяване на лечението с бортезомиб (вж. Точка 4.8).
Синдром на туморен лизис
Тъй като бортезомиб е цитотоксично вещество и следователно е способен бързо да унищожава злокачествени плазмени клетки и MCL клетки, могат да се наблюдават усложнения от синдрома на туморен лизис. Пациентите с риск от развитие на синдром на туморен лизис са тези, които са показали висока туморна тежест преди започване на лечението. Тези пациенти трябва да бъдат внимателно наблюдавани и да се вземат предпазни мерки.
Едновременното приложение на други лекарства
Пациентите на едновременно лечение с бортезомиб и мощни инхибитори на CYP3A4 трябва да бъдат внимателно наблюдавани. Трябва да се внимава особено при едновременно приложение на бортезомиб и субстрати на CYP3A4 или CYP2C19 (вж. Точка 4.5).
Нормалната чернодробна функция трябва да бъде потвърдена при пациенти, приемащи перорални хипогликемици и лекувани с повишено внимание (вж. Точка 4.5).
Потенциално имунокомплексни медиирани реакции
Нечесто се съобщава за потенциални реакции, свързани с имунния комплекс, като серумна болест, полиартрит с обрив и пролиферативен гломерулонефрит. Приложението на бортезомиб трябва да се преустанови в случай на сериозни събития.
04.5 Взаимодействия с други лекарствени продукти и други форми на взаимодействие -
Образование инвитро показват, че бортезомиб е слаб инхибитор на изоензимите на цитохром Р450 (CYP) 1A2, 2C9, 2C19, 2D6 и 3A4. Като се има предвид ограниченият принос (7%) на изоензима CYP2D6 в метаболизма на бортезомиб, се смята, че този ниско метаболизиращ фенотип не влияе върху общата наличност на бортезомиб.
Проучване за взаимодействие лекарство-лекарство, основано на данни от 12 пациенти, за да се изследва ефекта на кетоконазол, мощен инхибитор на CYP3A4, върху фармакокинетиката на бортезомиб (инжектиран интравенозно), показва средно увеличение на AUC. 35% бортезомиб (90% CI [ 1.032-1.772)] Следователно, пациентите, получаващи едновременно лечение с бортезомиб и мощни инхибитори на CYP3A4 (напр. Кетоконазол, ритонавир), трябва да бъдат внимателно наблюдавани.
В проучване за взаимодействие лекарство-лекарство, въз основа на данни от 17 пациенти, за изследване на ефекта на омепразол, мощен инхибитор на CYP2C19, върху фармакокинетиката на бортезомиб (инжектиран интравенозно), няма доказателства за ефект. Значим върху фармакокинетиката на бортезомиб .
Клинично проучване за лекарствено взаимодействие, основано на данни от 6 пациенти, за да се изследва ефекта на рифампицин, мощен индуктор на CYP3A4, върху фармакокинетиката на бортезомиб (инжектиран интравенозно), показва средно намаление на AUC. 45% бортезомиб. Следователно, едновременното употребата на бортезомиб с мощни индуктори на CYP3A4 (напр. рифампицин, карбамазепин, фенитоин, фенобарбитал и жълт кантарион) не се препоръчва, тъй като ефикасността може да бъде намалена.
В същото клинично проучване за лекарствено взаимодействие, върху данни от 7 пациенти, за да се провери ефекта на дексаметазон, слаб индуктор на CYP3A4, върху фармакокинетиката на бортезомиб (инжектиран интравенозно), няма значителен ефект върху фармакокинетиката на бортезомиб.
Проучване за взаимодействие лекарство-лекарство, основано на данни от 21 пациенти, за оценка на ефекта на мелфалан-преднизон върху фармакокинетиката на бортезомиб (инжектиран интравенозно), показва увеличение на AUC на бортезомиб със 17%.
Това не се счита за клинично значимо.
В клинични проучвания хипогликемия и хипергликемия се съобщават рядко при пациенти с диабет, приемащи перорални хипогликемични лекарства. Пациентите на перорална антидиабетна терапия, получаващи VELCADE, може да изискват внимателно проследяване на кръвната захар и корекция на дозата на антидиабетните лекарства.
04.6 Бременност и кърмене -
Контрацепция при мъже и жени
Мъжете и жените с детероден потенциал трябва да използват подходящи контрацептивни мерки по време на приложението и в продължение на 3 месеца след лечението.
Бременност
Няма налични клинични данни за експозиция на бортезомиб по време на бременност.Тератогенният потенциал на бортезомиб не е напълно проучен.
В предклинични проучвания, прилагането на бортезомиб в максимално поносими дози от майката не показва ефект върху ембрионално -феталното развитие при плъхове и зайци. Не са провеждани проучвания върху животни, за да се установи ефект върху раждането и постнаталното развитие (вж. Точка 5.3). VELCADE не трябва да се използва по време на бременност, освен ако клиничното състояние на пациента налага използването му.
Пациентката трябва да бъде информирана за потенциалните рискове за плода, ако VELCADE се прилага по време на бременност, или ако пациентката забременее по време на лечението.
Талидомид е мощен тератоген при хора и предизвиква тежки животозастрашаващи вродени дефекти. програмата за превенция на бременността с талидомид Вижте Резюме на характеристиките на продукта на талидомид за допълнителна информация.
Време за хранене
Не е известно дали бортезомиб се екскретира в кърмата. Поради възможността от сериозни нежелани реакции на VELCADE при кърмачета, кърменето трябва да се преустанови по време на терапията с VELCADE.
Плодовитост
Не са провеждани проучвания за фертилитета с VELCADE (вж. Точка 5.3).
04.7 Ефекти върху способността за шофиране и работа с машини -
VELCADE може да повлияе умерено способността за шофиране или работа с машини.
VELCADE може много често да се свързва с умора, често със замаяност, рядко със синкоп, често с ортостатична / постурална хипотония или замъглено зрение. Пациентите трябва да бъдат изключително внимателни при шофиране или работа с машини (вж. Точка 4.8).
05.0 ФАРМАКОЛОГИЧНИ СВОЙСТВА -
05.1 "Фармакодинамични свойства -
Фармакотерапевтична група: антинеопластични лекарства, други антинеопластични лекарства.
ATC код: L01XX32.
Механизъм на действие
Бортезомиб е протеазомен инхибитор. Специално е показано, че инхибира химотрипсиноподобната активност на 26S протеазомата в клетките на бозайници. 26S протеазомата е голям полипептиден комплекс, отговорен за разграждането на убиквитинирани протеини. Убиквитин-протеазомният метаболитен път играе съществена роля за контролиране на оборота специфични протеини, като по този начин се поддържа хомеостазата в клетките. Инхибирането на 26S протеазомата предотвратява тази насочена протеолиза и засяга предаването на сигнала в клетката, което води до смърт на раковите клетки.
Бортезомиб е силно селективен за протеазомата. При концентрации от 10 mcM бортезомиб не инхибира нито един от многото оценени рецептори и протеази и е повече от 1500 пъти по -селективен за протеазомата от втория целеви ензим. Оценена е кинетиката на инхибиране на протеозомите инвитро и бортезомиб се дисоциира от протеазомата с t½ от 20 минути, като по този начин демонстрира, че инхибирането на бортезомиб е обратимо.
Бортезомиб-медиираното инхибиране на протеазомата има многобройни ефекти върху раковите клетки, включително, но не само, промяната на регулаторните протеини, които контролират прогресията на клетъчния цикъл и "активирането на ядрения фактор kB (NF-kB). Инхибирането на L" на протеазомата води до спиране на клетъчния цикъл и апоптоза.
NF-kB е транскрипционен фактор, чието активиране се изисква на много етапи от канцерогенезата, включително клетъчен растеж и оцеляване, ангиогенеза, клетъчно взаимодействие и метастази. При миелом бортезомиб влияе върху способността на миеломните клетки да взаимодействат с микросредата на костния мозък.
Проучванията показват, че бортезомиб е цитотоксичен за множество видове ракови клетки и че тези клетки са много по -чувствителни към проапоптотичните ефекти на инхибирането на протеазомите от нормалните. Бортезомиб причинява намаляване на туморния растеж. in vivo в много предклинични модели на рак, включително множествен миелом.
Данни in vitro, ex vivo и при животински модели предполагат, че бортезомиб повишава остеобластната диференциация и активност и инхибира остеокластичната функция.Тези ефекти са наблюдавани при пациенти с множествена миелома с напреднала остеолитична болест и лекувани с бортезомиб.
Клинична ефикасност при преди това нелекуван множествен миелом
Международно, рандомизирано (1: 1), отворено, проспективно фазово III (MMY-3002 VISTA) клинично проучване е проведено при 682 пациенти, за да се прецени дали VELCADE (Vc) (1,3 mg / m², инжектиран интравенозно) в комбинация с мелфалан ( М) (9 mg / m²) и преднизон (P) (60 mg / m²) подобряват времето до прогресия (TTP) в сравнение с мелфалан (9 mg / m²) и преднизон (60 mg / m²) при пациенти с преди това нелекуван множествен миелом . Лечението е продължило до 9 цикъла (приблизително 54 седмици) и е било прекратено рано в случай на прогресия на заболяването или неприемлива токсичност. В проучването средната възраст на пациентите е 71 години, 50% са мъже, 88% са от бялата раса, а средната оценка на състоянието на пациентите по Karnofsky е 80. Пациентите са имали IgG / IgA / миелом с лека верига при 63% / 25 % / 8% от случаите, среден хемоглобин от 105 g / l и среден брой на тромбоцитите 221,5 x 109 / l. В двете групи процентът на пациентите с креатининов клирънс ≤ 30 е подобен. Ml / min ( 3% във всяка ръка).
По време намеждинен анализ планиран, първичната крайна точка, времето до прогресиране, е достигната и на пациентите в рамото M + P е предложено лечение с Vc + M + P. Средното проследяване е 16,3 месеца. След средно проследяване Крайната преживяемост е актуализирана в продължение на 60,1 месеца. Статистически значима полза от преживяемостта се наблюдава в полза на групата на лечение с Vc + M + P (HR = 0,695, p = 0,00043) въпреки последващите терапии, включително схеми, базирани на VELCADE. Средна преживяемост при лечението с Vc + M + P групата е била 56,4 месеца в сравнение с 43,1 месеца в групата на лечение с M + P. Резултатите от ефикасността са показани в Таблица 11.
Таблица 11: Резултати от ефикасността след окончателно актуализиране на данните за оцеляване на VISTA
Пациенти кандидати за трансплантация на стволови клетки
Две рандомизирани, отворени фаза III многоцентрови клинични изпитвания (IFM-2005-01, MMY-3010) бяха проведени, за да демонстрират безопасността и ефикасността на VELCADE в двойна и тройна комбинация с други химиотерапевтични средства като индукционна терапия преди трансплантация на стволови клетки при пациенти преди това не лекуван от множествен миелом.
В проучване IFM-2005-01 VELCADE в комбинация с дексаметазон [VcDx, n = 240] е сравнен с винкристин-доксорубицин-дексаметазон [VDDx, n = 242]. Пациентите в групата на VcDx са получили четири 21-дневни цикъла, всеки от които се състои от VELCADE (1,3 mg / m², прилаган интравенозно два пъти седмично на 1, 4, 8 и 11 ден) и перорален дексаметазон (40 mg / m2) на ден на дни 1 до 4 и на дни 9 до 12, в цикли 1 и 2 и в дни 1 до 4 в цикли 3 и 4).
Сто деветдесет и осем пациенти (82%) и 208 пациенти (87%) съответно в VDDx и VcDx групите са претърпели автоложна трансплантация на стволови клетки; повечето пациенти са претърпели единична трансплантация. Демографията на пациента и изходните характеристики на заболяването са сходни между двете лечебни групи. В проучването средната възраст на пациентите е 57 години, 55% са мъже и 48% от пациентите са с висок цитогенетичен риск.Средната продължителност на лечението е 13 седмици за групата VDDx и 11 седмици за групата VDDx. VcDx Средният брой цикли, получени от двете групи, е 4 цикъла.
Първичната крайна точка на ефикасността на проучването е степента на индукционен отговор (CR + nCR). Статистически значима разлика в CR + nCR се наблюдава в полза на групата VELCADE в комбинация с дексаметазон. Вторичните крайни точки на ефикасност включват процент отговор (CR + nCR, CR + nCR + VGPR + PR) след трансплантация, преживяемост без прогресия и обща преживяемост Основните резултати от ефикасността са представени в Таблица 12.
Таблица 12: Резултати от ефикасността в проучване IFM-2005-01
В проучване MMY-3010 VELCADE в комбинация с талидомид и дексаметазон [VcTDx, n = 130] се сравнява с талидомид-дексаметазон [TDx, n = 127]. Пациентите в групата на VcTDx са получили шест 4-седмични цикъла, всеки от които се състои от VELCADE (1,3 mg / m², прилаган два пъти седмично на 1, 4, 8 и 11 ден, последван от период на почивка от 17 дни от 12 до 28), дексаметазон (40 mg, прилагани перорално на ден 1 до 4 и дни 8 до 11), и талидомид (50 mg дневно, прилаган перорално на дни 1-14, като дозата се увеличава до 100 mg на дни 15-28 и след това при 200 mg на ден ден).
Сто и пет пациенти (81%) и 78 пациенти (61%) в групите VcTDx и TDx съответно. те са претърпели единична автоложна трансплантация на стволови клетки. Демографията на пациента и изходните характеристики на заболяването са сходни между двете лечебни групи. Пациентите в групите VcTDx и TDx съответно са имали средна възраст 57 и 56 години, 99% и 98% от пациентите са били от бялата раса; 58% и 54% са мъже. В групата с VcTDx 12% от пациентите са цитогенетично класифицирани като високорискови в сравнение с 16% от пациентите в групата на TDx. Средната продължителност на лечението е 24,0 седмици, а средният брой на получените цикли на лечение е 6,0 и е постоянен в групите на лечение.
Първичните крайни точки за ефикасност на проучването са процентите на отговор след индукция и посттрансплантационен отговор (CR + nCR). Статистически значима разлика в CR + nCR се наблюдава в полза на лекуваната група с VELCADE в комбинация с дексаметазон и талидомид. Вторичните крайни точки за ефикасност включват преживяемост без прогресия и обща преживяемост. Основните резултати от ефикасността са представени в таблица 13.
Таблица 13: Резултати от ефикасността от проучване MMY-3010
Клинична ефикасност при пациенти с рецидивиращ или рефрактерен множествен миелом
Профилите на безопасност и ефикасност на VELCADE (инжектиран интравенозно) бяха оценени в две проучвания при препоръчителната доза от 1,3 mg / m²: рандомизирано, контролирано дексаметазон (Dex) фаза III (APEX), проведено при 669 пациенти с рецидивиращ и рефрактерен множествен миелом , които са преминали 1 до 3 предишни линии на лечение и еднофазово проучване фаза II, проведено при 202 пациенти с рецидивиращ и огнеупорен множествен миелом, които са преминали поне две предишни линии на лечение с прогресия на заболяването след последната терапия.
Във фаза III проучване при всички пациенти, включително тези, които са получили само една предходна линия на лечение, лечението с VELCADE е довело до значително удължаване на времето до прогресия, значително удължаване на преживяемостта и значително увеличаване на степента на отговор. в сравнение с лечението с дексаметазон (вж. Таблица 14).
Въз основа на данните, получени от "междинен анализ Предварително планиран, Комитетът за наблюдение препоръча прекратяване на лечението с дексаметазон в полза на лечението с VELCADE за всички пациенти, рандомизирани на лечение с дексаметазон, независимо от състоянието на заболяването. на рамото на VELCADE, общата преживяемост е по -дълга и процентът на отговор е по -висок както при пациентите, които са били рефрактерни на последната им терапия, така и при тези, които не са го направили.
От 669 записани пациенти, 245 (37%) са били на 65 или повече години. Параметрите на отговора, както и TTP бяха значително по-добри за VELCADE независимо от възрастта.
В огнеупорна популация от фаза II на проучванията отговорите са оценени от независима комисия и се прилагат критериите за отговор. от Европейската група за трансплантация на костен мозък. Средната обща преживяемост на всички пациенти, включени в проучването, е 17 месеца (диапазон на състоянието на ефективност, от статуса на делеция на хромозома 13 или от броя или вида на предишните терапии. Степента на отговор на пациентите, вече преминали 2-3 или повече от 7 линии на лечение това е съответно 32% (10/32) и 31% (21/67).
Таблица 14: Обобщение на резултатите от ефикасността от Фаза III (APEX) и II проучвания
Във фаза II на проучването пациентите, които не са постигнали оптимален отговор на монотерапията с VELCADE, са лекувани с високи дози дексаметазон и VELCADE. Протоколът позволява на пациенти, които са постигнали по -малко от оптимален отговор на монотерапия с VELCADE, да получават дексаметазон.
Общо 74 пациенти, подлежащи на оценка, са лекувани с дексаметазон и VELCADE. Комбинираното лечение направи възможно получаването на отговор или подобрение на отговора [MR 11% или PR 7%] при 18% от пациентите.
Клинична ефикасност при пациенти с рецидивиращ / рефрактерен множествен миелом с подкожно приложение на VELCADE
Открито, рандомизирано, рандомизирано клинично изпитване от фаза III, което не е по-малко, сравнява ефикасността и безопасността на подкожното приложение на VELCADE с интравенозното приложение.Това проучване включва 222 пациенти с рецидивиращ / рефрактерен множествен миелом, рандомизирани в съотношение 2: 1 1,3 mg / m² VELCADE подкожно или интравенозно за 8 цикъла.За тези пациенти, които не са постигнали оптимален отговор само на VELCADE (по -малко от пълния отговор [CR]) след 4 цикъла, им е било позволено да получават 20 mg дексаметазон на деня на приложението на VELCADE и на следващия ден.Пациенти с изходна степен ≥ 2 периферна невропатия или брой на тромбоцитите
Това проучване постига основната цел на непълноценност, оценена по отношение на степента на отговор (CR + PR) след 4 цикъла на монотерапия с VELCADE както за подкожно, така и за интравенозно приложение, като процентът на отговор е 42% и при двата. В допълнение, вторични крайни точки за ефикасност свързани с отговора и времето до събитието показват последователни резултати както за подкожния, така и за интравенозния път (Таблица 15).
Таблица 15: Обобщение на анализите на ефикасността, сравняващи подкожно и интравенозно приложение на VELCADE
Лечение с VELCADE в комбинация с пегилиран липозомен доксорубицин (проучване DOXIL-MMY-3001)
Открито, рандомизирано, многоцентрово проучване от фаза III на паралелна група беше проведено при 646 пациенти, сравняващо безопасността и ефикасността на VELCADE плюс пегилиран липозомален доксорубицин срещу монотерапия с VELCADE при пациенти с множествена миелома, които преди това са получавали поне 1 терапия и които не са показа прогресия на заболяването по време на антрациклинова терапия. Първичната крайна точка за ефикасност беше време до прогресия (TTP), докато вторичните крайни точки за ефикасност бяха общата преживяемост (OS) и общата степен на отговор (ORR: (пълен отговор + частичен отговор), използвайки критериите на "Европейска група за кръв и мозък Трансплантация (EBMT).
Резултатите от „междинен анализ дефиниран от протокола (въз основа на 249 TTP събития) доведе до преждевременно прекратяване на проучването за ефикасност. Този междинен анализ показа 45% намаление на риска от TTP (95% CI; 29-57%, стр
Окончателният анализ за обща преживяемост (ОС), извършен след средно проследяване от 8,6 години, не показва значителна разлика в ОС между двете терапевтични групи. Средната ОС е 30,8 месеца (95% ДИ; 25,2-36,5 месеца) за пациенти на VELCADE монотерапия и 33,0 месеца (95% ДИ; 28,9-37,1 месеца) за пациенти на комбинирана терапия с VELCADE и пегилиран липозомален доксорубицин.
Лечение с VELCADE в комбинация с дексаметазон
При липса на директно сравнение между VELCADE и VELCADE в комбинация с дексаметазон при пациенти с прогресиращ множествен миелом, беше извършен „сдвоен статистически анализ“, за да се сравнят резултатите от нерандомизираното рамо на VELCADE в комбинация с дексаметазон (фаза II на проучването отворен етикет MMY-2045), с резултати, получени в рамената за лечение с монотерапия VELCADE от различни фазови III рандомизирани проучвания (M34101-039 [APEX] и DOXIL MMY-3001) в същото показание.
Анализът на съвпадената двойка е статистически метод, при който пациентите в лекуваната група (напр. VELCADE в комбинация с дексаметазон) и пациентите в сравнителната група (напр. VELCADE) са сравними по отношение на объркващите фактори чрез индивидуално сдвояване на изследваните субекти. Този метод свежда до минимум ефектите от объркващи фактори, наблюдавани при оценката на ефектите от лечението, като се използват нерандомизирани данни.
Идентифицирани са 127 двойки двойки пациенти. Анализът показа подобрение в общия процент на отговор (ORR: CR + PR) (съотношение на шансовете 3.769; 95% CI 2.045-6.947; p
Има ограничена информация за повторно лечение с VELCADE при рецидивиращ множествен миелом.
Проведено е фаза II MMY-2036 (RETRIEVE), едноръчно проучване с отворен етикет, за да се определи ефикасността и безопасността на повторното лечение с VELCADE. Сто и тридесет пациенти (на възраст ≥ 18 години) с множествен миелом, които преди това са имали поне един частичен отговорът на режим, съдържащ VELCADE, е оттеглен след прогресиране.Най -малко 6 месеца след предишната терапия, VELCADE е започнат при последната поносима доза от 1,3 mg / m² (n = 93) или ≤ 1,0 mg / m² (n = 37) и е приложен в дни 1, 4, 8 и 11 на всеки 3 седмици в продължение на до 8 цикъла, като монотерапия или в комбинация с дексаметазон според стандартната терапия. Дексаметазон е прилаган в комбинация с VELCADE на 83 пациенти в цикъл 1 и още 11 пациенти са получавали дексаметазон по време на следващите цикли на повторно лечение VELCADE.
Първичната крайна точка е най -добре потвърденият отговор на повторно лечение според критериите на EBMT.Най -добрият общ процент на отговор (CR + PR) за повторно лечение при 130 пациенти е 38,5% (95% CI: 30,1; 47)., 4).
Клинична ефикасност при пациенти, които преди това не са били лекувани с мантийно -клетъчен лимфом (MCL)
LYM-3002 е фаза III, рандомизирано, отворено проучване, сравняващо ефикасността и безопасността на комбинацията от VELCADE, ритуксимаб, циклофосфамид, доксорубицин и преднизон (VcR-CAP; n = 243) с тези на ритуксимаб, циклофосфамид, доксорубицин, винкристин и преднизон (R-CHOP; n = 244) при нелекувани преди това възрастни пациенти с MCL (Етап II, III или IV). Пациентите в рамото за лечение с VcR-CAP са получавали VELCADE (1,3 mg / m²; в дни 1, 4, 8, 11, период на почивка 12-21), ритуксимаб 375 mg / m² IV на ден 1; циклофосфамид 750 mg / m² IV на ден 1; доксорубицин 50 mg / m² IV на ден 1 и преднизон 100 mg / m² перорално в дни 1 до 5 от 21-дневния цикъл на лечение с VELCADE. Пациентите с документиран първи отговор на цикъл 6 са получили два допълнителни курса на лечение.
Първичната крайна точка за ефикасност е преживяемостта без прогресия на базата на оценка на Независим комитет за преглед (IRC). Вторичните крайни точки включват време до прогресия (TTP), време до следващото лечение с анти-лимфом (TNT), продължителност на "интервала без лечение (TFI) ), общ процент на отговор (ORR) и пълен процент на отговор (CR / CRu), обща преживяемост (OS) и продължителност на отговора.
Демографските и изходните характеристики на заболяването като цяло бяха добре балансирани между двете рамена на лечение: средната възраст на пациентите беше 66 години, 74% бяха мъже, 66% бяха бели и 32% азиатски, 69% от пациентите. / или MCL положителна биопсия на костен мозък, 54% от пациентите са имали рейтинг на Международния прогностичен индекс (IPI) ≥ 3, а 76% са имали стадий IV заболяване. Продължителността на лечението (медиана = 17 седмици) и продължителността на проследяването (медиана = 40 месеца) са сравними в двете рамена на лечение. Пациентите в двете терапевтични рамена получават медиана от 6 цикъла, като 14% от пациентите в групата на VcR-CAP и 17% от пациентите в групата R-CHOP получават допълнителните 2 цикъла. Повечето пациенти и в двете групи са завършили лечението, 80% в групата VcR-CAP и 82% в групата R-CHOP. Резултатите от ефикасността са представени в таблица 16:
Таблица 16: Резултати от ефикасността от изследване LYM-3002
Средният PFS, определен от изследователя, е 30,7 месеца в групата с VcR-CAP и 16,1 месеца в групата R-CHOP (коефициент на опасност [HR] = 0,51; p
Средната продължителност на пълния отговор е 42,1 месеца в групата с VcR-CAP в сравнение с 18 месеца в групата с R-CHOP. Общата продължителност на отговора е била с 21,4 месеца по-дълга в групата с VcR-CAP (медиана 36,5 месеца срещу 15,1 месеца в групата R-CHOP). При средна продължителност на проследяване от 40 месеца, средната обща преживяемост (ОС) е в полза на VcR-CAP (56,3 месеца в групата R-CHOP и не е постигната в групата на VcR-CAP), (HR оценка = 0,80; р = 0,173). Наблюдава се тенденция към удължаване на общата преживяемост в полза на групата VcR-CAP; очакваната 4-годишна преживяемост е 53,9% в групата на R-CHOP и 64,4% в групата на VcR-CAP.
Пациенти с лекувана преди това амилоидоза с лека верига (AL)
Беше проведено открито, нерандомизирано проучване фаза I / II за определяне на безопасността на VELCADE при пациенти с амилоидоза, лекувана преди това с лека верига (AL). По време на проучването не бяха наблюдавани нови опасения за безопасността и по -специално VELCADE не доведе до влошаване на увреждането на органите (сърце, бъбреци и черен дроб).
В проучвателен анализ на ефикасността за двете свързани дозови кохорти е докладвана степен на отговор от 67,3% (от които 28,6% пълен отговор) по отношение на хематологичния отговор (протеин М), при 49 оценени пациенти, лекувани с максимално разрешените дози от 1,6 mg / m² веднъж седмично и 1,3 mg / m² два пъти седмично.За двата свързани курса на дози, едногодишната преживяемост е 88,1%.
Педиатрична популация
Европейската агенция по лекарствата се отказа от задължението да представи резултатите от проучванията с VELCADE във всички подгрупи на педиатричната популация с множествен миелом и мантийно -клетъчен лимфом (вж. Точка 4.2 за информация относно педиатричната употреба).
05.2 "Фармакокинетични свойства -
Абсорбция
След интравенозно болусно приложение на 1,0 mg / m² и 1,3 mg / m² на 11 пациенти с множествен миелом и стойности на креатининов клирънс над 50 ml / min, средните максимални плазмени концентрации на бортезомиб при първите дози са 57 и 112 ng / mL , съответно. При следващи дози средните максимални наблюдавани плазмени концентрации варират от 67 до 106 ng / mL за дозата от 1,0 mg / m² и между 89 и 120 ng / mL за дозата от 1,3 mg / m².
След многократно интравенозно болус или подкожно инжектиране на доза от 1,3 mg / m² при пациенти с множествен миелом (n = 14 във венозната група, n = 17 в подкожната група), общата системна експозиция на лекарството (AUClast) е еквивалентна за подкожната и интравенозни пътища на приложение Cmax след подкожно приложение (20,4 ng / ml) е по -ниско от интравенозно (223 ng / ml). Средното геометрично съотношение AUC е 0,99 и с 90% доверителни интервали те са 80,18% - 122,80%.
Разпределение
При пациенти с множествен миелом средният обем на разпределение (Vd) на бортезомиб варира от 1659 до 3294 l след еднократно или многократно интравенозно дозиране при 1,0 mg / m² или 1,3 mg / m². Това предполага, че бортезомиб е широко разпространен в периферните тъкани. В диапазон на концентрация на бортезомиб от 0,01 до 1,0 μg / ml, свързващ се с човешки плазмени протеини инвитро той е средно 82.9%. Свързаната с плазмените протеини фракция на бортезомиб не зависи от концентрацията.
Биотрансформация
Образование инвитро върху човешките чернодробни микрозоми и върху цитохром Р450 изоензимите, експресирани от човешка с-ДНК, показват, че бортезомиб основно претърпява окислителен метаболизъм чрез ензимите на цитохром Р450, 3А4, 2С19 и 1А2. Основният метаболитен път се състои от деборониране, което води до два обеборирани метаболита, които впоследствие се хидроксилират до различни метаболити. Деборираните метаболити на бортезомиб са неактивни като инхибитори на 26S протеазомата.
Елиминиране
Средният елиминационен полуживот (t1 / 2) на бортезомиб по време на лечението с много дози варира от 40 до 193 часа. Бортезомиб се изчиства по-бързо след първата доза, отколкото при следващите дози. Средният общ клирънс е 102 и 112 l / h след първата доза от 1,0 mg / m² и 1,3 mg / m² съответно и между 15 и 32 l / h и между 18 и 32 l / h за следващи дози от 1,0 mg / m² и 1,3 mg / m², съответно.
Специални популации
Чернодробна недостатъчност
Ефектът на чернодробната недостатъчност върху фармакокинетиката на бортезомиб е проучен във фаза I клинично проучване при 61 пациенти с първични солидни тумори с различна степен на чернодробно увреждане и лекувани с дози бортезомиб, включително между 0,5 и 1,3 mg / m².
Леката чернодробна недостатъчност не променя нормализираната дозата AUC на бортезомиб в сравнение с тази, наблюдавана при пациенти с нормална чернодробна функция. При пациенти с умерено или тежко чернодробно увреждане, нормализираните от дозата средни стойности на AUC се увеличават с приблизително 60% .При пациенти с умерено или тежко чернодробно увреждане се препоръчва по-ниска начална доза. раздел 4.2, Таблица 6).
Бъбречна недостатъчност
Проведено е фармакокинетично проучване при пациенти с различна степен на бъбречно увреждане, които са класифицирани по стойностите на креатининовия клирънс (CrCL) в следните групи: Нормални (CrCL ≥60 ml / min / 1,73 m², n = 12), Леки ( CrCL = 40-59 mL / min / 1.73 m², n = 10), умерен (CrCL = 20-39 mL / min / 1.73 m², n = 9) и тежък (интравенозен CrCL в дози от 0,7 до 1,3 mg / min) m² два пъти седмично. Експозицията на VELCADE (нормализирани дозата AUC и Cmax) е сходна при всички групи пациенти (вж. точка 4.2).
05.3 Предклинични данни за безопасност -
При концентрации
Бортезомиб не показва генотоксичност при теста за мутагенност инвитро (Тест на Еймс), нито в микроядрения тест in vivo извършва при мишки.
В проучвания за токсичност за развитието, проведени при плъхове и зайци, е установена ембриофетална смъртност при токсични за майката дози, но без ембриофетална токсичност под токсичната доза за майката. Не са провеждани проучвания за фертилитета, но е извършена оценка на репродуктивните тъкани в проучвания за обща токсичност. В шестмесечното проучване при плъхове са установени дегенеративни ефекти както върху тестисите, така и върху яйчниците. Следователно е вероятно бортезомиб да има потенциален ефект върху фертилитета при мъжете и жените. Не са провеждани проучвания за перинаталното и постнаталното развитие.
Проучвания за обща токсичност при много цикли, проведени при плъхове и маймуни, разкриха, че основните целеви органи са: стомашно -чревния тракт, което води до повръщане и / или диария; хематопоетични и лимфни тъкани, водещи до цитопения в периферната кръв, атрофия на лимфната тъкан и хематопоетична хипоцелуларност на костния мозък; периферна невропатия (наблюдавана при маймуни, мишки и кучета), засягаща аксоните на сензорните нерви; и леки промени в бъбреците. След прекратяване на лечението всички тези целеви органи показаха частично до пълно възстановяване.
Въз основа на проучвания върху животни, преминаването на бортезомиб през кръвно -мозъчната бариера изглежда ограничено и значението при хората е неизвестно.
Фармакологичните проучвания за сърдечно -съдовата безопасност, проведени при маймуни и кучета, показват, че интравенозното приложение на дози от mg / m2 2 до 3 пъти над препоръчаната от клиничната доза води до увеличаване на сърдечната честота, намаляване на сърдечната контрактилност, хипотония и смърт. При кучета намалената сърдечна контрактилност и хипотонията се контролират чрез остро лечение с положителни инотропни средства или вазопресори и се наблюдава леко увеличаване на коригирания QT интервал.
06.0 ФАРМАЦЕВТИЧНА ИНФОРМАЦИЯ -
06.1 Помощни вещества -
Манитол (E421)
Азот
06.2 Несъвместимост "-
Този лекарствен продукт не трябва да се смесва с други продукти, с изключение на споменатите в точка 6.6.
06.3 Срок на валидност "-
Неотворен флакон
3 години.
Приготвен разтвор
Готовият разтвор трябва да се използва веднага след приготвянето.
Ако не се използва незабавно, отговорност на потребителя е да се съобрази с условията и времето за съхранение на лекарствения продукт преди употреба.
Въпреки това, физическата и химическата стабилност на приготвения разтвор е доказана за 8 часа при 25 ° C, когато се съхранява в оригиналния флакон и / или в спринцовка. Общото време за съхранение на разтворения лекарствен продукт преди приложение не трябва да надвишава 8 часа.
06.4 Специални условия на съхранение -
Съхранявайте при температура не по -висока от 30 ° C.
Съхранявайте флакона във външната опаковка, за да предпазите лекарството от светлина.
За условията на съхранение след разтваряне на лекарствения продукт, вижте точка 6.3.
06.5 Естество на непосредствената опаковка и съдържанието на опаковката -
Флакон от 10 ml от стъкло тип I, със сива бромобутилова запушалка и алуминиево уплътнение, с кралско синя капачка съдържа 3,5 mg бортезомиб.
Флаконът се съдържа в прозрачен блистер, състоящ се от тава с капак.
Всяка опаковка съдържа 1 флакон за еднократна употреба.
06.6 Инструкции за употреба и боравене -
Общи предпазни мерки
Бортезомиб е цитотоксичен агент. Затова трябва да се внимава особено при работа и приготвяне на VELCADE. Препоръчително е да носите ръкавици и друго защитно облекло, за да предотвратите контакт с кожата.
Работата с VELCADE трябва да се извършва при стриктно спазване на асептичните техники поради липсата на консерванти.
Има случаи на смърт след неволно интратекално приложение на VELCADE. VELCADE 1 mg прах за инжекционен разтвор е предназначен само за интравенозно приложение, докато VELCADE 3,5 mg прах за инжекционен разтвор е предназначен за интравенозно или подкожно приложение.VELCADE не трябва да се прилага интратекално.
Инструкции за разтваряне
VELCADE трябва да се разтваря от медицински специалист.
Интравенозно инжектиране
Всеки флакон от 10 ml, съдържащ VELCADE 3,5 прах за инжекционен разтвор, трябва да се разтвори с 3,5 ml натриев хлорид 9 mg / ml (0,9%) инжекционен разтвор. Разтварянето на лиофилизирания прах отнема по -малко от 2 минути. След разтваряне всеки ml разтвор съдържа 1 mg бортезомиб. Разтвореният разтвор е бистър и безцветен, с крайно рН между 4 и 7. Приготвеният разтвор трябва да бъде визуално проверен преди прилагане, за да се провери за наличие на частици или промяна в цвета. разтворът не трябва да се използва и трябва да се изхвърли.
Подкожно инжектиране
Всеки флакон от 10 ml, съдържащ VELCADE 3,5 прах за инжекционен разтвор, трябва да се разтвори с 1,4 ml натриев хлорид 9 mg / ml (0,9%) инжекционен разтвор. Разтварянето на лиофилизирания прах отнема по -малко от 2 минути. След разтваряне всеки ml разтвор съдържа 2,5 mg бортезомиб. Разтвореният разтвор е бистър и безцветен, с крайно рН между 4 и 7. Приготвеният разтвор трябва да бъде визуално проверен преди прилагане, за да се провери за наличие на частици или промяна в цвета. разтворът не трябва да се използва и трябва да се изхвърли.
Изхвърляне
VELCADE е само за еднократна употреба.
Неизползваното лекарство и отпадъците от това лекарство трябва да се изхвърлят в съответствие с местните разпоредби.
07.0 ПРИТЕЖАТЕЛ НА „РАЗРЕШЕНИЕТО ЗА ТЪРГОВЕ“
JANSSEN-CILAG INTERNATIONAL N.V.
Turnhoutseweg, 30
B-2340 Beerse
Белгия
08.0 НОМЕР НА РАЗРЕШЕНИЕ ЗА ТЪРГОВЕ -
EU/1/04/274/001
036559019
09.0 ДАТА НА ПЪРВО РАЗРЕШЕНИЕ ИЛИ ПОДНОВЯВАНЕ НА РАЗРЕШЕНИЕТО -
Дата на първо разрешаване: 26 април 2004 г.
Дата на последното подновяване на разрешението: 26 април 2014 г.
10.0 ДАТА НА ПРЕГЛЕД НА ТЕКСТА -
04/2015








.jpg)